Clear Sky Science · pl
Wpływ elektrochemicznych procesów uzdatniania wody na korozję stali węglowej w miejskim systemie zaopatrzenia w wodę
Dlaczego rury wody z kranu mają znaczenie
Elektrochemiczne systemy uzdatniania wody stają się w miastach coraz powszechniejsze, ponieważ skutecznie usuwają zanieczyszczenia, zmiękczają wodę i niszczą drobnoustroje. Jednak te same reakcje elektryczne, które oczyszczają wodę, mogą jednocześnie powoli niszczyć metalowe rury doprowadzające ją do naszych domów. Badanie to analizuje, jak takie uzdatnianie wpływa na stal węglową, powszechny materiał rur, i wyjaśnia, dlaczego korozja może znacznie przyspieszyć, gdy prąd elektryczny oddziałuje z chemicznym składem wody z kranu.
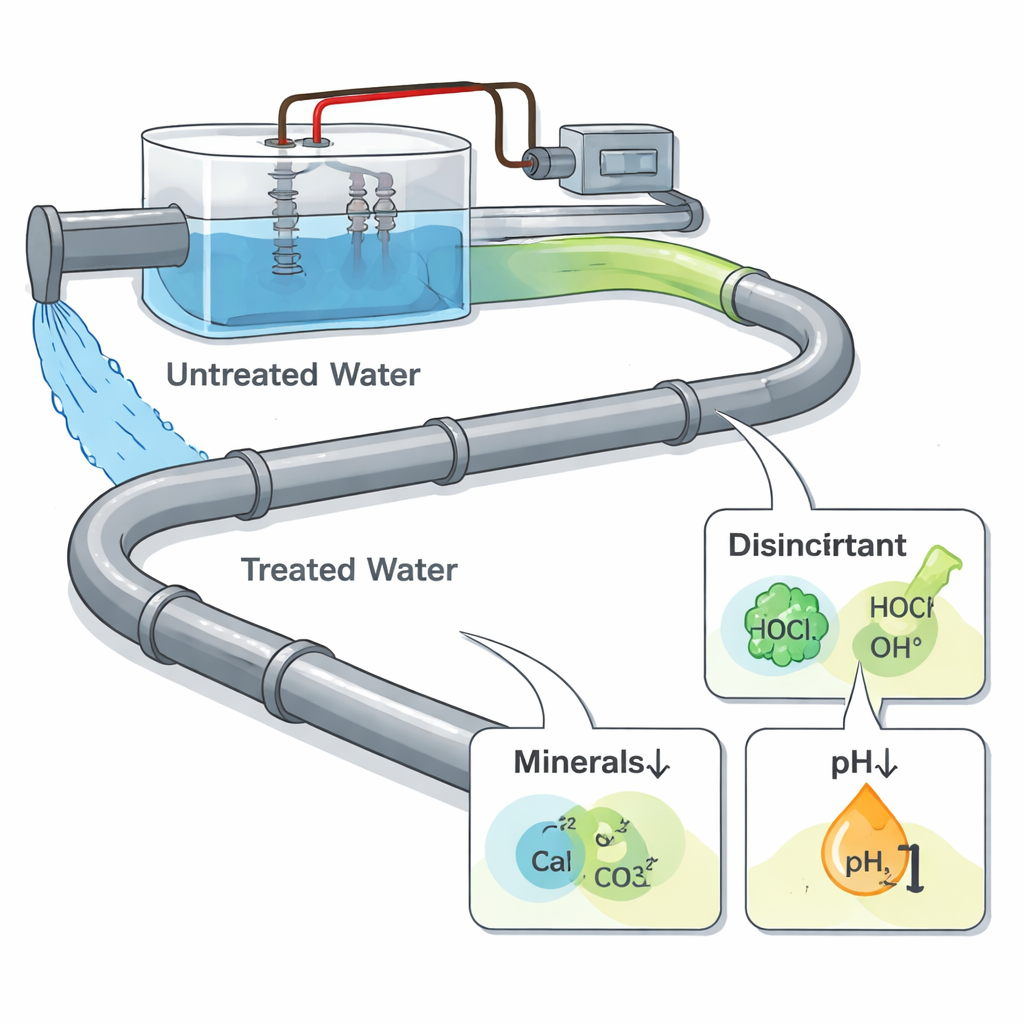
Oczyszczanie wody przy użyciu prądu
Elektrochemiczne uzdatnianie wody polega na przepuszczaniu prądu elektrycznego przez wodę za pomocą metalowych płyt zwanych elektrodami. Proces ten może usuwać niepożądane jony, rozkładać zanieczyszczenia organiczne i wytwarzać środki dezynfekujące, dlatego jest atrakcyjny dla systemów miejskich i przemysłowych. W przeciwieństwie do tradycyjnego uzdatniania, rury same w sobie nie są połączone elektrycznie z systemem — przepływa przez nie jedynie woda pochodząca z jednostki. Oznacza to, że dodatkowa korozja nie wynika z bezpośredniego działania prądu na rurę, lecz ze zmian chemii wody: powstawania nowych utleniających środków dezynfekujących, przesunięć w kwasowości oraz przemieszczania jonów mineralnych, które zwykle pomagają tworzyć ochronne warstwy wewnątrz rur.
Szybsza utrata metalu i głębsze ukryte uszkodzenia
Naukowcy przeprowadzili 90-dniowy eksperyment z użyciem rzeczywistej wody miejskiej, eksponując próbki stali węglowej na różne napięcia od 0 do 9 woltów, a następnie śledząc utratę masy, uszkodzenia powierzchni i zachowanie elektrochemiczne. Stwierdzili, że już w ciągu pierwszych trzech dni włączenie elektrolizy nasiliło korozję, a wyższe napięcie zawsze wiązało się z większymi uszkodzeniami. Przy 9 woltach ogólna szybkość korozji wzrosła ponad 25-krotnie w porównaniu z wodą, która nie przeszła procesu elektrycznego. Za pomocą skanów 3D wykazali także, że drobne jamki w metalu stawały się znacznie głębsze wraz ze wzrostem napięcia. Przy najwyższym napięciu najgłębsze jamki były niemal pięciokrotnie głębsze niż w wodzie nieuzdatnionej elektrochemicznie, co znacząco skracało spodziewany okres eksploatacji stali, nawet jeśli średnia utrata metalu nie wydawała się wyjątkowo duża.
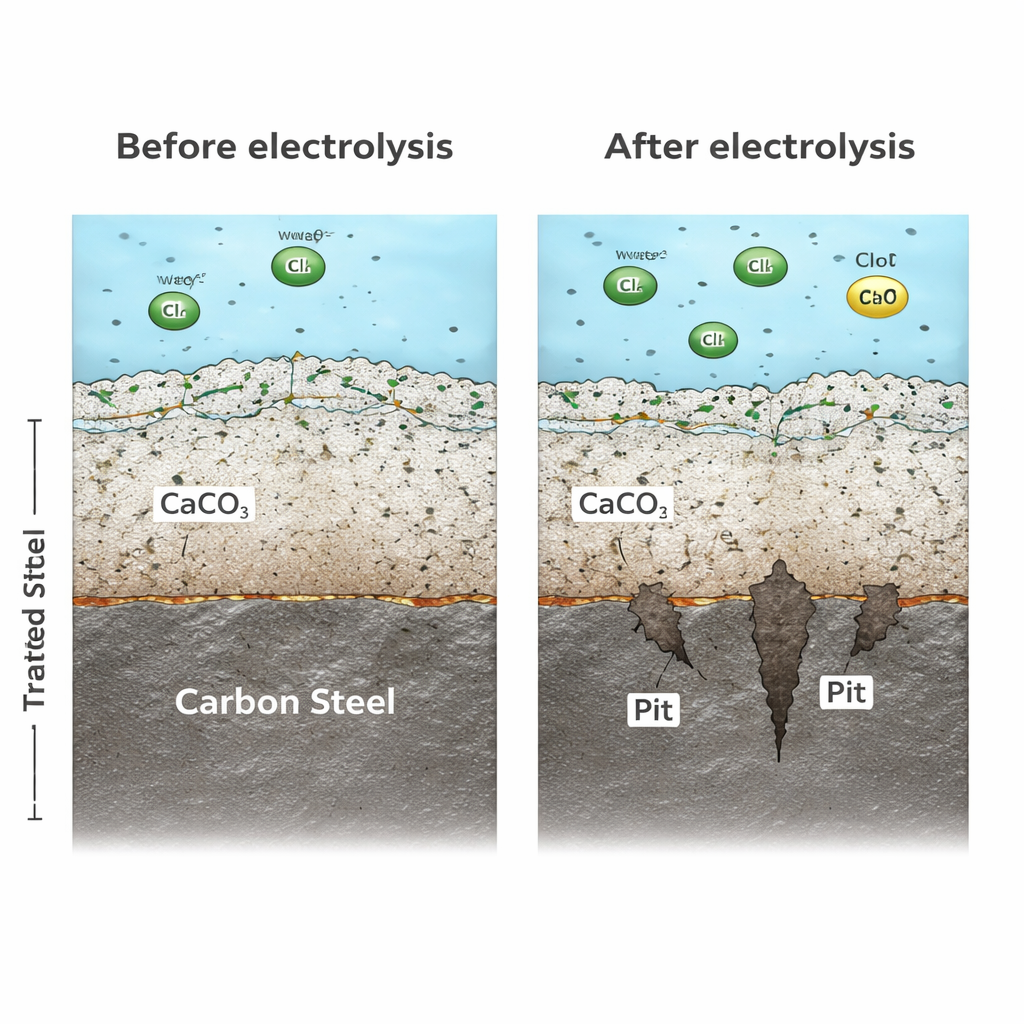
Dlaczego warstwy ochronne zawodziły
W wielu przewodach wodnych minerały zawarte w wodzie naturalnie tworzą cienką, zwartą warstwę, która pomaga osłonić metal. W wodzie nieuzdatnionej rolę tę często pełni węglan wapnia. W wodzie po elektrochemicznym uzdatnianiu ochrona ta w dużej mierze zanikała. Ponieważ katoda w jednostce uzdatniającej przyciąga jony wapnia i węglanowe oraz sprzyja ich wytrącaniu się tam, mniej tych jonów pozostaje do budowy solidnej osłony na ścianach rur. Badania mikroskopowe i rentgenowskie wykazały, że zamiast zwartej, bogatej w minerały bariery stal w wodzie uzdatnionej rozwijała luźną, porowatą warstwę rdzy z drobnymi, niestabilnymi kryształami. Słaba powłoka pozwalała korozyjnym gatunkom i elektronóm swobodnie się przemieszczać, więc korozja utrzymywała się szybko zamiast zwalniać z czasem.
Mocniejszy atak chemiczny w wodzie
Aby ustalić, co napędzało dodatkowy atak, zespół rozdzielił różne czynniki. Kiedy przeprowadzano elektrolizę w roztworze siarczanowym bez chlorków, produkty rozkładu wody — takie jak tlen, wodór i krótkotrwałe rodniki — praktycznie nie zmieniały zachowania korozji stali. Gdy jednak obecny był chlorek, ten sam jon spotykany w zwykłej soli i wielu wodach zasilających, obraz się zmieniał. Elektroliza przekształcała część chlorku w podchloryn, silniejszy i bardziej reaktywny środek dezynfekujący. Badania elektrochemiczne wykazały, że wraz ze wzrostem prądu stal stawała się znacznie bardziej podatna na korozję w roztworach chlorkowych. Symulacje komputerowe potwierdziły to: podchloryn obniżał barierę energetyczną dla atomów żelaza opuszczających powierzchnię metalu, co ułatwiało przebieg korozji bardziej niż sam chlorek. Równocześnie szybkie tworzenie produktów rdzy zużywało jony wodorotlenkowe, przesuwając wodę w kierunku niższego pH, czyli bardziej kwaśnych warunków, co dodatkowo sprzyjało korozji.
Co to oznacza dla systemów wodnych
Dla osób niezajmujących się tą dziedziną sedno sprawy jest takie: oczyszczanie i dezynfekcja wody prądem nie jest z automatu łagodne dla rur, którymi ta woda płynie. W systemach, gdzie woda zawiera chlorki, elektrochemiczne uzdatnianie może przekształcić część tych chlorków w silniejszy, bardziej korozyjny środek dezynfekujący, jednocześnie odsuwając minerały potrzebne do tworzenia naturalnej ochrony. Efektem jest szybsze przerzedzanie metalu i głębsze jamki, które mogą skrócić żywotność rur oraz zwiększyć ryzyko przecieków lub zanieczyszczenia. Autorzy sugerują, by projektanci i operatorzy takich systemów traktowali korozję jako kluczowy problem projektowy — poprzez ograniczanie napięcia, redukcję chlorków przed uzdatnianiem, wybór elektrod, które wytwarzają mniej agresywnych produktów ubocznych, oraz długoterminowy monitoring korozji punktowej i chemii wody — by mieć pewność, że czystsza woda nie będzie okupiona zawodzącą infrastrukturą.
Cytowanie: Zhao, S., Jing, Y., He, X. et al. Effect of electrochemical water treatment processes on carbon steel corrosion in urban water supply system. npj Mater Degrad 10, 23 (2026). https://doi.org/10.1038/s41529-026-00736-5
Słowa kluczowe: elektrochemiczne uzdatnianie wody, korozja stali węglowej, miejskie przewody wodociągowe, chlorki i podchloryn, trwałość infrastruktury wodnej