Clear Sky Science · pl
Elastyczne ferroelektryczne biomateriały do naprawy skóry, nerwów i tkanek mięśniowo-szkieletowych
Inteligentne materiały, które pomagają ciału się leczyć
Gdy złamiemy kość, naderwiemy ścięgno, uszkodzimy nerw lub pojawi się uporczywa rana skóry, lekarze często potrafią ustabilizować uraz — ale doprowadzenie do pełnej odbudowy zdrowej tkanki wciąż jest trudne. Ten artykuł opisuje nową klasę „inteligentnych” materiałów, które dopasowują się do ciała i zamieniają codzienne ruchy w mikrosygnały elektryczne. Sygnały te naśladują własny bioelektryczny język organizmu i delikatnie pobudzają komórki do wzrostu, reorganizacji i naprawy uszkodzonej skóry, nerwów, mięśni, chrząstki oraz kości.
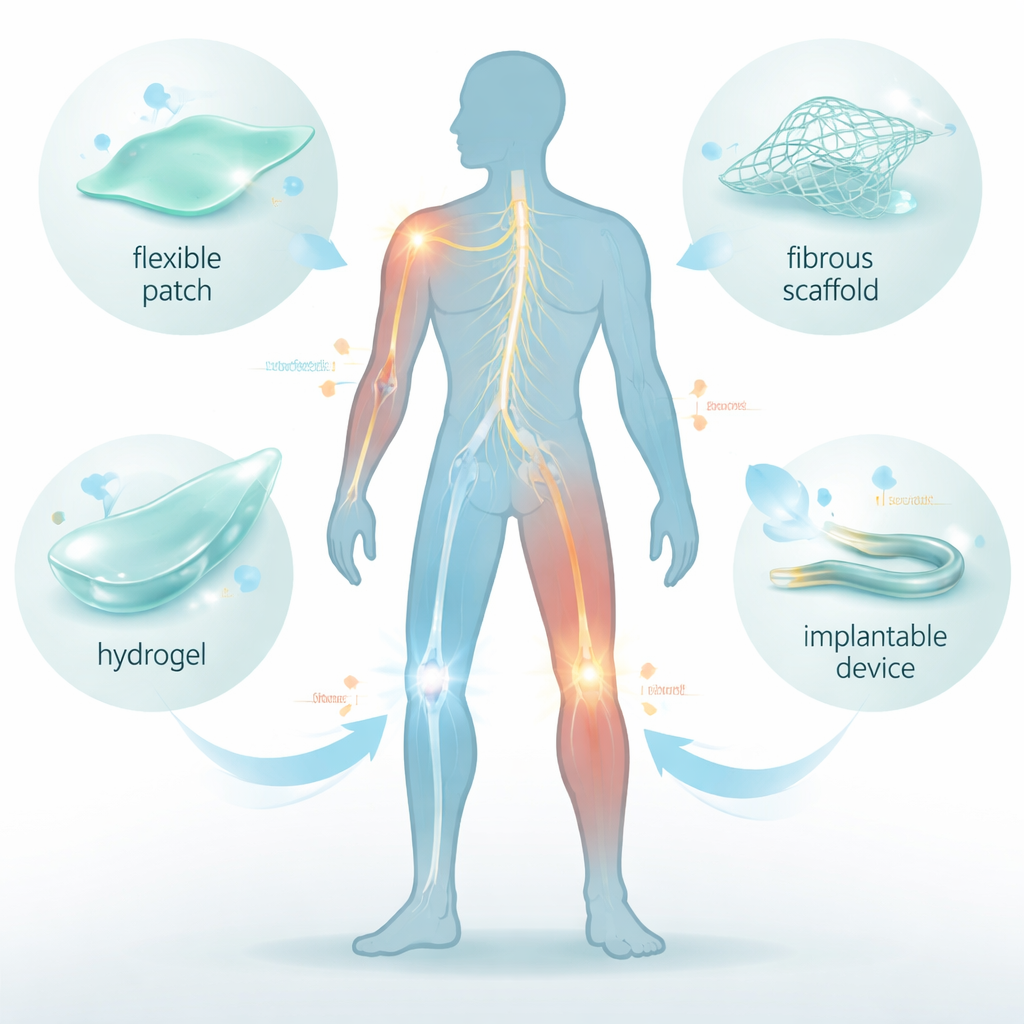
Dlaczego elektryczność ma znaczenie w gojeniu
Każda żywa tkanka niesie subtelne wzory elektryczne. Nerwy wyładowują się impulsami napięcia, kości generują niewielkie ładunki, gdy chodzimy, a skóra tworzy naturalne pola elektryczne wokół ran. Te sygnały kierują komórkami — informują je, kiedy się poruszać, dzielić i różnicować. Uraz lub przewlekłe zapalenie może zaburzyć ten elektryczny krajobraz, spowalniając lub błędnie kierując naprawę. Przegląd wyjaśnia, jak elastyczne ferroelektryczne biomateriały zostały zaprojektowane, by przywracać lub wzmacniać te sygnały. Reagują na zginanie, rozciąganie lub zmiany temperatury, wytwarzając drobne, miejscowe napięcia, zasadniczo tłumacząc ruch mechaniczny na własne elektryczne „wskazówki gojenia” organizmu.
Z czego zbudowane są te inteligentne materiały
Autorzy koncentrują się na kilku rodzinach materiałów ferroelektrycznych, które można uczynić miękkimi i przyjaznymi dla ciała. Polimery takie jak PVDF, jego kopolimer P(VDF-TrFE) oraz PLLA to tworzywa, które przy odpowiedniej obróbce zachowują się jak miniaturowe generatory: ruch powoduje powstawanie ładunku. Cząstki ceramiczne, takie jak tytanian baru (BaTiO₃), żelazotlenek bizmutu (BiFeO₃) i nioban potasowo-sodowy (KNN), oferują silną reakcję elektryczną, ale same są kruche, więc miesza się je z elastycznymi polimerami. Poprzez strojenie struktury krystalicznej, ułożenia włókien i porowatości, naukowcy mogą tworzyć cienkie folie, sieci nanowłókien, rusztowania drukowane w 3D i wstrzykiwalne hydrożele, które dopasowują się do zakrzywionych powierzchni ciała, jednocześnie generując biologicznie istotne poziomy stymulacji elektrycznej.
W jaki sposób sygnały napędzane ruchem komunikują się z komórkami
Gdy te materiały są naciskane, rozciągane lub pobudzane ultradźwiękami, dostarczają pobliskim komórkom drobne impulsy elektryczne. W błonie komórkowej znajdują się kanały jonowe, które otwierają się w odpowiedzi na bodźce elektryczne lub mechaniczne, pozwalając na napływ jonów wapnia. Krótkie spięcie wapniowe działa jak główny przełącznik, uruchamiając sieci kontrolujące przeżycie komórek, migrację, wzrost i różnicowanie w komórki kostne, chrzęstne, nerwowe lub mięśniowe. Bodźce elektryczne reorganizują też receptory powierzchniowe, wpływają na sposób, w jaki komórki przyczepiają się do otoczenia, przekształcają zużycie energii w mitochondriach, a nawet kierują komórki odpornościowe z dala od przedłużonego zapalenia w stronę zachowań sprzyjających gojeniu. Dzięki temu prosty ruch mechaniczny — na przykład chodzenie po zabiegu — może przez te materiały zostać przetworzony w znaczące biologiczne instrukcje.
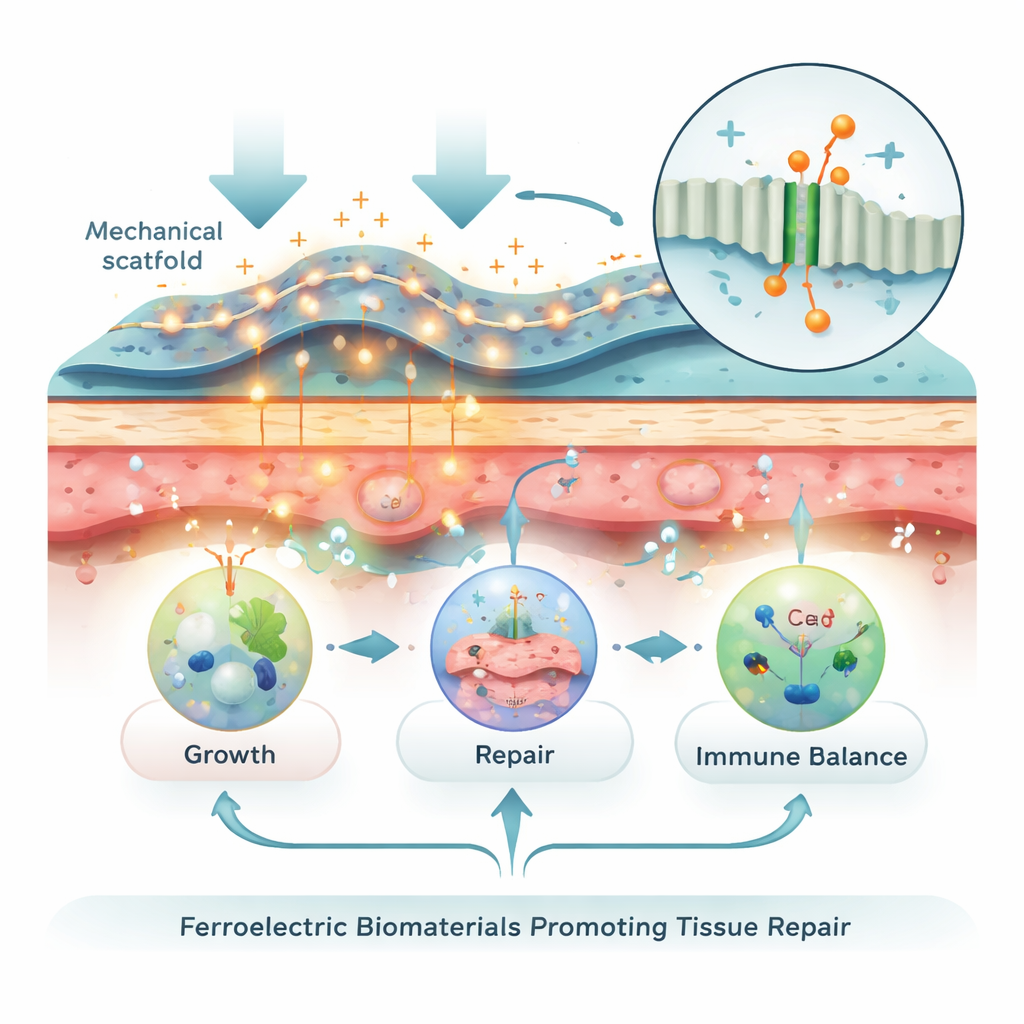
Zastosowania w praktyce: kości, nerwy, skóra i inne
Przegląd opisuje szybki postęp w wielu tkankach. W kościach i chrząstce rusztowania ferroelektryczne i hydrożele umieszczone w ubytkach generują małe napięcia podczas normalnego ruchu stawów lub przy ukierunkowanych ultradźwiękach, zwiększając aktywność genów kostotwórczych i sprzyjając odbudowie wysokiej jakości chrząstki. W obwodowych nerwach elastyczne przewody z włókien piezoelektrycznych prowadzą odrastające aksony i, gdy są aktywowane ruchem lub falami dźwiękowymi, dostarczają delikatnej, ciągłej stymulacji porównywalnej z przeszczepami nerwowymi. Dla skóry samonapędzane opatrunki i plastry drukowane w 3D wzmacniają własne prądy rany, przyspieszając zamknięcie, angiogenezę, kontrolę infekcji, a nawet redukując bliznowacenie. Podobne strategie pomagają włóknom mięśniowym w wyrównaniu i dojrzewaniu oraz wspierają silniejsze przyczepienie ścięgna do kości po urazach mankietu rotatorów czy więzadeł.
Od obietnicy w laboratorium do codziennych terapii
Mimo entuzjazmu autorzy podkreślają, że większość tych technologii znajduje się wciąż na wczesnym etapie badań na zwierzętach lub w warunkach laboratoryjnych. Wyzwania obejmują produkcję tych złożonych, warstwowych materiałów w skali przemysłowej z zachowaniem niezawodności, zapewnienie ich odporności na sterylizację i wieloletnie przebywanie w organizmie oraz dopasowanie tempa degradacji do tempa gojenia tkanek. Niektóre powszechnie stosowane polimery, jak PVDF, praktycznie się nie rozkładają w organizmie, co rodzi pytania o ich długoterminowy los. Przyszłe prace będą wymagać lepszych systemów kontroli — potencjalnie wykorzystujących sztuczną inteligencję — do regulowania stymulacji w czasie rzeczywistym, a także nowych materiałów ferroelektrycznych, które będą zarówno skuteczne, jak i naprawdę biodegradowalne. Jeśli te przeszkody zostaną pokonane, elastyczne ferroelektryczne biomateriały mogłyby umożliwić implanty, opatrunki i miękkie elektroniczne „skóry”, które cicho zbierają nasze ruchy, by zasilać precyzyjną, spersonalizowaną naprawę skóry, nerwów, mięśni i całego układu mięśniowo-szkieletowego.
Cytowanie: Sheng, N., Wang, Y., Luo, X. et al. Flexible ferroelectric biomaterials for skin, neural, and musculoskeletal tissue repair. npj Flex Electron 10, 29 (2026). https://doi.org/10.1038/s41528-026-00532-w
Słowa kluczowe: elastyczne biomateriały, stymulacja elektryczna, regeneracja tkanek, polimery piezoelektryczne, gojenie ran