Clear Sky Science · pl
Półautomatyczne przesiewowe badania genomowe noworodków uwypuklają złożoność raportowania
Dlaczego małe kropelki krwi mogą kryć wielkie odpowiedzi
W ciągu kilku dni po urodzeniu większość niemowląt przechodzi dyskretne, ratujące życie badanie: nakłucie pięty i naniesienie krwi na kartę. Badanie to analizuje, co się stanie, jeśli z tej samej próbki sięgniemy dalej i odczytamy znacznie więcej informacji z kodu genetycznego dziecka. Badacze z Południowej Australii postanowili sprawdzić, czy dodanie szeroko zakrojonej analizy DNA do rutynowych badań noworodków może bezpiecznie wykrywać więcej uleczalnych schorzeń we wczesnym stadium — bez przytłaczania rodzin i lekarzy mylącymi lub nieprzydatnymi informacjami.
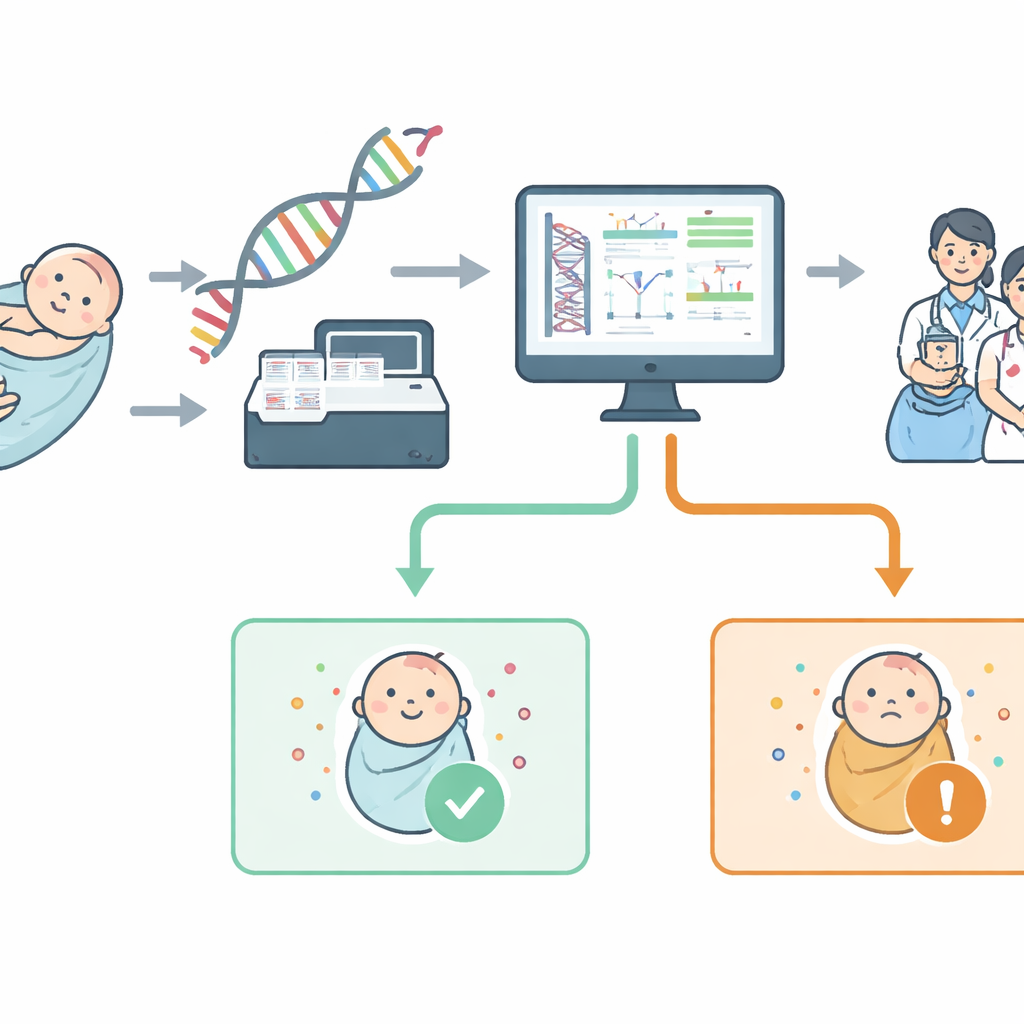
Od nakłucia pięty do skanu genomu
Tradycyjne badania przesiewowe noworodków szukają kilku/kilkudziesięciu schorzeń, mierząc związki chemiczne we krwi. Natomiast genomowe badania przesiewowe czytają fragmenty DNA, by bezpośrednio szukać zmian powodujących choroby w określonych genach. Projekt NewbornsInSA opracował test oparty na sekwencjonowaniu całego genomu, ale celowo ograniczył poszukiwania do „wirtualnego” panelu 613 genów. Geny te wybrano z udziałem lokalnych klinicystów, stosując proste kryteria: schorzenie powinno zaczynać się w dzieciństwie, powodować poważne problemy zdrowotne, mieć sensowną strategię leczenia lub zapobiegania oraz być wiarygodnie wykrywalne w laboratorium. Organizacje społeczne i grupy pacjentów pomogły następnie pogrupować te choroby według znanych kategorii układów ciała, aby rodzice lepiej rozumieli, co obejmuje test.
Test w praktyce
Zanim zaproponowano tę kontrolę opartą na DNA nowym rodzinom, zespół musiał wykazać jej skuteczność. Wyjęto 46 przechowywanych kart z krwią od dzieci, których genetyczne rozpoznania były już znane, ale ukryte przed analitykami. Wykorzystując sekwencjonowanie całego genomu i dwa oddzielne systemy oprogramowania, sprawdzono, czy ich pipeline poprawnie oznaczy dzieci, które faktycznie miały jedno z docelowych schorzeń. Wynik był zachęcający: proces wykrył 97% prawdziwych przypadków i nie wygenerował fałszywych alarmów po przeglądzie ekspertów. Jeden przypadek, który nie został wykryty, uwypuklił kluczowe ograniczenie każdego badania opartego na genach — gdy dowody naukowe dotyczące konkretnej zmiany DNA są niekompletne, komputery, a nawet eksperci, mogą być zmuszeni oznaczyć ją jako „niepewną” i potraktować jako wynik negatywny.
Pozwalając komputerom wykonać ciężką pracę
Odczytanie całego genomu generuje tysiące wariantów dla każdego dziecka, co jest zbyt wiele, by ludzie mogli je sprawdzić pojedynczo. Aby sobie z tym poradzić, badacze stworzyli półautomatyczny przebieg pracy. Autorskie skrypty, zintegrowane z komercyjną platformą analityczną, skanują opatrzoną adnotacjami listę wariantów i automatycznie wydzielają dzieci, u których wyraźnie nie stwierdzono alarmujących ustaleń, oznaczając je jako „niskie ryzyko”. Tylko przypadki ze zmianami wyglądającymi na potencjalnie szkodliwe — takimi jak znane warianty chorobotwórcze lub prawdopodobnie niszczące funkcję genu — są przekazywane do ekspertów do szczegółowej oceny. W pierwszych 100 badanych noworodków ta automatyzacja natychmiast zmniejszyła liczbę dzieci wymagających ręcznego przeglądu o ponad połowę, co jest kluczowym krokiem, jeśli taki przesiew ma być skalowany na całe populacje.
Prawdziwe dzieci, prawdziwe decyzje
Gdy zespół zastosował przebieg pracy do pierwszych 100 zarejestrowanych noworodków, u pięciorga dzieci uzyskano wyniki sugerujące wysokie prawdopodobieństwo konkretnego schorzenia. Były to m.in. zaburzenia rytmu serca mogące powodować niebezpieczne arytmie, problem metaboliczny już podejrzany w standardowym przesiewie, zmiana genetyczna zwiększająca ryzyko uszkodzenia słuchu po niektórych antybiotykach oraz łagodna postać dziedzicznej hiperglikemii. W każdym przypadku wynik uruchomił dostosowane dalsze działania: badania serca i monitorowanie, elektroniczne ostrzeżenia dotyczące unikania konkretnych leków lub planowanie opieki przy przyszłych ciążach. Jednocześnie wiele innych ustaleń celowo nie zostało zgłoszonych, ponieważ wiązały się z łagodnymi objawami, nowotworami pojawiającymi się w wieku dorosłym, niepewnym ryzykiem lub złożonymi wzorcami, których obecna wiedza nie pozwala z pewnością zinterpretować u zdrowego noworodka. Te trudne decyzje wymagały godzin lektury literatury i dyskusji między genetykami a specjalistami, co podkreśla, że sąd ekspercki wciąż ma znaczenie.
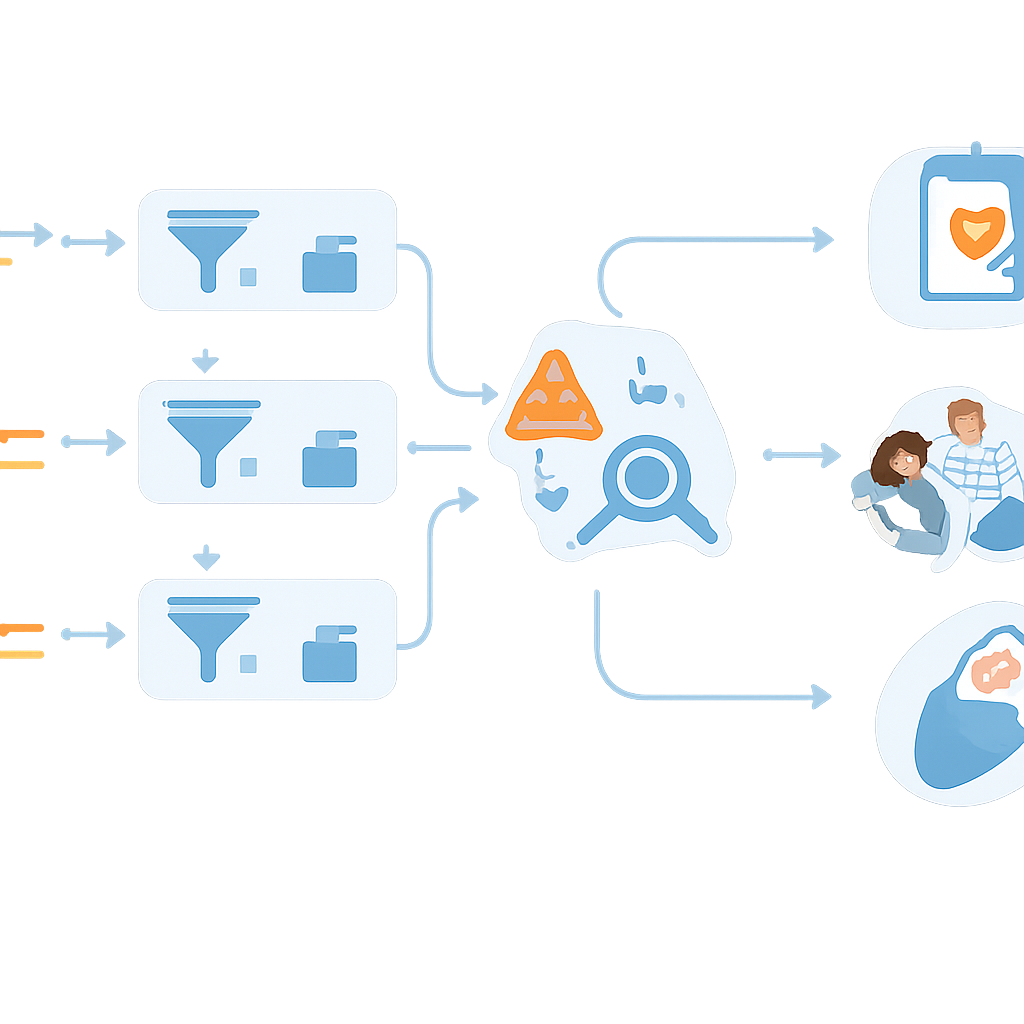
Równoważenie wczesnej pomocy i przyszłego obciążenia
Praca ta pokazuje, że technicznie możliwe jest wykorzystanie danych z całego genomu pozyskanych z maleńkiej kropelki krwi do wykrywania większej liczby uleczalnych chorób dziecięcych niż testy standardowe, z wysoką dokładnością i wsparciem sprytnego oprogramowania. Jednocześnie obnaża też etyczny i praktyczny spacer po linie: każdy dodatkowy gen podnosi prawdopodobieństwo ujawnienia informacji, która teraz może nie pomóc dziecku, może niepotrzebnie niepokoić rodziców albo stać się istotna dopiero za dekady. Półautomatyczne, starannie kuratorowane podejście zespołu NewbornsInSA — gdzie komputery wykluczają wyraźne negatywy, a ludzie skupiają się na niuansowanych przypadkach — oferuje model wdrożenia odpowiedzialnego przesiewu genomowego noworodków, podczas gdy trwające badania uzupełniające śledzą jego rzeczywiste korzyści i ryzyka dla rodzin.
Cytowanie: Chowdhury, A., Marri, S., Anastasi, L. et al. Semi-automated genomic newborn screening highlights complexities in reporting. npj Genom. Med. 11, 13 (2026). https://doi.org/10.1038/s41525-026-00553-4
Słowa kluczowe: genomowe badania przesiewowe noworodków, sekwencjonowanie całego genomu, suche kropelki krwi, interpretacja wariantów genetycznych, wczesne wykrywanie rzadkich chorób