Clear Sky Science · pl
Analiza transkryptomiczna w celu odkrycia mechanizmu radiosentyzacji AR-dodatnich potrójnie ujemnych raków piersi przy hamowaniu receptora androgenowego
Dlaczego to badanie ma znaczenie dla osób z rakiem piersi
Radioterapia jest głównym elementem leczenia wielu osób z agresywnymi rakami piersi, ale niektóre guzy są z natury trudniejsze do zniszczenia promieniowaniem niż inne. To badanie stawia praktyczne pytanie o rzeczywiste implikacje kliniczne: czy klasa leków blokujących sygnały androgenowe, już stosowana w raku prostaty, może uczynić pewną podgrupę potrójnie ujemnych raków piersi bardziej wrażliwą na promieniowanie — i dlaczego działa to w niektórych przypadkach, a w innych nie?
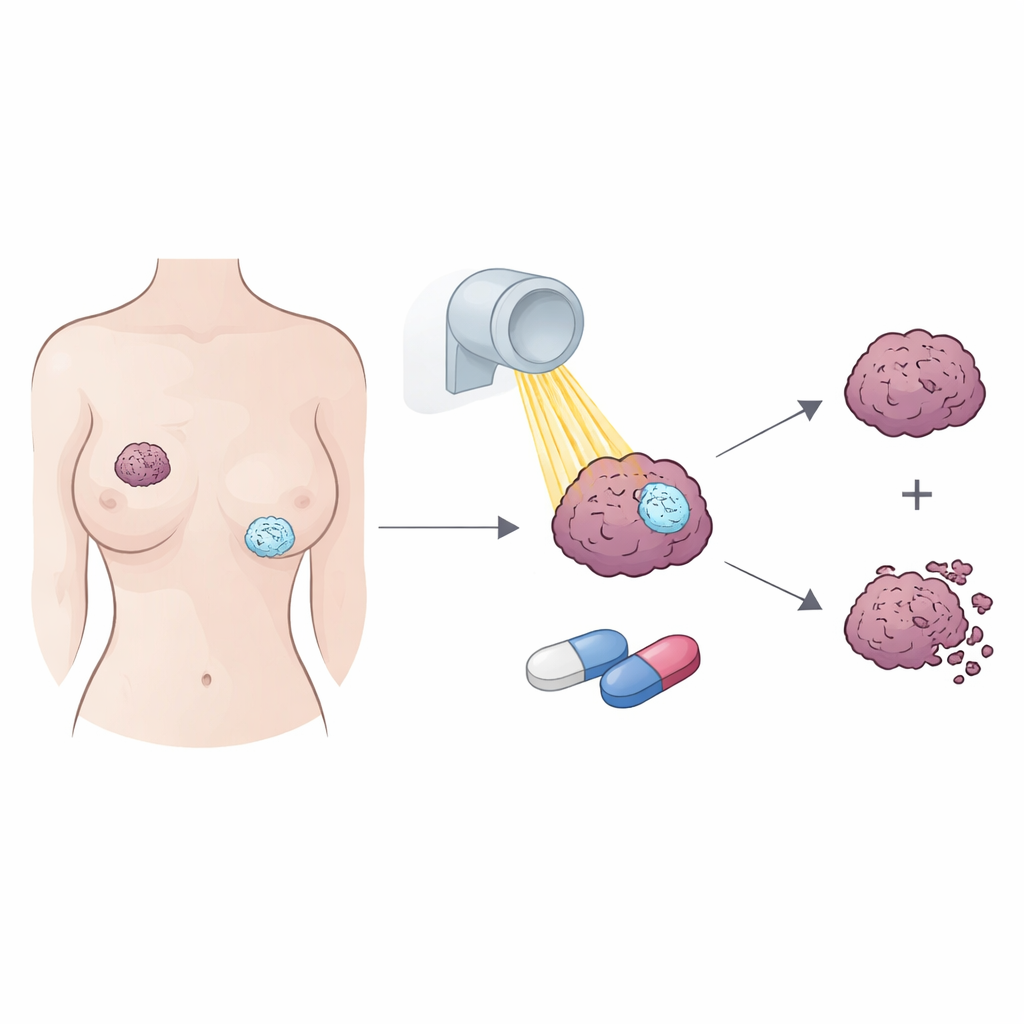
Trudna do leczenia postać raka piersi
Potrójnie ujemne raki piersi nie posiadają trzech powszechnych molekularnych celów — receptorów estrogenowych, receptorów progesteronowych i HER2 — więc pacjenci często muszą polegać wyłącznie na chirurgii, chemioterapii i radioterapii. Jednak część tych guzów wyraża receptor androgenowy, białko reagujące na hormony podobne do testosteronu i mogące napędzać wzrost guza. Wcześniejsze badania wykazały, że blokowanie tego receptora może spowalniać te nowotwory i potencjalnie wzmacniać działanie promieniowania, ale nie było jasne, jak dokładnie to działa i które leki oraz które guzy odnoszą największą korzyść.
Testowanie nowoczesnych blokerów hormonów z radioterapią
Naukowcy badali kilka modeli laboratoryjnych komórek potrójnie ujemnego raka piersi, które różniły się przede wszystkim ilością receptoru androgenowego. Skoncentrowali się na dwóch nowszych lekach antyandrogenowych, apalutamidzie i darolutamidzie, łącząc krótkie ekspozycje na te leki ze standardowymi dawkami promieniowania rentgenowskiego. W komórkach o wysokim poziomie receptora androgenowego apalutamid wyraźnie zwiększał uszkodzenia wywołane promieniowaniem, pozostawiając mniej komórek zdolnych do tworzenia nowych kolonii. Darolutamid natomiast wykazywał niewielki lub żaden wpływ na wrażliwość na promieniowanie w tych samych komórkach, a żaden z leków nie pomagał w komórkach o bardzo niskim poziomie receptora androgenowego. Wyniki te sugerują, że nie wszystkie leki blokujące androgeny działają tak samo w raku piersi i że guzy muszą silnie polegać na tym receptorze, by kombinacja była skuteczna.
Obserwacja przemieszczania się kluczowego białka wewnątrz komórki
Aby zrozumieć, co dzieje się wewnątrz komórek nowotworowych po sygnałach hormonalnych lub promieniowaniu, zespół śledził lokalizację samego receptora androgenowego. Gdy komórki wystawiono na syntetyczny androgen, receptor przemieścił się do jądra komórkowego, centrum kontroli, gdzie geny są włączane i wyłączane. Sama radioterapia nie wypchnęła receptora z jądra; wręcz przeciwnie, pozostawał tam po leczeniu, gotów wpływać na aktywność genów. Jednak gdy komórki otrzymały przed radioterapią lek antyandrogenowy enzalutamid, poziom receptora w jądrze spadł, a więcej egzemplarzy pozostało w cytoplazmie. Wspiera to tezę, że blokowanie wejścia receptora do jądra zaburza jego zdolność do uruchamiania ochronnego programu genowego po napromienieniu.
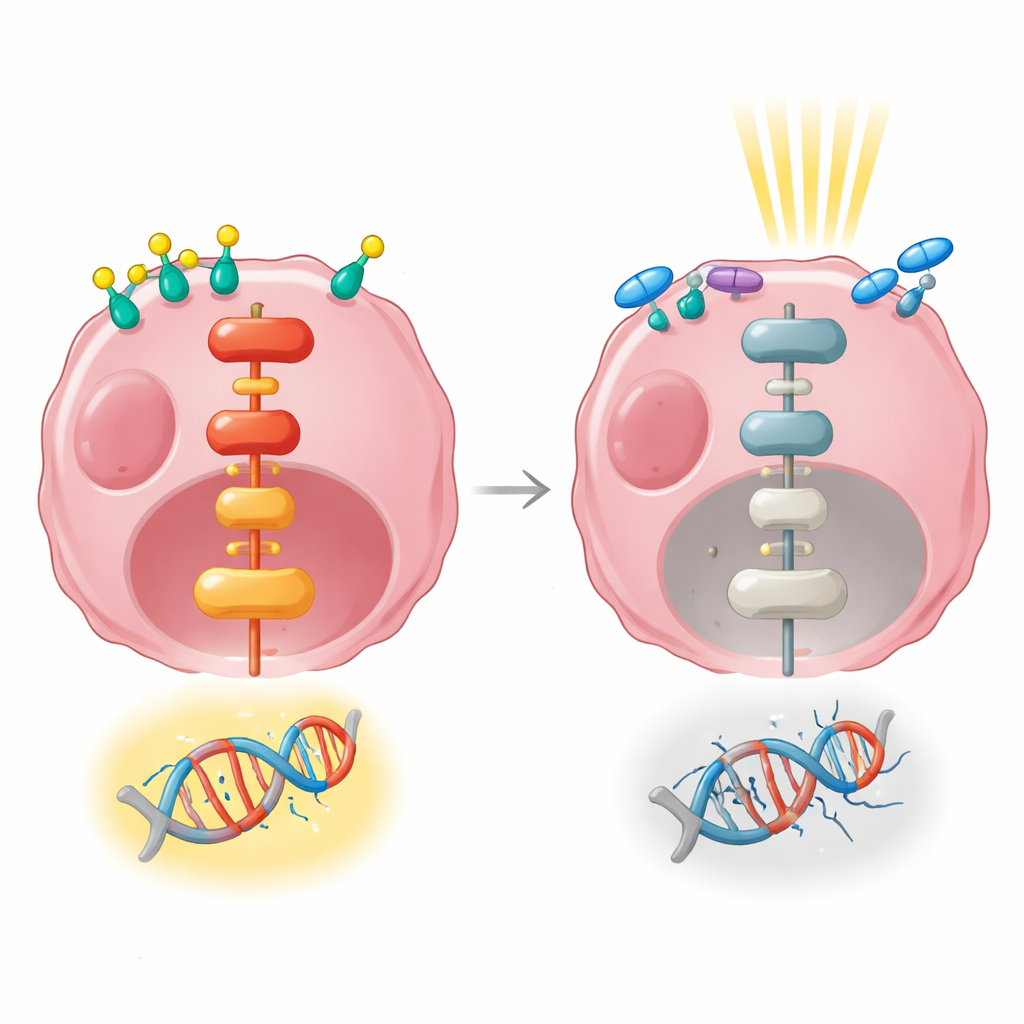
Sygnały genowe łączące hormony z opornością
Następnie badacze użyli sekwencjonowania RNA, by uzyskać szerokie spojrzenie na to, które geny były włączane lub wyłączane po stymulacji hormonalnej, promieniowaniu lub obu tych czynnikach. Leczenie hormonem samo w sobie zmieniało aktywność setek genów i silnie wpływało na szlaki kontrolujące wzrost komórek, przyleganie i komunikację ze środowiskiem. Promieniowanie podane samotnie, w wczesnym punkcie czasowym, zmieniało znacznie mniej genów. Gdy stymulacja hormonalna i promieniowanie były połączone, aktywowane były wiele tych samych szlaków związanych ze wzrostem, w tym ważna droga sygnałowa znana jako MAPK/ERK, która przekazuje sygnały z powierzchni komórki do jądra. Ten szlak jest znany z tego, że pomaga komórkom przetrwać i naprawiać uszkodzenia DNA.
Badanie szlaku przetrwania chroniącego DNA
Ponieważ sygnalizacja MAPK/ERK pojawiała się wielokrotnie w ich analizach, badacze sprawdzili, czy wzmocnienie tego szlaku mogłoby cofnąć korzyść z blokady androgenowej podczas radioterapii. Zmodyfikowali komórki nowotworowe tak, by nadprodukowały stale aktywną formę ERK, kluczowego składnika szlaku, a następnie powtórzyli leczenie promieniowaniem z apalutamidem. W tym ustawieniu apalutamid przestał zwiększać wrażliwość komórek na promieniowanie: wzmocniony sygnał ERK wydawał się je chronić. Wraz z pomiarami białek wyniki te wskazują na sygnalizację MAPK/ERK jako istotne ogniwo łączące aktywność receptora androgenowego z zdolnością komórki do naprawy pęknięć DNA wywołanych promieniowaniem.
Co to oznacza dla przyszłej opieki nad rakiem piersi
Mówiąc prościej, praca ta sugeruje, że niektóre potrójnie ujemne raki piersi przetrwają promieniowanie, używając sygnałów związanych z androgenami do uruchomienia wewnętrznego obwodu przetrwania, który pomaga im naprawiać uszkodzone DNA. Leki takie jak apalutamid i enzalutamid mogą przerwać ten obwód w guzach, które silnie zależą od receptora androgenowego, zwiększając skuteczność radioterapii, podczas gdy guzy z niskim poziomem receptora lub z alternatywnymi drogami przetrwania mogą nie odnieść korzyści. Mapując zaangażowane szlaki genowe — zwłaszcza drogę MAPK/ERK — to badanie toruje drogę do bardziej precyzyjnych kombinacji blokerów hormonów, inhibitorów szlaków i radioterapii, które mogą poprawić wyniki u pacjentów z tą trudną do leczenia postacią raka piersi.
Cytowanie: McBean, B., Hauk, B., Michmerhuizen, A.R. et al. Transcriptomic analysis to uncover the mechanism of radiosensitization of AR-positive triple-negative breast cancers with AR inhibition. npj Breast Cancer 12, 50 (2026). https://doi.org/10.1038/s41523-026-00916-1
Słowa kluczowe: potrójnie ujemny rak piersi, receptor androgenowy, radioterapia, radiosentyzacja, szlak sygnałowy MAPK ERK