Clear Sky Science · pl
Programowalna miejscowa immunochemioterapia dla raka piersi potrójnie ujemnego poprzez przestrzenno‑czasowo kontrolowane uwalnianie oligodeoksynukleotydów CpG, gemcytabiny i paklitakselu
Przekształcanie trudnego raka piersi w cel lokalny
Rak piersi potrójnie ujemny jest jedną z najtrudniejszych postaci raka piersi do leczenia, ponieważ brakuje w nim zwykłych molekularnych przełączników, do których przyczepia się wiele współczesnych leków. Pacjenci często muszą polegać na silnej chemioterapii, która rozchodzi się po całym organizmie, powodując poważne skutki uboczne i zbyt często rozczarowujące długoterminowe wyniki. W tym badaniu autorzy badają zupełnie inną koncepcję: zamiast zalewać organizm lekami, czy można umieścić przy guzie niewielkie, programowalne źródło leku, które uwalnia chemioterapeutyki i środki pobudzające układ odpornościowy w starannie zaplanowanej sekwencji, dokładnie tam, gdzie są najbardziej potrzebne?
Maleńkie źródło o dużych ambicjach
Naukowcy stworzyli to, co nazywają platformą Programowalnej Lokalnej Immunochemioterapii, w skrócie PLICT. Wyobraźcie to sobie jako miękką, wstrzykiwalną kulkę, która siedzi obok guza piersi i powoli uwalnia leczenie przez tygodnie. Kulka łączy hydrofilowy żel, który szybko uwalnia stymulator odporności oraz jeden lek chemioterapeutyczny — gemcytabinę, z mikroskopijnymi plastikowymi sferami, które powoli wydzielają drugi lek, paklitaksel. Stymulator odporności, krótki odcinek DNA zwany CpG, ma obudzić lokalne komórki odpornościowe, podczas gdy połączone chemioterapeutyki bezpośrednio atakują komórki nowotworowe i przekształcają mikrośrodowisko guza, aby komórki odpornościowe mogły wnikać i wykonywać swoją pracę.
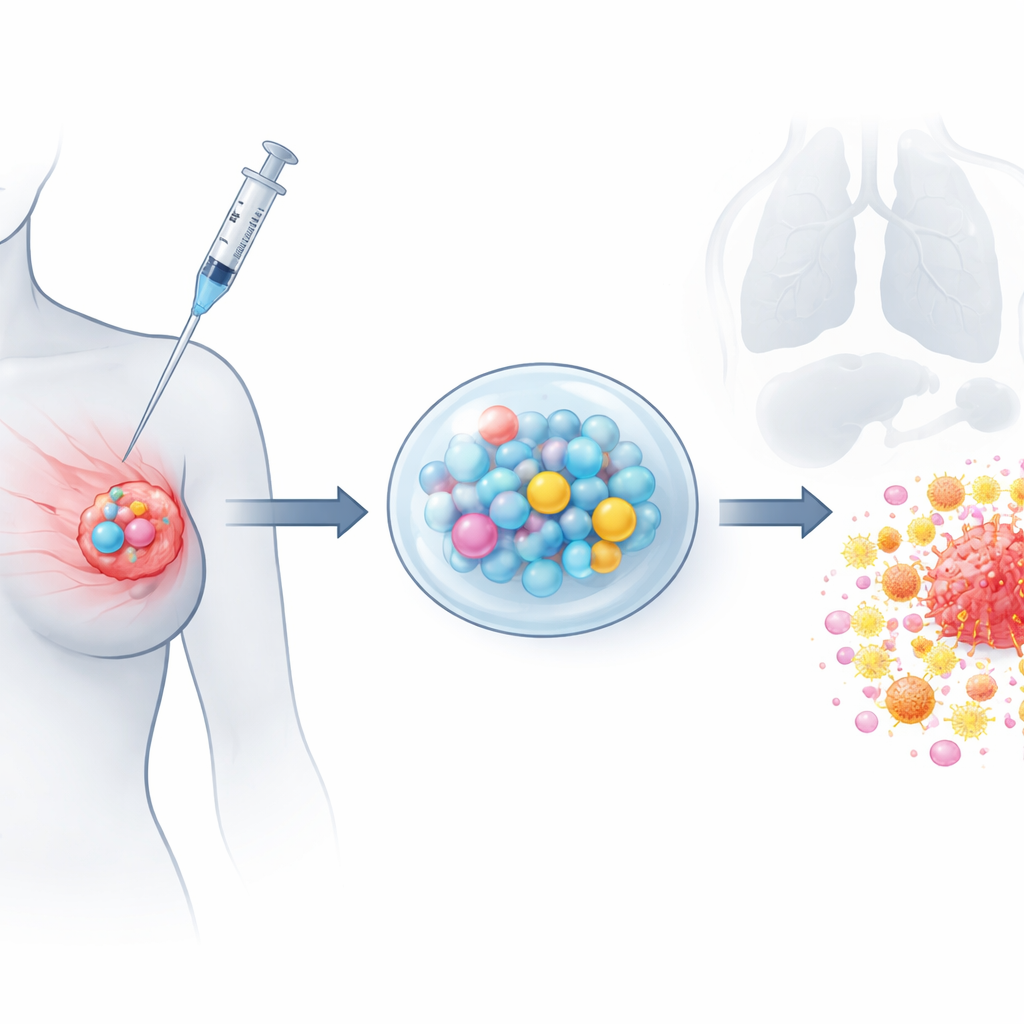
Opracowanie zaplanowanego uwalniania ataku na raka
Aby zbudować ten system, zespół użył wysokonapięciowej metody „elektrospray” do formowania jednorodnych mikrosfer załadowanych paklitakselem z biodegradowalnego polimeru. Obrazowanie pokazało gładkie, kuliste cząstki o wielkości około jednej dziesiątej szerokości ludzkiego włosa, a testy laboratoryjne potwierdziły, że paklitaksel uwalniał się równomiernie przez co najmniej miesiąc bez wczesnego wyrzutu. Oddzielnie osadzili gemcytabinę i CpG w żelu wrażliwym na temperaturę, który jest płynny po schłodzeniu i staje się półstały w temperaturze ciała. Charakterystyka chemiczna potwierdziła, że oba leki pozostały nienaruszone wewnątrz nośników. W połączeniu żel zapewnia szybkie, wczesne dawkowanie gemcytabiny i CpG, natomiast mikrosfery oferują przedłużone, powolne uwalnianie paklitakselu, naśladując korzyści długotrwałej, niskodawkowej chemioterapii z jednorazowej, lokalnej aplikacji.
Próba strategii lokalnej u myszy
Zespół następnie przetestował PLICT w modelu myszy z rakiem piersi potrójnie ujemnym. Myszy najpierw rozwinęły małe guzy piersi, a następnie otrzymały albo standardowe zastrzyki paklitakselu samego, paklitakselu z gemcytabiną, albo jednorazowy lokalny implant PLICT obok guza. W ciągu czterech tygodni guzy w grupie kontrolnej szybko rosły, te poddane standardowej chemioterapii rosły wolniej, ale guzy traktowane PLICT były dramatycznie mniejsze zarówno pod względem rozmiaru, jak i masy. Obrazowanie całego zwierzęcia i usuniętych narządów wykazało, że PLICT także skuteczniej niż konwencjonalne zastrzyki ograniczał przerzuty do odległych miejsc, zwłaszcza do płuc. Pomiar poziomów leków wyjaśnił dlaczego: paklitaksel był silnie skoncentrowany w guzach leczonych PLICT, lecz niski w odległej tkance tłuszczowej i porównywalny we krwi, co sugeruje silne lokalne zatrzymywanie przy mniejszej ekspozycji poza celem.
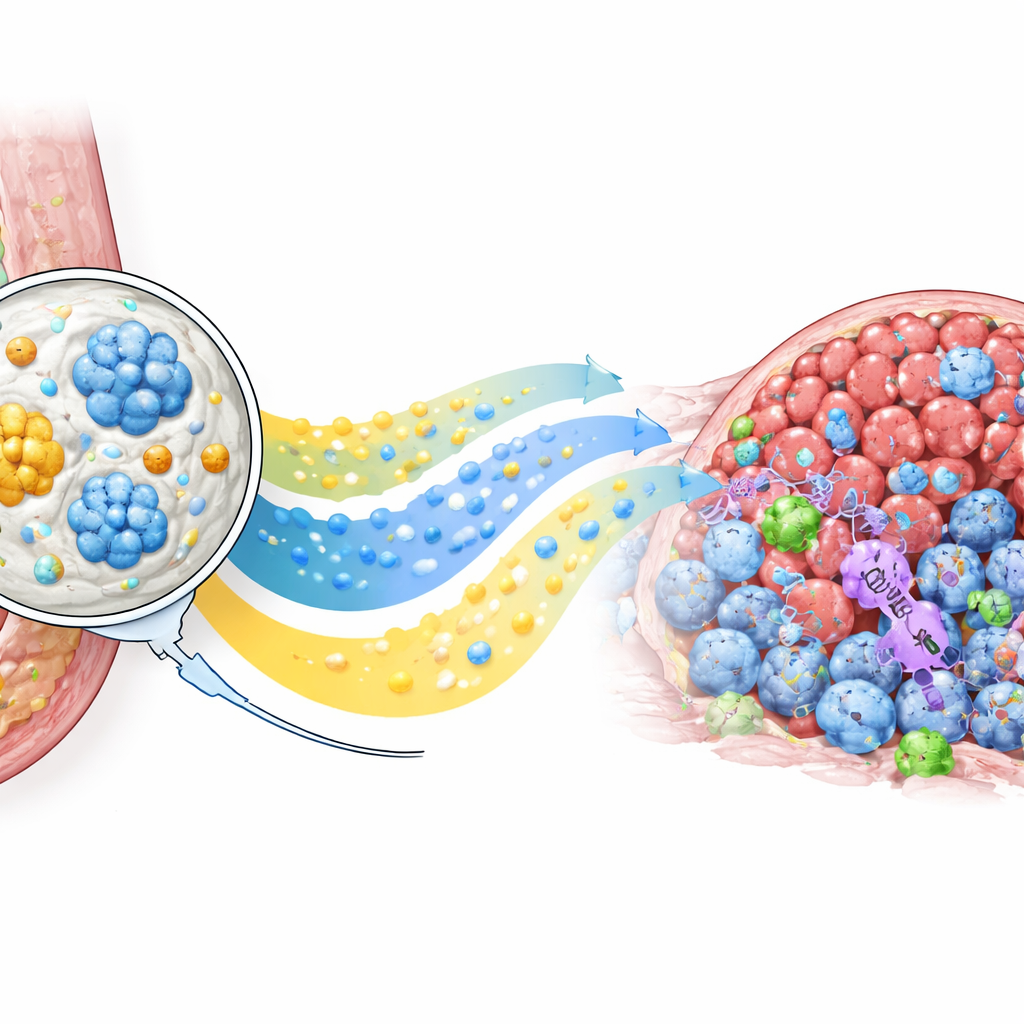
Rekrutowanie własnych obrońców organizmu
Ponad samo zmniejszenie guzów, PLICT zmienił krajobraz immunologiczny wewnątrz nich. Szczegółowe analizy komórkowe wykazały wyraźny wzrost komórek CD8 zabijających nowotwór w guzach leczonych PLICT w porównaniu ze wszystkimi innymi grupami, wraz ze spadkiem niektórych komórek regulatorowych T, które zwykle tłumią ataki immunologiczne. Barwienie tkanek dla CD69, markera niedawno aktywowanych limfocytów T, potwierdziło, że wiele z tych infiltrujących komórek było aktywowanych i gotowych do działania. Jednocześnie standardowa chemioterapia powodowała widoczne uszkodzenia tkanki wątroby, podczas gdy narządy myszy leczonych PLICT wyglądały pod mikroskopem niemal normalnie. Razem te ustalenia wskazują, że lokalne źródło nie tylko zwiększa bezpośrednią ekspozycję leku w guzie, lecz także zapala korzystniejszą, mniej stłumioną odpowiedź immunologiczną bez dodatkowego obciążenia dla ważnych narządów.
Co to może znaczyć dla przyszłej opieki onkologicznej
Dla osób nietechnicznych przesłanie jest jasne: przekształcając chemioterapię i stymulację odporności w powolny, precyzyjnie etapowany dopływ dostarczany tuż obok guza, podejście to uzyskało silniejszą kontrolę guza i mniej ogólnoustrojowych efektów ubocznych u zwierząt niż standardowe zastrzyki leków. Prace są nadal na etapie przedklinicznym i pozostają pytania, jak taki system sprawdziłby się u ludzi lub w różnych warunkach leczenia. Jednak koncepcja wstrzykiwalnego, programowalnego „magazynu leku”, który dyskretnie uwalnia wiele czynników w sekwencji, może otworzyć nowe sposoby leczenia agresywnych nowotworów, takich jak rak piersi potrójnie ujemny — skupiając walkę tam, gdzie ma największe znaczenie, przy jednoczesnym oszczędzaniu reszty organizmu.
Cytowanie: Hsieh, CH., Hsu, MY., Lin, CF. et al. Programmable local immunochemotherapy for triple-negative breast cancer via spatiotemporally controlled release of CpG oligodeoxynucleotides, gemcitabine, and paclitaxel. npj Breast Cancer 12, 45 (2026). https://doi.org/10.1038/s41523-026-00910-7
Słowa kluczowe: rak piersi potrójnie ujemny, miejscowe dostarczanie leków, immunoterapia, kontrolowane uwalnianie, mikrosfery hydrożelowe