Clear Sky Science · pl
Ekspresja genów docelowych receptora estrogenowego β ujawnia nowe funkcje represyjne w agresywnym raku piersi
Dlaczego to badanie ma znaczenie
Zapalny rak piersi jest jedną z najbardziej agresywnych i śmiertelnych postaci raka piersi, często szybko się rozprzestrzeniając i pozostawiając pacjentki z niewieloma opcjami terapii ukierunkowanej. Badanie to analizuje mniej znany sensor hormonalny w komórkach piersi — receptor estrogenowy beta — i pokazuje, jak może on działać jako naturalny hamulec rozprzestrzeniania się guza. Zrozumienie mechanizmu działania tego wbudowanego hamulca może otworzyć drogę do nowych leków, które spowolnią lub zapobiegną tworzeniu przerzutów u pacjentek, które obecnie mają bardzo ograniczone możliwości leczenia.
Inna twarz zapalnego raka piersi
W przeciwieństwie do wielu raków piersi zależnych od klasycznego receptora estrogenowego alfa, zapalny rak piersi zwykle pozbawiony jest tego białka i w związku z tym słabo reaguje na standardowe terapie hormonalne. Autorzy skupiają się zamiast tego na drugim receptorze estrogenowym, receptorze estrogenowym beta (ERβ), który wcześniej powiązali z mniejszą liczbą przerzutów zarówno u pacjentek, jak i w modelach myszowych. Wcześniejsze prace sugerowały, że ERβ spowalnia wewnętrzne rusztowanie komórkowe i mechanizmy ruchu. W tym badaniu zespół postanowił mapować w całym genomie, jak ERβ zmienia aktywność genów i które molekuły downstream mogą wyjaśniać jego ochronną, anty‑metastatyczną rolę.
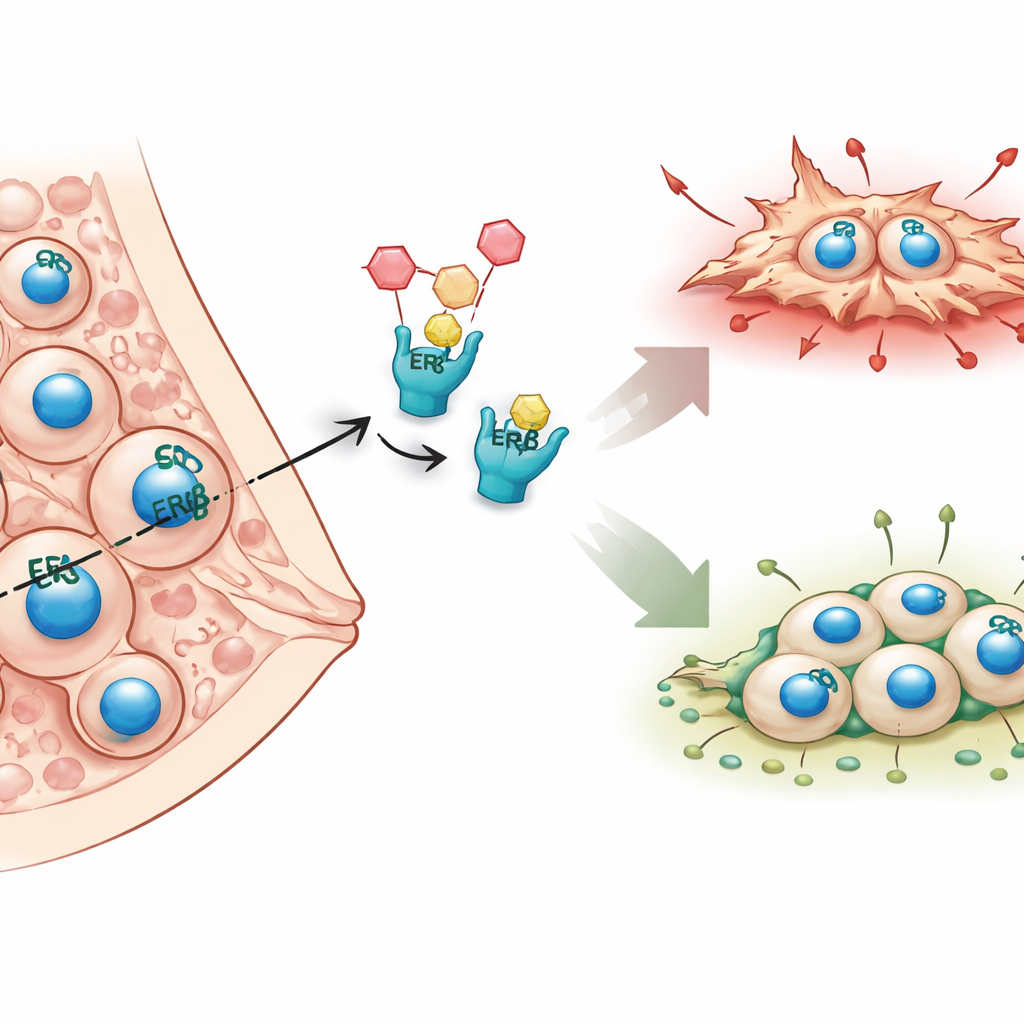
Odczytywanie instrukcji komórki nowotworowej
Aby odsłonić wpływ ERβ, badacze zastosowali dwie potężne metody sekwencjonowania na liniach komórkowych zapalnego raka piersi. Jedna metoda, ChIP‑seq, precyzyjnie wskazuje miejsca, gdzie ERβ przyłącza się do DNA, niczym zaznaczanie konkretnych stron i wersów w podręczniku instrukcji komórkowej. Druga metoda, RNA‑seq, mierzy, które geny są włączane lub wyłączane, gdy ERβ jest obecny, nieobecny lub aktywowany przez selektywny lek. Porównanie tych zestawów danych wykazało tysiące miejsc DNA wiązanych przez ERβ, z których większość znajduje się nie tylko przy klasycznych włącznikach genów, lecz także głęboko wewnątrz lub pomiędzy genami, co sugeruje szerokie spektrum kontroli. Odkryto również, że ERβ często współpracuje z rodzinami innych czynników transkrypcyjnych, tworząc kompleksy, które wspólnie decydują o uciszaniu lub aktywacji konkretnych genów.
Przeprogramowanie wzrostu, ruchu i metabolizmu
Zintegrowana analiza wykazała, że ERβ ma tendencję do tłumienia genów sprzyjających ruchowi komórek, zmienności kształtu i inwazji, szczególnie tych związanych z cytoszkieletem aktynowym i sygnalizacją Rho GTPaz — szlakami znanymi z napędzania przerzutów. Jednocześnie ERβ wspiera programy genowe związane z rozwojem tkanek i różnicowaniem komórek, skłaniając komórki nowotworowe ku bardziej osiadłemu, mniej agresywnemu fenotypowi. Badanie ujawniło także zaskakującą rolę ERβ w regulacji szlaków metabolicznych, zwłaszcza tych obejmujących kwasy tłuszczowe i fosfolipidy, które są kluczowym paliwem i materiałami budulcowymi dla szybko rosnących guzów. Co ważne, efekty te obserwowano nie tylko w komórkach zaprojektowanych do nadprodukcji ERβ, lecz także w komórkach z naturalnym poziomem receptora, co podkreśla ich znaczenie w realnych warunkach.
Małe cząsteczki RNA i wpływ kliniczny
Poza genami kodującymi białka, zespół przeanalizował mikroRNA — drobne cząsteczki RNA, które precyzyjnie modulują ekspresję genów. Znaleziono dziesiątki mikroRNA, których poziomy zmieniały się po usunięciu lub przywróceniu ERβ, z których wiele powiązano wcześniej z supresją guza w raku piersi. Łącząc te mikroRNA z ich genami docelowymi, autorzy pokazali, że ERβ kontroluje niektórych czynników napędzających nowotwór pośrednio, poprzez wielowarstwową sieć regulacyjną. Następnie zwrócono się do danych klinicznych, badając guzy od osób z zapalnym i niezapalnym rakiem piersi. Kilka genów kontrolowanych przez ERβ silnie korelowało z przeżywalnością pacjentek: wysokie poziomy niektórych (takich jak SERPINA1 i HSPB8) prognozowały lepsze wyniki, podczas gdy wysokie poziomy innych (takich jak PITX1 i HOMER3) wiązały się z gorszym przeżyciem. Stawia to te molekuły downstream jako potencjalne markery prognostyczne i przyszłe cele terapeutyczne.
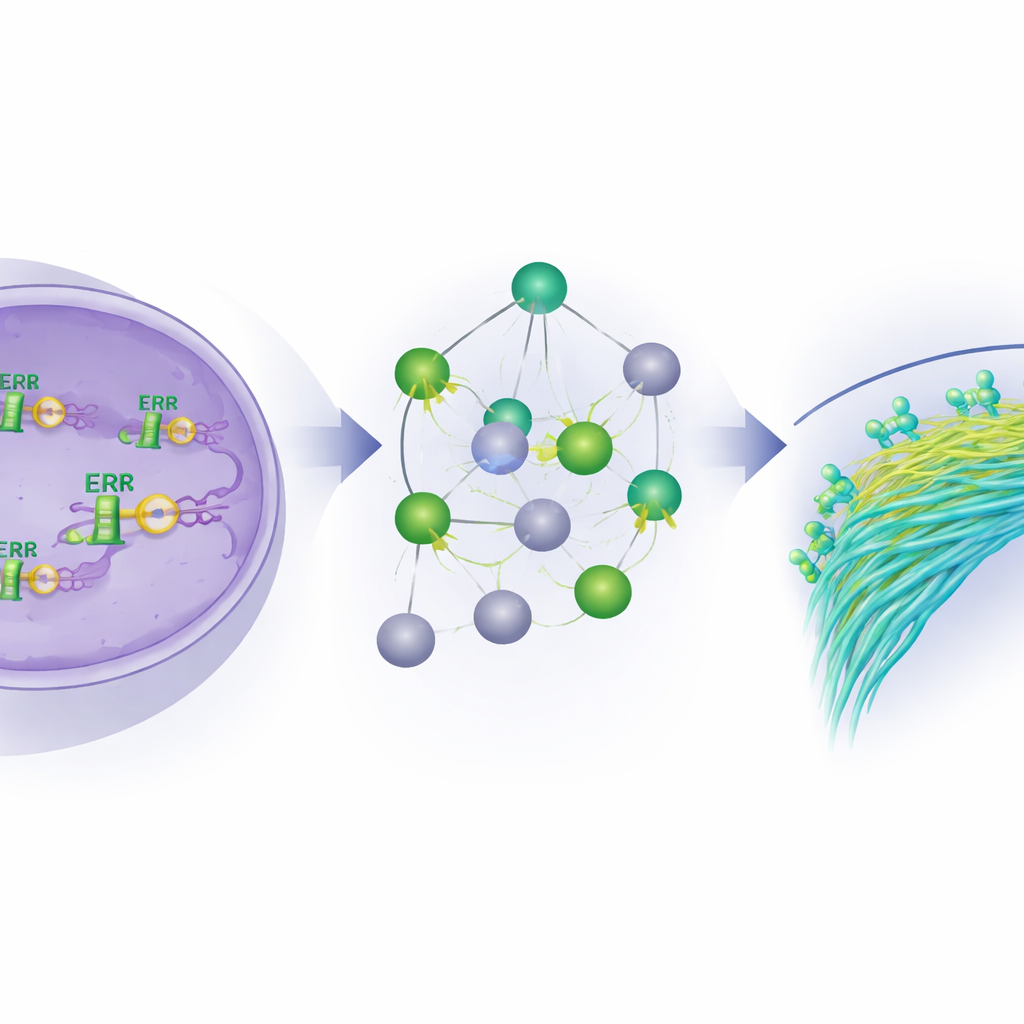
Od molekularnego hamulca do przyszłych terapii
Podsumowując, badanie przedstawia ERβ jako centralny hamulec zachowań inwazyjnych komórek zapalnego raka piersi. Poprzez wiązanie DNA, współpracę z innymi regulatorami oraz kształtowanie sieci genów i mikroRNA, ERβ tłumi programy napędzające migrację komórek i przerzuty, a jednocześnie promuje bardziej stabilne, zróżnicowane stany i przestrojenie metabolizmu nowotworowego. Dla pacjentek sugeruje to, że leki aktywujące ERβ lub hamujące jego kluczowe cele downstream — zwłaszcza te zaangażowane w ruch komórek i wykorzystanie kwasów tłuszczowych — mogą stać się podstawą nowych, bardziej precyzyjnych terapii dla tej trudnej do leczenia choroby.
Cytowanie: Tastsoglou, S., Karagounis, I.V., Miliotis, M. et al. Estrogen receptor β target gene expression reveals novel repressive functions in aggressive breast cancer. npj Breast Cancer 12, 38 (2026). https://doi.org/10.1038/s41523-026-00905-4
Słowa kluczowe: zapalny rak piersi, receptor estrogenowy beta, przerzuty, regulacja genów, metabolizm nowotworowy