Clear Sky Science · pl
Oś CXCL10/CXCR3 jest niezbędna do utrzymania immunologicznej dormancji w raku piersi potrójnie ujemnym
Dlaczego niektóre nowotwory „śpią” zamiast się rozprzestrzeniać
Rak piersi bywa czasem jak agent przebywający w ukryciu. Po początkowym leczeniu kilka komórek nowotworowych może ukrywać się w organizmie przez lata, nie rosnąc na tyle, by było je widać w badaniach obrazowych — ale cały czas zdolne do „obudzenia się” i wywołania zagrażających życiu przerzutów. Artykuł bada, dlaczego taki stan „snu”, zwany dormancją, występuje w szczególnie agresywnej postaci choroby, raku piersi potrójnie ujemnym, i ujawnia sygnał chemiczny, który pomaga układowi odpornościowemu utrzymać te komórki pod kontrolą.
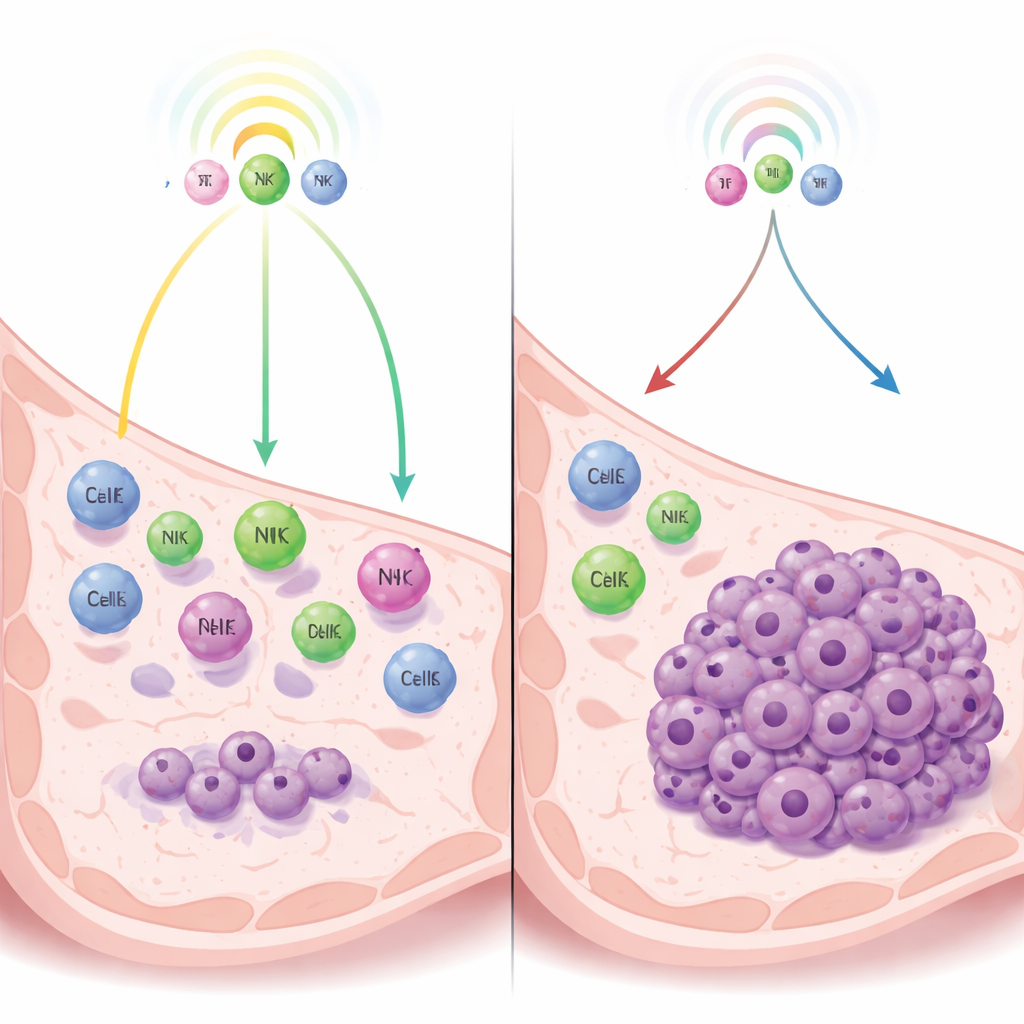
Siłowanie się między rakiem a układem odpornościowym
Autorzy koncentrują się na rodzaju dormancji kontrolowanej nie przez brak unaczynienia ani wewnętrzne hamulce komórkowe, lecz przez nadzór immunologiczny — stałe czuwanie komórek odpornościowych, które potrafią powstrzymywać guzy bez ich całkowitego wyeliminowania. Wykorzystując modele mysie raka piersi potrójnie ujemnego, porównują komórki guza, które naturalnie pozostają w stanie dormancji, z blisko spokrewnionymi komórkami tworzącymi szybko rosnące guzy. Analizując, które geny są włączone, odkrywają, że komórki w dormancji silnie aktywują szlaki interferonowe — systemy alarmowe układu odpornościowego, które stymulują uwalnianie przekaźników chemicznych przyciągających komórki odpornościowe do obszaru guza.
Kluczowy przekaźnik chemiczny, który utrzymuje guzy w spokoju
Wśród wielu cząsteczek włączonych w komórkach uśpionych wyróżnia się jedna: CXCL10, małe białko działające jak znak przyciągający komórki odpornościowe posiadające jego partnera, receptor CXCR3. Komórki nowotworowe w dormancji produkują znacznie więcej CXCL10 niż ich agresywne odpowiedniki. Gdy badacze celowo wyłączają CXCL10 w komórkach dormantnych i wszczepiają je myszom z nieuszkodzonym układem odpornościowym, wcześniej ciche komórki szybko tworzą guzy. Zablokowanie receptora CXCR3 przeciwciałem daje podobny skutek. W obu przypadkach komórki nowotworowe przełamują impas z układem odpornościowym i zaczynają rosnąć, co pokazuje, że oś CXCL10/CXCR3 nie jest jedynie skorelowana z dormancją — jest wymagana do jej utrzymania.
Jak zmiana lokalnego mikrośrodowiska przechyla szalę
Obniżenie poziomu CXCL10 to coś więcej niż ingerencja w pojedynczy szlak; przekształca cały lokalny krajobraz immunologiczny. W guzach, które utraciły CXCL10, ubywa pomocnych limfocytów CD4 i CD8, podczas gdy zwiększa się liczba niektórych komórek mieloidalnych, które mogą tłumić odpowiedzi immunologiczne. Liczby komórek NK i komórek dendrytycznych również się zmieniają. Ten wzorzec występuje zarówno w guzach pierwotnych, jak i w płucach, do których komórki nowotworowe mogą docierać i ukrywać się. Nawet kiedy przerzuty płucne są zbyt małe, by zobaczyć je pod mikroskopem, markery molekularne wykazują, że więcej komórek nowotworowych z powodzeniem zasiedla płuca przy braku CXCL10, a mniej limfocytów T przenika do tych tkanek. Jednak u myszy całkowicie pozbawionych funkcjonującego układu odpornościowego usunięcie CXCL10 nie ma znaczenia — komórki dormantne rosną niezależnie — co podkreśla, że ten sygnał działa poprzez kontrolę immunologiczną, a nie przez bezpośrednie hamowanie wzrostu komórek nowotworowych.
Dlaczego zwiększenie sygnału pomaga, ale nie jest magicznym przełącznikiem
Zespół testuje także odwrotny pomysł: czy zwiększenie CXCL10 może przemienić agresywny guz w dormantny? Gdy inżynierują szybko rosnące komórki nowotworowe, by produkowały dodatkowe CXCL10, guzy rosną wolniej i pojawiają się później, a pewne typy komórek odpornościowych we krwi zwiększają się. Jednak pełna dormancja nie rozwija się; ostatecznie wszystkie myszy i tak rozwijają guzy. To sugeruje, że choć CXCL10 jest niezbędny do utrzymania dormancji, gdy reszta mechanizmów odpornościowych jest sprawna, sam w sobie nie potrafi zbudować tego złożonego stanu od podstaw. Inne szlaki muszą współdziałać, aby stworzyć długotrwałą równowagę między atakiem immunologicznym a przetrwaniem komórek nowotworowych.
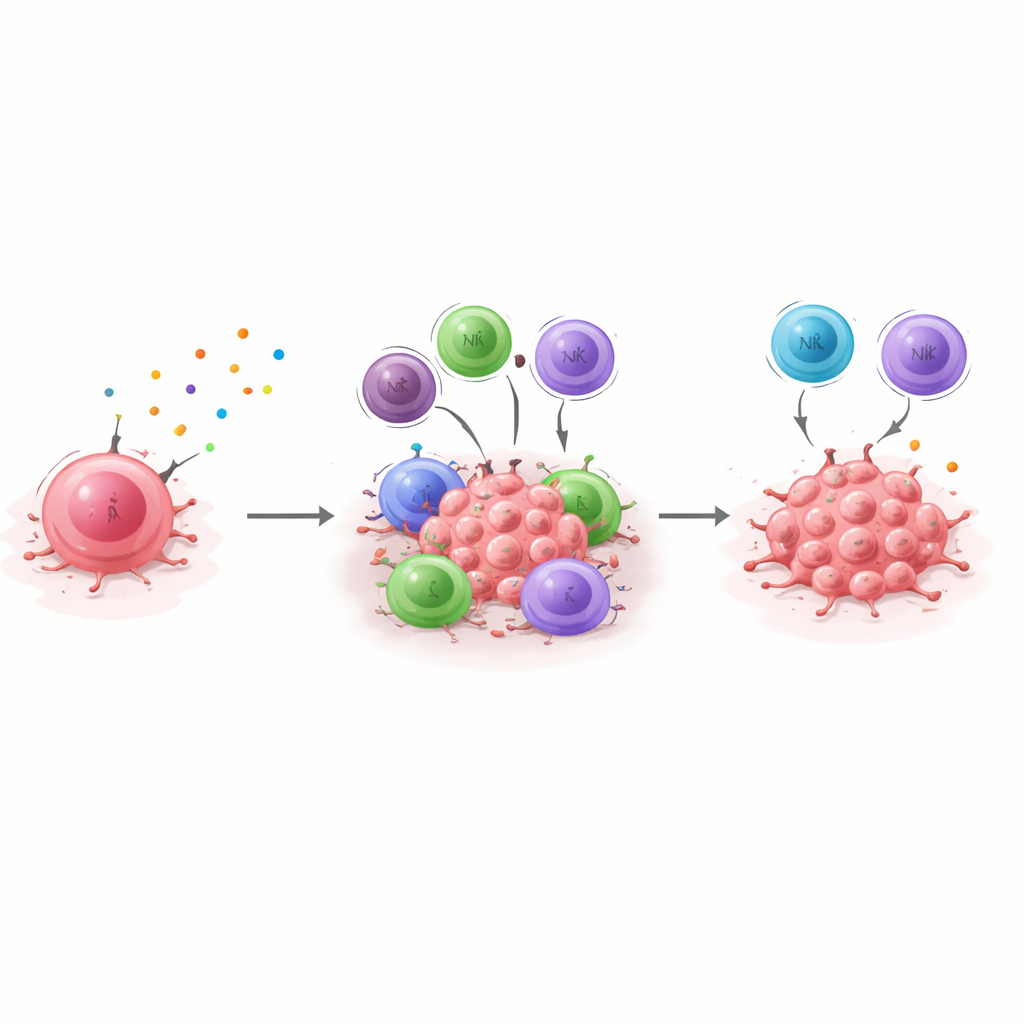
Od eksperymentów na myszach do prognozy dla pacjentów
Aby powiązać swoje odkrycia z chorobą ludzką, badacze wyprowadzają „sygnaturę dormancji” — zestaw genów, które konsekwentnie są wyżej ekspresjonowane w komórkach dormantnych i spadają po wyciszeniu CXCL10. Następnie analizują duże bazy danych pacjentów z rakiem piersi i sprawdzają, jak ta sygnatura koreluje z przeżyciem. W raku piersi potrójnie ujemnym pacjentki, których guzy wykazują wyższy poziom tej sygnatury dormancji, żyją dłużej całkowicie i mają tendencję do dłuższego pozostawania bez wznowy, co jest zgodne z tym, że immunologicznie kontrolowana dormancja opóźnia nawrót. Efekt nie jest obserwowany w ten sam sposób w guzach zależnych od hormonów, co podkreśla biologiczne różnice między podtypami raka piersi. Razem wyniki sugerują, że oś CXCL10/CXCR3 jest centralnym filarem immunologicznie pośredniczonej dormancji w raku piersi potrójnie ujemnym, a pomiar tej sygnatury dormancji mógłby pomóc zidentyfikować pacjentki, które prawdopodobnie skorzystają z terapii wzmacniających kontrolę immunologiczną — lub przeciwnie, które mogą wymagać bliższego, długoterminowego monitorowania, ponieważ ich rak jest słabiej utrzymywany w ryzach.
Cytowanie: Yilmaz, A., Haerri, L., Granda, M.E. et al. The CXCL10/CXCR3 axis is essential for sustaining immunological dormancy in triple-negative breast cancer. npj Breast Cancer 12, 36 (2026). https://doi.org/10.1038/s41523-026-00903-6
Słowa kluczowe: rak piersi potrójnie ujemny, dormancja guza, nadzór immunologiczny, sygnalizacja chemokin, oś CXCL10 CXCR3