Clear Sky Science · pl
Klasyfikatory zdrowej tkanki piersi (NBT): postępy w klasyfikacji przedziałów w normalnej histologii piersi
Poszukiwanie wczesnych wskazówek w „normalnej” tkance piersi
Badania przesiewowe raka piersi zwykle koncentrują się na guzach lub podejrzanych zgrubieniach, ale istotne sygnały ostrzegawcze mogą pojawiać się znacznie wcześniej, zanim guz w ogóle się uformuje. W tym badaniu zadano proste pytanie o dalekosiężnych konsekwencjach: czy sztuczna inteligencja (AI) może nauczyć się, jak wygląda prawdziwie zdrowa tkanka piersi, tak aby nawet drobne, wczesne zmiany były wyraźniej widoczne? Poprzez nauczenie komputerów rozpoznawania głównych składników budulcowych normalnej tkanki piersi, badacze mają nadzieję stworzyć mocniejszą mapę odniesienia do wychwytywania pierwszych etapów rozwoju raka.
Dlaczego zdrowa tkanka piersi jest ważna
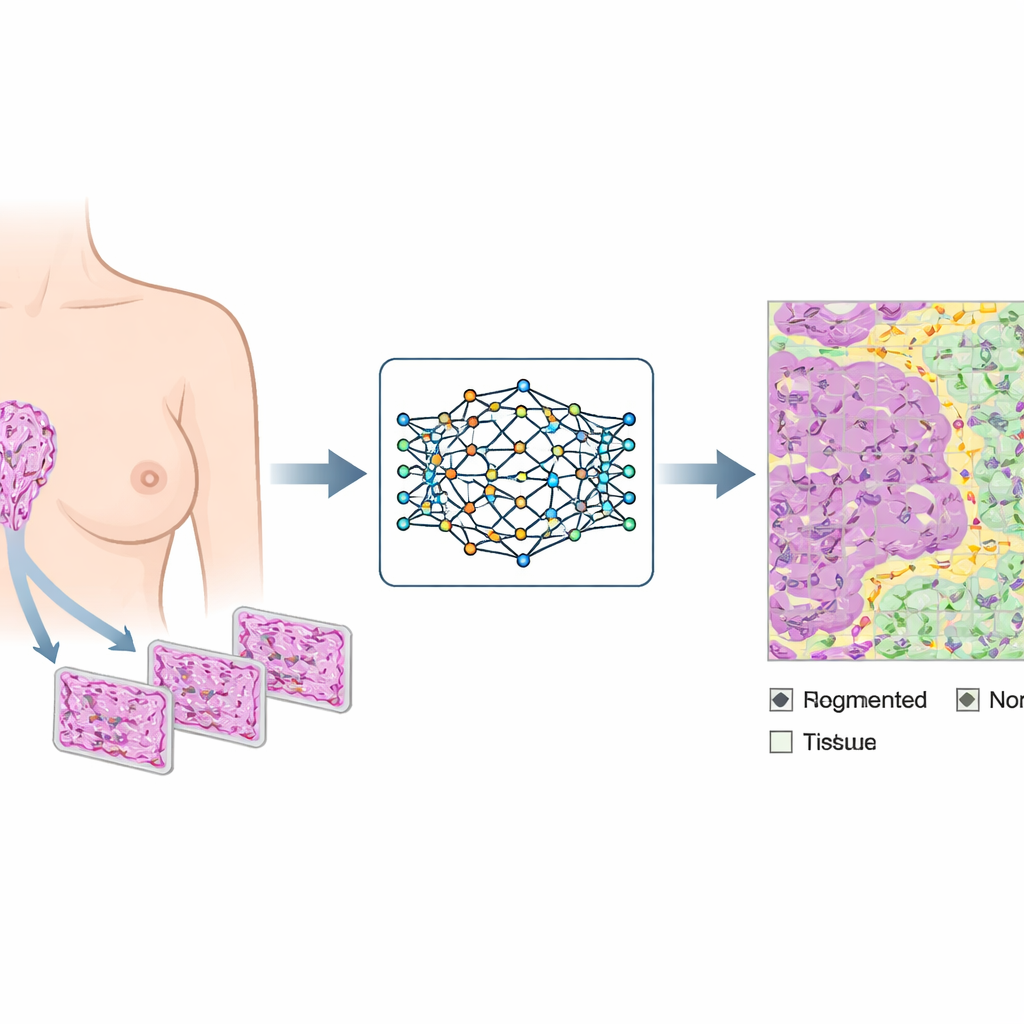
Większość badań nad rakiem piersi skupia się na tkance chorobowej, tymczasem nowotwór zaczyna się w tkance wyglądającej pod mikroskopem na prawidłową. W piersi struktury produkujące mleko i otaczająca je tkanka podporowa znajdują się w mieszaninie obszarów włóknistych i tłuszczowych. Subtelne zmiany w tych rejonach, zwłaszcza wokół zrazików (drobnych pęcherzyków produkujących mleko) i otaczającego je zrębu (tkanki łącznej wspierającej), mogą sygnalizować zwiększone ryzyko raka. Ma to szczególne znaczenie dla kobiet noszących dziedziczne mutacje BRCA1 lub BRCA2 oraz dla tych poddawanych zabiegom zmniejszającym ryzyko. Aby odczytać te ciche sygnały, naukowcy potrzebują precyzyjnych, ilościowych metod opisu, jak wygląda „normalne” w różnych populacjach i ośrodkach medycznych.
Budowa zróżnicowanej biblioteki zdrowych preparatów
Zespół zgromadził 70 obrazów cyfrowych o wysokiej rozdzielczości normalnej tkanki piersi z pięciu instytucji w Wielkiej Brytanii, Holandii, Szwajcarii oraz z publicznego banku tkanek. Próbki pochodziły od kobiet w wieku 16–74 lat o różnym profilu, w tym ochotniczek zdrowych, kobiet poddawanych redukcji piersi, nosicielek dziedzicznych zmian genetycznych zwiększających ryzyko oraz kobiet z rakiem w przeciwnej piersi. Ekspertki i eksperci patologii starannie oznaczyli trzy kluczowe składniki na każdym preparacie: nabłonek (warstwy komórek wyściełające przewody i zraziki), zrąb (tkanka włóknista i łączna) oraz adipocyty (komórki tłuszczowe). Ta czasochłonna anotacja dała bogaty i zróżnicowany zestaw odniesienia, odzwierciedlający rzeczywiste różnice w przygotowaniu tkanek, barwieniu i skanowaniu.
Nauczanie komputera rozpoznawania typów tkanek
Wykorzystując opisaną bibliotekę, badacze trenowali modele uczenia głębokiego — nazwane NBT-Classifiers — aby rozpoznawały trzy typy tkanek na podstawie małych fragmentów obrazu wyciętych z większych preparatów. Testowali różne rozmiary fragmentów i ustawienia techniczne, takie jak ujednolicanie barwienia oraz architektury sieci neuronowych, ostatecznie znajdując kombinację działającą najlepiej. Przy ocenie na zupełnie niezależnych kolekcjach normalnych preparatów z innych ośrodków modele poprawnie rozróżniały nabłonek, zrąb i tłuszcz z niemal idealną dokładnością. Wizualne „mapy ciepła” pokazały, że AI skupia się na biologicznie istotnych strukturach, takich jak obszary bogate w komórki, włókna kolagenowe i granice komórek tłuszczowych, odzwierciedlając sposób, w jaki ludzie-patolodzy interpretują tkankę.
Co sprawia, że tkanka jest prawidłowa
Aby dowiedzieć się, czy trening wyłącznie na zdrowej tkance daje przewagę, autorzy porównali swój model z istniejącym narzędziem trenowanym na mieszance próbek normalnych, przednowotworowych i nowotworowych. Oba potrafiły identyfikować szerokie typy tkanek, ale nowe NBT-Classifiers lepiej uchwyciły drobnoziarnistą architekturę prawdziwie normalnego nabłonka piersi. Gdy wystawiono je na fragmenty zawierające wczesne zmiany i guzy, model uczony tylko na zdrowych próbkach bardziej niezawodnie oddzielał obszary wyglądające zdrowo od nieprawidłowych. Wskazuje to, że nauczył się ostrzejszej definicji normalnej tkanki piersi, co może pomóc uwypuklić subtelne odchylenia towarzyszące wczesnej chorobie.
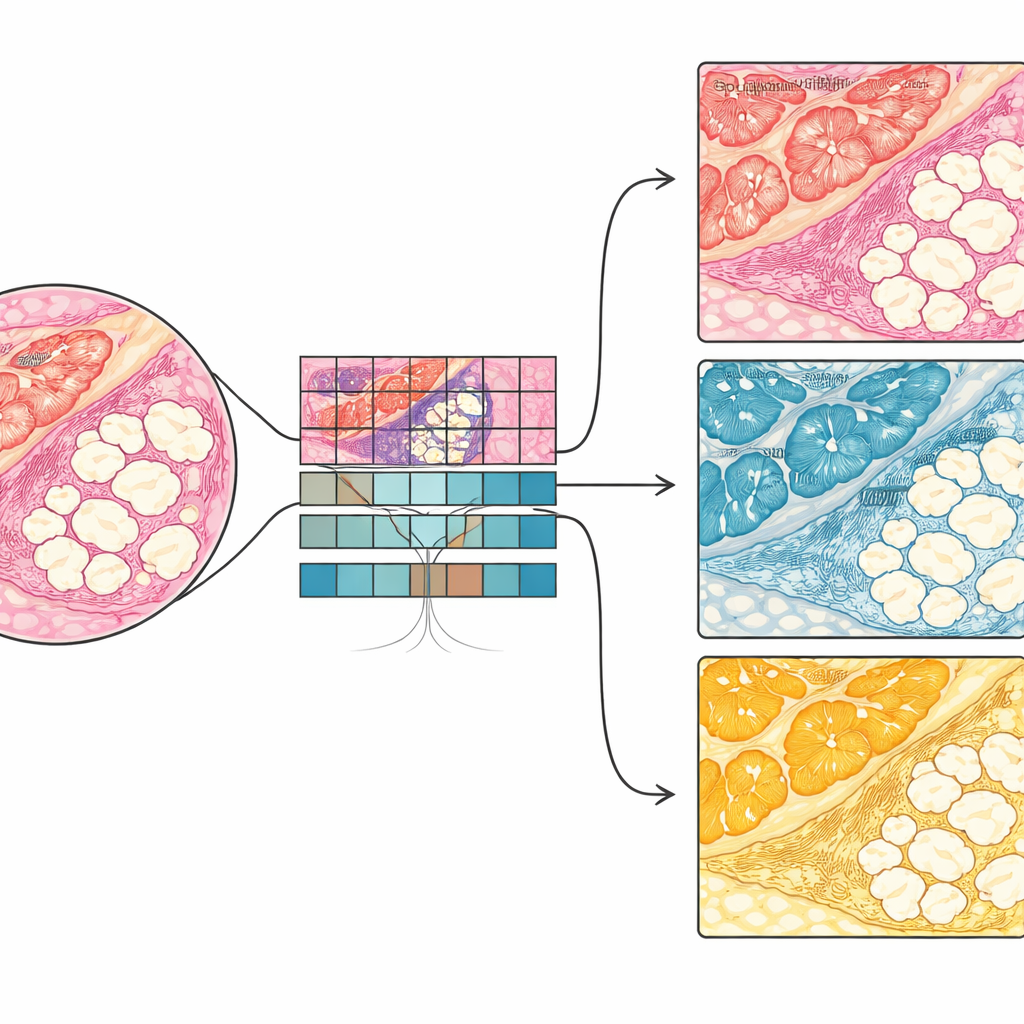
Od całych preparatów do wybranych regionów
Ponieważ modele działają na poziomie fragmentów, można je stosować na całych cyfrowych skanach, automatycznie kolorując każdą małą powierzchnię jako nabłonek, zrąb lub tłuszcz. Badacze zbudowali przepływ pracy typu end-to-end, który najpierw wykrywa, gdzie na preparacie obecna jest tkanka, a następnie uruchamia NBT-Classifiers, tworząc szczegółowe mapy przedziałów tkankowych. Z tych map system potrafi zlokalizować poszczególne zraziki i ich bezpośrednie otoczenie, wygenerować maski do dalszych pomiarów oraz przekazać wybrane rejony do bardziej zaawansowanych narzędzi analitycznych. Ułatwia to badanie specyficznych mikrośrodowisk — na przykład zrębu tuż poza zrazikami — gdzie mogą pojawiać się wczesne zmiany związane z rakiem, oraz łączenie cech strukturalnych z innymi typami danych, takimi jak przestrzenne mapy genów czy białek w przyszłych pracach.
Co to znaczy dla przyszłej prewencji raka piersi
Mówiąc prosto, to badanie pokazuje, że AI można wyszkolić do rozpoznawania elementów składowych zdrowej tkanki piersi z niezwykłą precyzją i w sposób zrozumiały dla patologów. Przekształcając ogromne, złożone cyfrowe preparaty w ustrukturyzowane mapy obszarów nabłonkowych, włóknistych i tłuszczowych, NBT-Classifiers tworzą wiarygodną podstawę tego, jak wygląda normalność wśród wielu kobiet i szpitali. Ten jaśniejszy obraz normalności może ułatwić wykrycie subtelnych śladów rozwoju raka wcześniej niż jest to obecnie możliwe, wspierając przyszłe narzędzia pomagające identyfikować kobiety o wyższym ryzyku i kierować strategią zapobiegania, zanim pojawią się widoczne guzy.
Cytowanie: Chen, S., Parreno-Centeno, M., Booker, G. et al. Normal breast tissue (NBT)-classifiers: advancing compartment classification in normal breast histology. npj Breast Cancer 12, 41 (2026). https://doi.org/10.1038/s41523-026-00896-2
Słowa kluczowe: zdrowa tkanka piersi, patologia obliczeniowa, uczenie głębokie, wczesne wykrywanie raka, histologia cyfrowa