Clear Sky Science · pl
Sygnalizacja CD52 przez makrofagowy Siglec‑G jako cel terapeutyczny w immunoterapii przeciwnowotworowej
Dlaczego niektóre raki piersi ukrywają się przed układem odpornościowym
Rak piersi potrójnie ujemny jest jedną z najgroźniejszych postaci raka piersi, ponieważ szybko się rozsiewa i brakuje dla niego wielu powszechnych celów terapeutycznych. To badanie bada nowo odkryty mechanizm, dzięki któremu guzy te mogą ukrywać się przed obroną organizmu, i pokazuje, że zablokowanie tej drogi ucieczki może poprawić skuteczność terapii opartych na układzie odpornościowym.
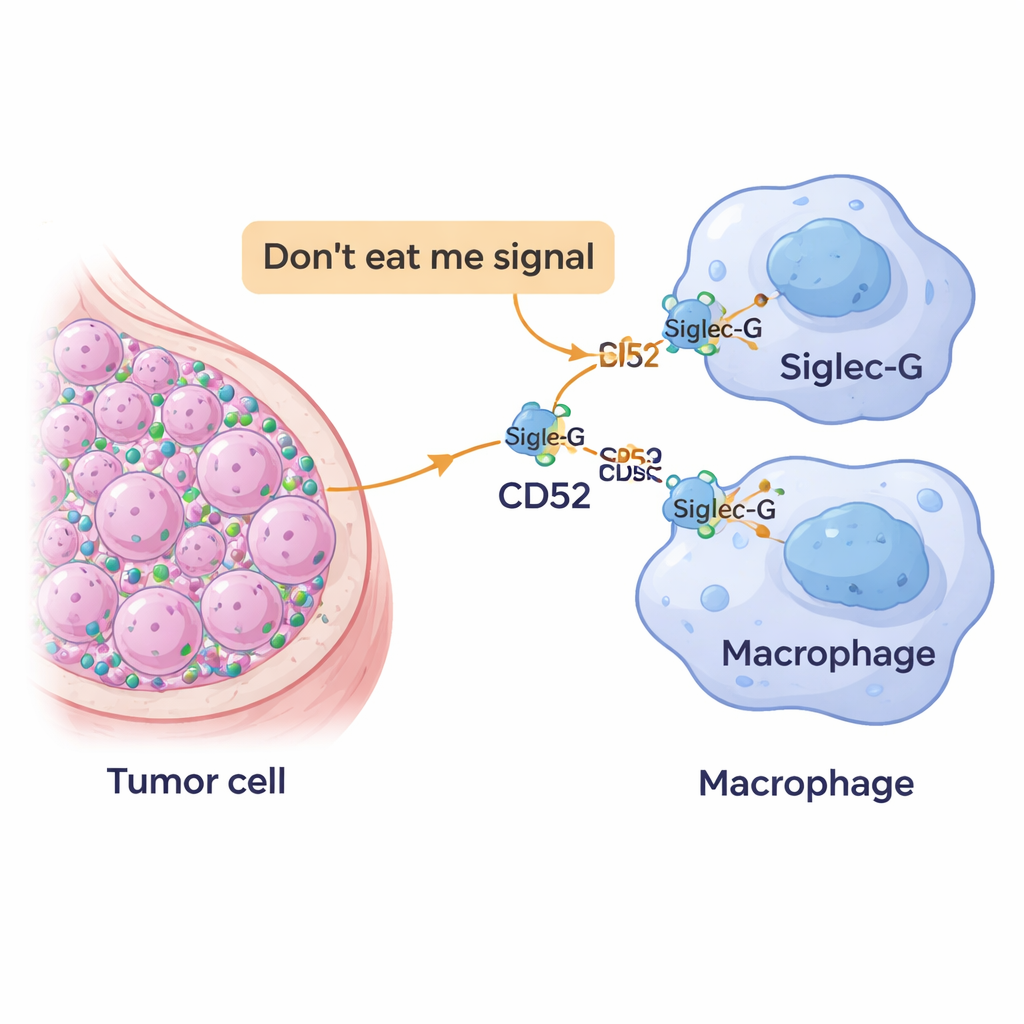
Nowa flaga „nie jedz mnie” na komórkach nowotworowych
Nasz układ odpornościowy polega na komórkach żernych zwanych makrofagami, które patrolują tkanki i pochłaniają niebezpieczne lub nieprawidłowe komórki. Aby uniknąć przypadkowego zniszczenia, zdrowe komórki prezentują na powierzchni markery sygnalizujące w efekcie „należę tutaj”. Komórki nowotworowe często przejmują ten mechanizm, nadużywając takich sygnałów i przekształcając je w silne flagi „nie jedz mnie”. Badacze skupili się na cząsteczce zwanej CD52, znanej już w kontekście nowotworów krwi i chorób autoimmunologicznych, i zapytali, czy komórki raka piersi również używają jej, by uciec przed atakiem makrofagów.
Wykrycie CD52 w agresywnych guzach piersi
Zespół przeanalizował duże publiczne bazy danych dotyczące nowotworów oraz próbki tkanek od pacjentek. Stwierdzili, że guzy piersi, a zwłaszcza potrójnie ujemne, wytwarzają więcej CD52 niż prawidłowa tkanka piersiowa. Co więcej, guzy z wyższym poziomem CD52 były częściej gorzej zróżnicowane, cecha często związana z bardziej agresywną chorobą. Równocześnie komórki odpornościowe w obrębie i wokół guzów nosiły wysokie poziomy partnera molekularnego nazwanego Siglec‑10 (oraz jego mysiego odpowiednika Siglec‑G), który znajduje się na makrofagach i może przekazywać do nich sygnały uspokajające. Razem te obserwacje sugerowały, że CD52 na komórkach nowotworowych może bezpośrednio komunikować się z Siglec‑G na makrofagach, powstrzymując je od wykonywania swojej funkcji.
Wyłączenie CD52, aby uwolnić makrofagi
Aby sprawdzić ten pomysł, naukowcy użyli narzędzi do edycji genów, by usunąć CD52 z mysich komórek raka piersi potrójnie ujemnego. Gdy zmodyfikowane komórki zmieszano z makrofagami w laboratorium, makrofagi połknęły znacząco więcej komórek nowotworowych niż w przypadku kontaktu z niezmodyfikowanymi komórkami raka. Co istotne, same komórki nowotworowe nie wykazywały zmian tempa wzrostu ani śmierci po utracie CD52, co wskazuje, że kluczowy efekt dotyczył rozpoznawania immunologicznego, a nie biologii samych komórek nowotworowych. Gdy te same komórki guza wszczepiono myszom, komórki pozbawione CD52 tworzyły mniejsze guzy i były otoczone makrofagami wykazującymi więcej oznak fagocytozy komórek nowotworowych. Jeśli makrofagi zostały usunięte z myszy, przewaga w zahamowaniu wzrostu znikała, potwierdzając, że główną rolą CD52 jest osłanianie guzów przed byciem zjedzonymi.
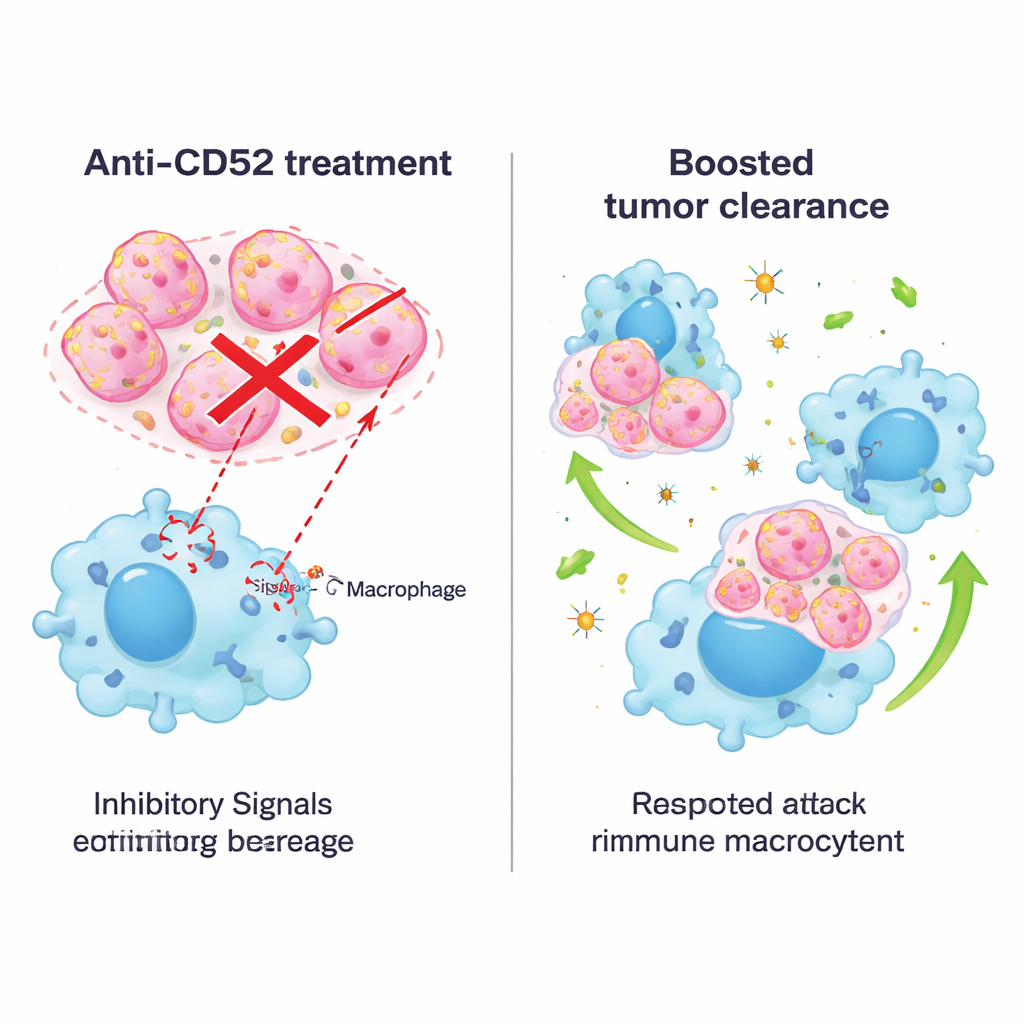
Blokowanie sygnału przeciwciałami i łączenie terapii
Ponieważ leki ukierunkowane przeciw CD52 są już stosowane w innych chorobach, badacze przetestowali następnie przeciwciało blokujące w modelach mysich. Leczenie myszy z guzami przeciwciałem anty‑CD52 zmniejszało wzrost nowotworu, wydłużało przeżycie i nie powodowało oczywistych uszkodzeń narządów ani utraty masy ciała. W hodowlach podobne przeciwciała zwiększały zdolność zarówno mysich, jak i ludzkich makrofagów do fagocytowania komórek raka piersi z kilku podtypów, nie tylko potrójnie ujemnego. Zespół połączył następnie blokadę CD52 z terapią anty‑PD‑1, szeroko stosowanym lekiem blokującym punkt kontrolny ukierunkowanym na limfocyty T. W spontanicznym mysim modelu raka piersi potrójnie ujemnego połączenie zadziałało lepiej niż każdy z zabiegów osobno: guzy kurczyły się bardziej, makrofagi stawały się bardziej zapalne i aktywne, a do guza wchodziło więcej silnych komórek T zabijających nowotwór, podczas gdy mniej było komórek T wykazujących cechy wyczerpania.
Co to oznacza dla przyszłej opieki nad rakiem piersi
Ta praca odsłania CD52 jako wcześniej nierozpoznany sygnał „nie jedz mnie”, którego komórki raka piersi potrójnie ujemnego używają, by odpierać makrofagi. Przerywając rozmowę między CD52 na komórkach nowotworowych a Siglec‑G na makrofagach, badacze byli w stanie ponownie pobudzić zarówno komórki odpornościowe wrodzone, jak i pośrednio komórki T, szczególnie w połączeniu z blokadą PD‑1. Choć potrzebne są dalsze badania bezpieczeństwa i badania kliniczne — ponieważ CD52 występuje również na wielu normalnych komórkach odpornościowych — wyniki wskazują na obiecującą strategię podwójnej blokady punktów kontrolnych, która mogłaby pomóc przekształcić trudne w leczeniu, oporne na immunoterapię guzy piersi w takie, które lepiej reagują na immunoterapię.
Cytowanie: Qin, X., Chang, Y., Qiu, Y. et al. CD52 signaling via macrophage Siglec-G represents a therapeutic target for cancer immunotherapy. npj Breast Cancer 12, 29 (2026). https://doi.org/10.1038/s41523-026-00895-3
Słowa kluczowe: rak piersi potrójnie ujemny, makrofagi, immunoterapia, CD52, blokada punktów kontrolnych