Clear Sky Science · pl
Wspólne dostarczenie chemokiny CXCL9 i liganda kostymulacyjnego TNFSF9 przez komórki macierzyste mezenchymalne przeprogramowuje mikrośrodowisko immunologiczne w potrójnie ujemnym raku piersi
Dlaczego to nowe podejście do raka piersi ma znaczenie
Potrójnie ujemny rak piersi jest jedną z najgroźniejszych postaci raka piersi, ponieważ rośnie szybko, wcześnie się rozprzestrzenia i pozbawiony jest powszechnych celów hormonalnych, na których opierają się wiele terapii. Immunoterapia wzbudziła nadzieje, jednak u wielu pacjentów komórki obronne organizmu po prostu nie wnikają do guza w wystarczającej liczbie, by przynieść efekt. W badaniu zbadano pomysłowe rozwiązanie: użycie żywych komórek jako ukierunkowanych „ciężarówek dostawczych”, które wprowadzają sygnały wzmacniające odpowiedź immunologiczną bezpośrednio do trudno leczonych guzów, co potencjalnie mogłoby uczynić więcej pacjentów podatnymi na skuteczne terapie immunologiczne.
Trudny nowotwór z zbyt małą pomocą ze strony układu odpornościowego
Standardowe leczenie potrójnie ujemnego raka piersi — operacja, chemioterapia i radioterapia — często nie zapobiega nawrotom, a średnie przeżycie w zaawansowanej chorobie wciąż nie przekracza dwóch lat. Jednym z kluczowych powodów jest to, że wiele z tych guzów jest „zimnych”, czyli zawiera niewiele komórek walczących z rakiem. Analizy dużych baz danych pacjentów wykazały, że osoby, których guzy naturalnie wytwarzają większe ilości dwóch cząsteczek związanych z odpornością, CXCL9 i TNFSF9, mają tendencję do dłuższego przeżycia i większej liczby limfocytów T oraz komórek NK w obrębie guza. CXCL9 to sygnał chemiczny przyciągający komórki odpornościowe do tkanki, podczas gdy TNFSF9 działa jak dodatkowy „przełącznik startu”, który pomaga tym komórkom skuteczniej atakować. Wzorzec sugerował, że podniesienie poziomu obu sygnałów bezpośrednio w guzie może przechylić szalę na korzyść układu odpornościowego.
Przekształcanie komórek macierzystych w inteligentne ciężarówki dostawcze
Naukowcy skupili się na komórkach macierzystych mezenchymalnych pozyskanych z oddanych ludzkich pępowin. Komórki te mają użyteczną właściwość: po wstrzyknięciu do krwiobiegu myszy z guzami piersi naturalnie kierują się w miejsca guza i utrzymują tam przez dni, jednocześnie w dużej mierze omijając normalne organy. Zespół genetycznie zmodyfikował te komórki tak, by uwalniały CXCL9 i eksponowały TNFSF9 na swojej powierzchni, tworząc terapię komórkową o podwójnym działaniu nazwaną MSC‑T9C9. Badania laboratoryjne wykazały, że zmodyfikowane komórki wydzielają wysokie poziomy CXCL9 i silnie aktywują mysie limfocyty T i komórki NK, nie zmieniając jednocześnie własnego wzrostu ani nie wywołując nowotworów. To czyniło je obiecującymi kandydatami na ukierunkowanych wzmacniaczy odpornościowych.
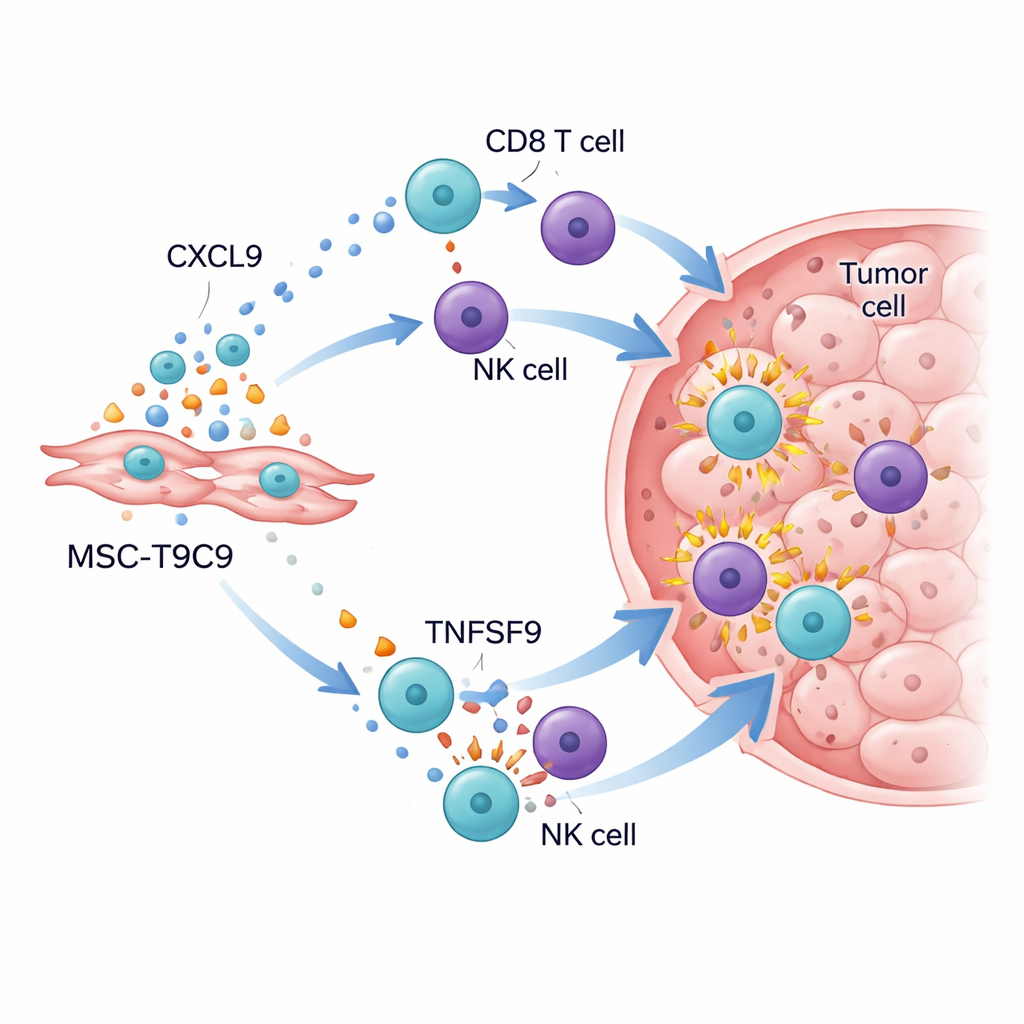
Przywołanie pola bitwy odpornościowej guza
Gdy zmodyfikowane komórki podano myszom z potrójnie ujemnymi guzami piersi, wyniki były uderzające. U myszy z prawidłowo działającym układem odpornościowym wielokrotne wstrzyknięcia MSC‑T9C9 znacznie spowolniły wzrost guza i zwiększyły umieranie komórek nowotworowych, podczas gdy kontrolne komórki macierzyste miały niewielki efekt. Szczegółowa analiza guzów wykazała dramatyczny wzrost liczby cytotoksycznych limfocytów CD8 i komórek NK oraz wyższe poziomy silnych molekuł efektorowych, takich jak granzyma B, interferon‑γ, czynnik martwicy nowotworów‑α i interleukina‑2. Jednocześnie środowisko guza przesunęło się z stanu supresyjnego: wzrosła liczba prozapalnych makrofagów wspierających odpowiedź, a chociaż komórki regulatorowe T wciąż były obecne, zostały przytłoczone przez nową falę komórek efektorowych. U myszy z zaburzeniami odporności, pozbawionych komórek T i NK, MSC‑T9C9 nie spowolniło wzrostu guza, co potwierdza, że korzyść polega na mobilizacji własnych mechanizmów obronnych organizmu.
Przygotowanie guzów do terapii z blokadą punktów kontrolnych
Nowoczesne leki immunoterapeutyczne, takie jak przeciwciała przeciw PD‑1, zwalniają molekularne „hamulce” na limfocytach T, ale działają najlepiej, gdy w guzie jest już odpowiednia liczba tych komórek. Badanie wykazało, że MSC‑T9C9 nie tylko przyciąga więcej limfocytów CD8 do guzów, lecz także wprowadza je w wysoce aktywny, lecz wrażliwy na hamowanie stan charakteryzujący się obecnością receptora PD‑1. W modelu myszy połączenie MSC‑T9C9 z lekiem przeciw PD‑1 dało najsilniejsze zmniejszenie guzów i najdłuższe przeżycie w porównaniu z każdym z tych zabiegów stosowanym osobno. Analizy ludzkich zbiorów danych onkologicznych wspierały ten pomysł: pacjenci z wyższymi łącznymi poziomami TNFSF9 i CXCL9 mieli większą szansę skorzystać z terapii blokujących punkty kontrolne, co sugeruje, że ta sama biologia może odnosić się do ludzi.
Bezpieczeństwo i przyszłe perspektywy
Każde leczenie wzmacniające odporność budzi obawy o niebezpieczne działania niepożądane, takie jak uogólnione zapalenie czy uszkodzenie narządów. Co budzi optymizm, myszy otrzymujące MSC‑T9C9 zachowywały normalną masę i zachowanie, nie wykazywały widocznych uszkodzeń głównych narządów i miały prawidłowe wyniki badań krwi oraz parametrów wątroby i nerek. Co ważne, wzrost aktywności immunologicznej był w dużej mierze ograniczony do samego guza, a sygnały zapalne we krwi nie wzrosły. Choć przed próbami u ludzi potrzeba więcej badań — w tym testów w bardziej realistycznych modelach i starannego doboru dawek — badanie sugeruje, że ukierunkowanie zmodyfikowanych komórek macierzystych do guzów, aby przywołać i aktywować komórki odpornościowe, może być ukierunkowanym i bezpieczniejszym sposobem przemiany „zimnych” potrójnie ujemnych raków piersi w „gorące”, lepiej reagujące na immunoterapię.
Cytowanie: Ye, P., Wen, Y., Liu, R. et al. Co-delivery of chemokine CXCL9 and costimulatory ligand TNFSF9 by mesenchymal stem cells reprograms the immune microenvironment for triple-negative breast cancer. npj Breast Cancer 12, 30 (2026). https://doi.org/10.1038/s41523-026-00893-5
Słowa kluczowe: potrójnie ujemny rak piersi, immunoterapia, komórki macierzyste mezenchymalne, mikrośrodowisko guza, blokada punktów kontrolnych