Clear Sky Science · pl
Interleukina‑1α pochodzenia gospodarza napędza immunosupresję guza przez przereprogramowanie związanych z nowotworem komórek mieloidalnych
Dlaczego te badania mają znaczenie dla pacjentek z rakiem
Immunoterapia zrewolucjonizowała leczenie niektórych nowotworów, ale wiele raków piersi wciąż unika rozpoznania przez układ odpornościowy. Artykuł bada mniej znanego sprawcę: cząsteczkę sygnałową zwaną interleukiną‑1 alfa (IL‑1α) wytwarzaną nie przez komórki nowotworowe, lecz przez normalne komórki gospodarza. Autorzy pokazują, że IL‑1α pochodzenia gospodarza może dyskretnie przekształcać komórki odpornościowe w sojuszników guza, a blokowanie tego sygnału u myszy prowadziło do kurczenia się lub ustępowania guzów piersi. Zrozumienie tego mechanizmu może pomóc w projektowaniu terapii, które zwiększą skuteczność immunoterapii u pacjentek z rakiem piersi.
Ukryty wpływowy czynnik w sąsiedztwie guza
Nowotwory nie rosną w izolacji; istnieją w zatłoczonym „sąsiedztwie” komórek odpornościowych, naczyń i tkanki łącznej, znanym jako mikrośrodowisko guza. Jednymi z najważniejszych mieszkańców są komórki mieloidalne, zwłaszcza makrofagi, które mogą albo zwalczać guz, albo go chronić. Klasyczne podręczniki dzielą makrofagi na M1 (walczące z guzem) i M2 (wspierające guz), ale w realnych guzach występuje wiele pośrednich stanów. Autorzy skupili się na IL‑1α, cząsteczce normalnie produkowanej przez tkanki niebędące nowotworowymi, aby sprawdzić, czy ten sygnał gospodarza kieruje napływające komórki mieloidalne ku pomocnym czy szkodliwym rolom w obrębie guzów piersi.
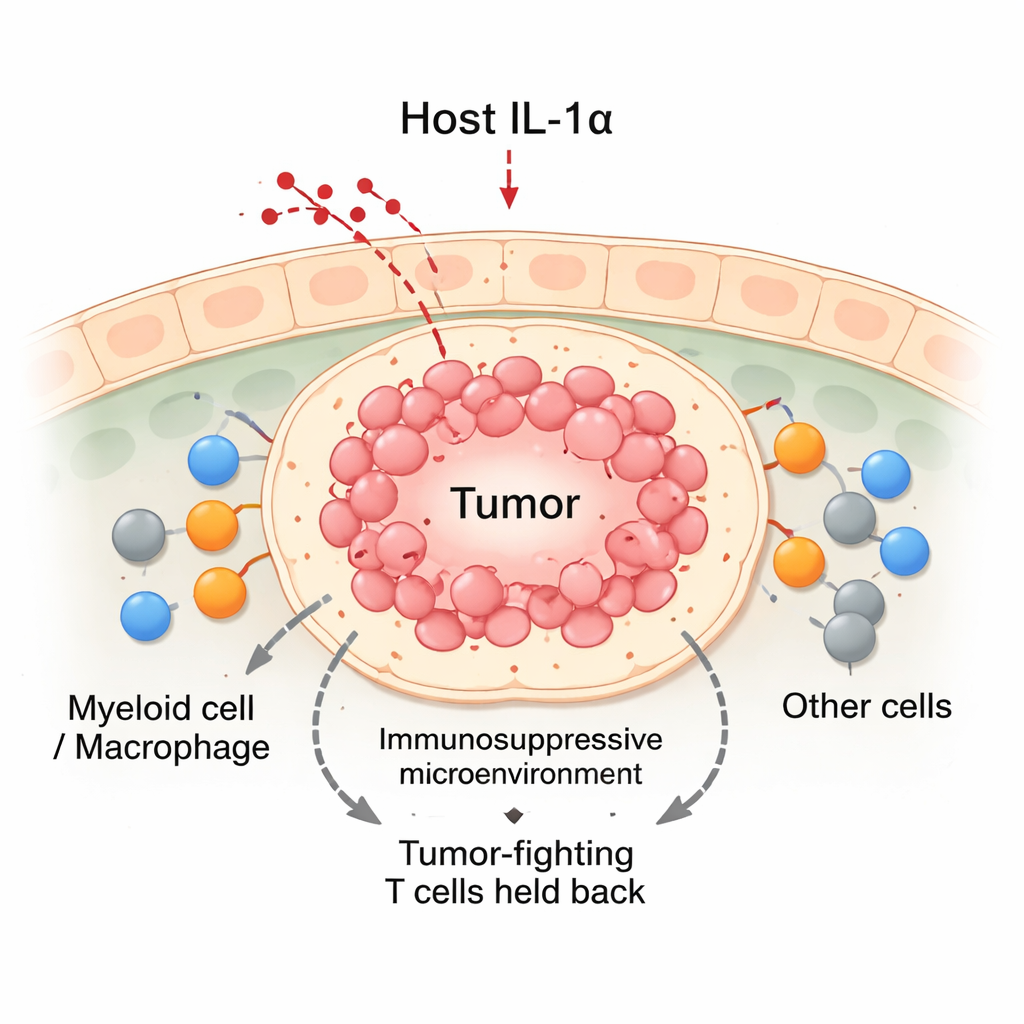
Wyłączenie IL‑1α przechyla szalę przeciwko guzom
Wykorzystując modele mysie raka piersi, zespół porównał zwierzęta normalne z myszami genetycznie pozbawionymi IL‑1α. Po przeszczepieniu komórek nowotworowych do gruczołów mlekowych, guzy u myszy normalnych rosły systematycznie. Natomiast u myszy pozbawionych IL‑1α guzy początkowo rosły przez około dwa tygodnie, po czym często ulegały regresji. Te regresyjne guzy zawierały więcej komórek odpornościowych ogółem, w tym znaczny napływ limfocytów CD8 „zabójców” oraz komórek mieloidalnych. Mimo że myszy pozbawione IL‑1α miały mniej krążących leukocytów we krwi, zgromadziły znacznie więcej komórek odpornościowych w miejscu guza. Szczegółowe analizy wykazały, że napływające limfocyty CD8 w guzach bez IL‑1α były bardziej aktywne, wytwarzały wyższe poziomy cytotoksycznych cząsteczek i wykazywały mniej oznak wyczerpania.
Jak IL‑1α przekształca związane z guzem komórki mieloidalne
Aby zrozumieć, co IL‑1α robi na poziomie komórkowym, badacze zastosowali sekwencjonowanie RNA pojedynczych komórek (scRNA‑seq), badając tysiące pojedynczych komórek z guzów. Odkryli, że tylko mała podgrupa makrofagów związanych z guzem — oznaczona receptorem CX3CR1 — produkowała IL‑1α. U myszy normalnych wiele napływających monocytów dojrzewało do tych makrofagów CX3CR1‑dodatnich, które wiązały się z zachowaniami immunosupresyjnymi. U myszy pozbawionych IL‑1α ta droga dojrzewania została zakłócona. Zamiast tego komórki mieloidalne częściej przyjmowały fenotyp iNOS‑dodatnich makrofagów zapalnych, kojarzony z aktywnością anty‑nowotworową. Funkcjonalnie, komórki mieloidalne z guzów bez IL‑1α mniej skutecznie indukowały hamulce takie jak PD‑1 i CTLA‑4 na komórkach T oraz wykazywały słabszą zdolność tłumienia proliferacji limfocytów T.
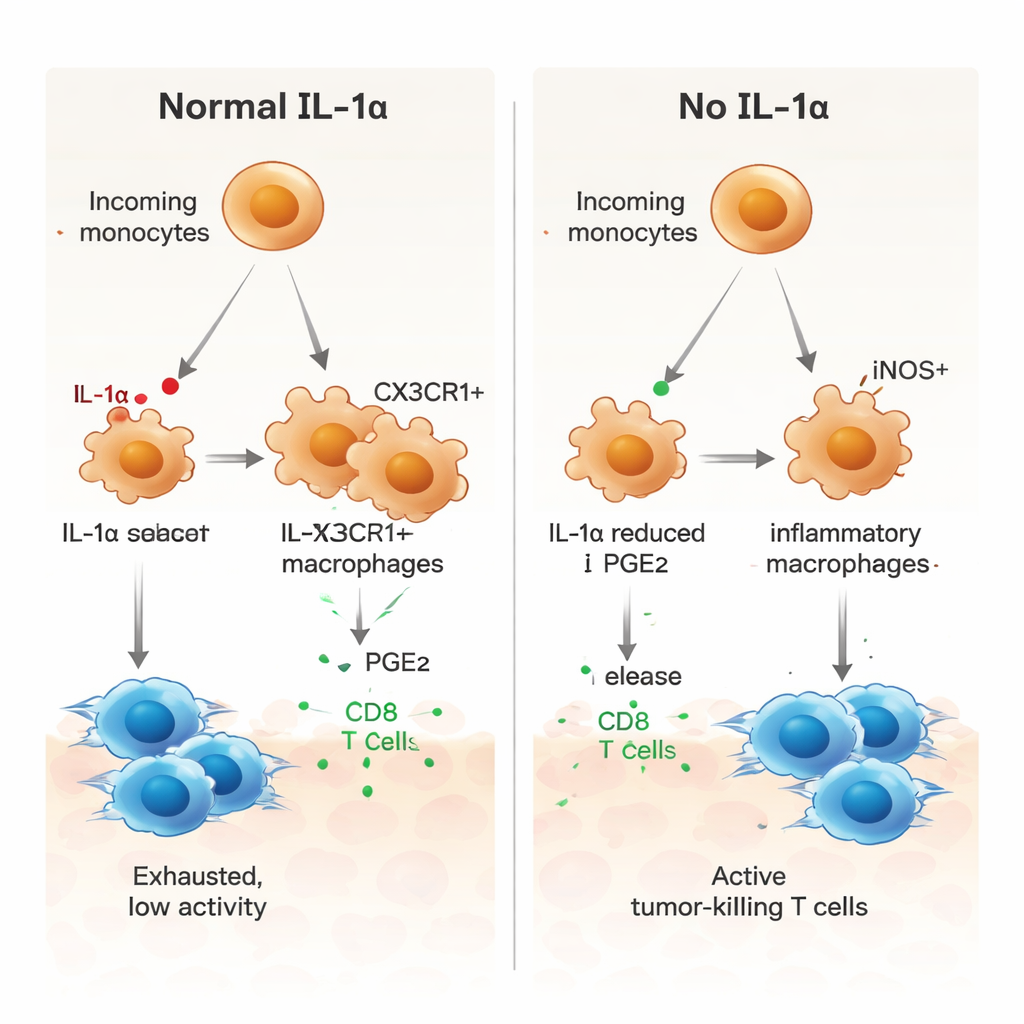
Kluczowa rola lipidowego posłańca, PGE2
Autorzy następnie badali, jak IL‑1α kieruje komórki mieloidalne ku stanowi wspierającemu guz. Analiza komunikacji danych scRNA‑seq wskazała kilka szlaków sygnałowych, w tym jeden z udziałem prostaglandyny E2 (PGE2), lipidowego mediatora znanego z promowania immunosupresji. W guzach pozbawionych IL‑1α makrofagi wykazywały niższą ekspresję receptorów dla czynnika wzrostu makrofagów (M‑CSF), receptorów TGF‑β oraz receptora dla PGE2, a pobliskie komórki stromalne wytwarzały mniej enzymów odpowiedzialnych za produkcję PGE2. W hodowlach laboratoryjnych makrofagi pochodzące z szpiku kostnego myszy bez IL‑1α wykazywały bardziej zapalny profil, z wyższym iNOS i niższym CX3CR1. Dodanie PGE2 odwracało tę zmianę i przywracało bardziej supresyjny wzorzec, podczas gdy blokada PGE2 w makrofagach normalnych przesuwała je ku stanowi prozapalnemu. Makrofagi pozbawione IL‑1α także silniej stymulowały proliferację swoistych dla guza limfocytów CD8, efekt osłabiany po ponownym dodaniu PGE2.
Łączenie wyników z myszy z immunologią człowieka
Aby sprawdzić, czy wyniki z modeli mysich odzwierciedlają biologię ludzką, zespół porównał sygnatury genowe różnych mysich podklastrów makrofagów z dużym panelem ludzkich komórek mieloidalnych kierowanych in vitro ku różnym stanom. Klastry makrofagów z guzów myszy normalnych przypominały ludzkie komórki przesunięte ku stanom M2‑podobnym, tłumiącym odporność, przez czynniki takie jak IL‑10, IL‑4 i glikokortykosteroidy. Natomiast te same klastry z guzów pozbawionych IL‑1α odpowiadały ludzkim komórkom w bardziej zapalnych, mniej supresyjnych warunkach. Co istotne, wzorce genowe związane z sygnalizacją PGE2 były wzbogacone w makrofagach zależnych od IL‑1α, lecz nieobecne przy braku IL‑1α, co wzmacnia tezę, że IL‑1α i PGE2 współdziałają w tworzeniu immunosupresyjnej niszy.
Co to może oznaczać dla przyszłych terapii raka piersi
Mówiąc wprost, badanie sugeruje, że cząsteczka pochodzenia gospodarza, IL‑1α, może dyskretnie „nakazywać” pewnym makrofagom ochronę guza i hamowanie komórek zabójczych T, częściowo przez sygnalizację PGE2. Gdy IL‑1α jest usunięta u myszy, makrofagi przechodzą w bardziej zapalny, przeciwnowotworowy stan, limfocyty CD8 stają się bardziej aktywne, a przeszczepione guzy piersi są często odrzucane. Ponieważ istniejące immunoterapie już dążą do ponownego pobudzenia wyczerpanych komórek T, ich łączenie z podejściami blokującymi IL‑1α lub jego szlak PGE2 mogłoby jeszcze bardziej przechylić mikrośrodowisko guza na korzyść układu odpornościowego pacjentki. Chociaż konieczne są dalsze badania nad bezpieczeństwem i skutecznością u ludzi, wyniki te wskazują na IL‑1α jako obiecujący nowy cel, który może uczynić raka piersi bardziej podatnym na atak immunologiczny.
Cytowanie: Keerthi Raja, M.R., Gupta, G., Atkinson, G. et al. Host-derived interleukin-1α drives tumor immunosuppression by reprogramming tumor-associated myeloid cells. npj Breast Cancer 12, 26 (2026). https://doi.org/10.1038/s41523-026-00890-8
Słowa kluczowe: immunoterapia raka piersi, mikrośrodowisko guza, makrofagi, interleukina-1 alfa, prostaglandyna E2