Clear Sky Science · pl
Ukierunkowane eliminowanie zakażeń zapalenia gruczołu mlekowego wywołanych przez Staphylococcus aureus za pomocą syntetycznych systemów dostarczających CRISPR‑Cas opartych na fagach
Walka z kosztowną infekcją w hodowli mleka
Mleko krów i innych zwierząt gospodarskich może zostać skażone przez bolesne zapalenie gruczołu mlekowego zwane mastitis, często wywoływane przez bakterię Staphylococcus aureus. Leczenie takich zakażeń zwykle wymaga długotrwałej kuracji antybiotykowej, co jest kosztowne, stresujące dla zwierząt i przyczynia się do narastającego problemu oporności na antybiotyki. W tym badaniu zbadano radykalnie odmienną strategię: przekształcenie naturalnego wirusopodobnego pasożyta bakterii w precyzyjną broń, która selektywnie tnie DNA bakterii i eliminuje zakażenia bez rozprzestrzeniania genów oporności.
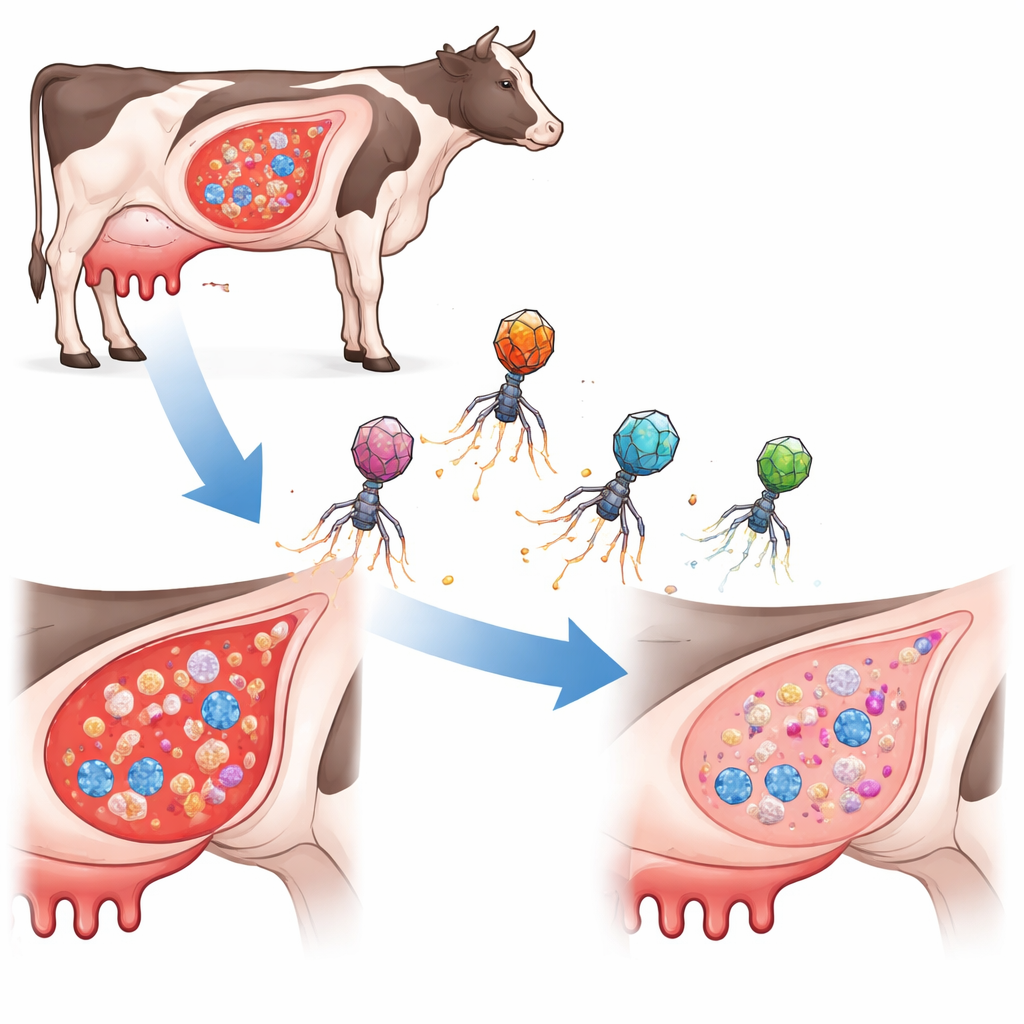
Nowy typ ukierunkowanego łowcy bakterii
Zamiast używać tradycyjnych antybiotyków czy zwykłych bakteriofagów (wirusów infekujących bakterie), badacze skonstruowali maleńkie elementy przenoszące DNA znane jako fagi‑indukowalne wyspy chromosomalne. W naturze wyspy te podróżują w osłonkach fagów, przeskakując między komórkami bakteryjnymi. Zespół przebudował je jako „ePICI”, które niosą narzędzie do edycji genów CRISPR‑Cas9 oraz krótkie sekwencje prowadzące skierowane przeciw trzem niewielkim, lecz istotnym regulatorowym RNA w S. aureus. Gdy ePICI wejdzie do komórki docelowej, syntetyzowany jest Cas9, który tnie chromosom bakterii w wybranym miejscu, zabijając komórkę od środka. Co istotne, te zaprojektowane cząstki nie replikują się samodzielnie, co ogranicza ich rozprzestrzenianie i zmniejsza ryzyko przypadkowego przenoszenia szkodliwych genów.
Jak bakteryjna osłona zmienia przebieg walki
S. aureus często przetrwa leczenie, tworząc biofilmy — lepkie społeczności zanurzone we własnej macierzy. Zespół porównał dwa powszechne typy macierzy: jedną zbudowaną głównie z białka zwanego Bap oraz drugą zrobioną z polisacharydu znanego jako PIA/PNAG. W testach laboratoryjnych biofilmy bogate w Bap silnie chroniły bakterie przed ePICI i przed standardowym fagiem pomocniczym, działając jak gęsta zbroja blokująca infekcję. Natomiast biofilmy oparte na polisacharydzie cukrowym ułatwiały zabijanie bakterii, prawdopodobnie dlatego, że enzymy na osłonkach wirusowych potrafią rozkładać te cukry i pomóc cząstkom dotrzeć do celu.
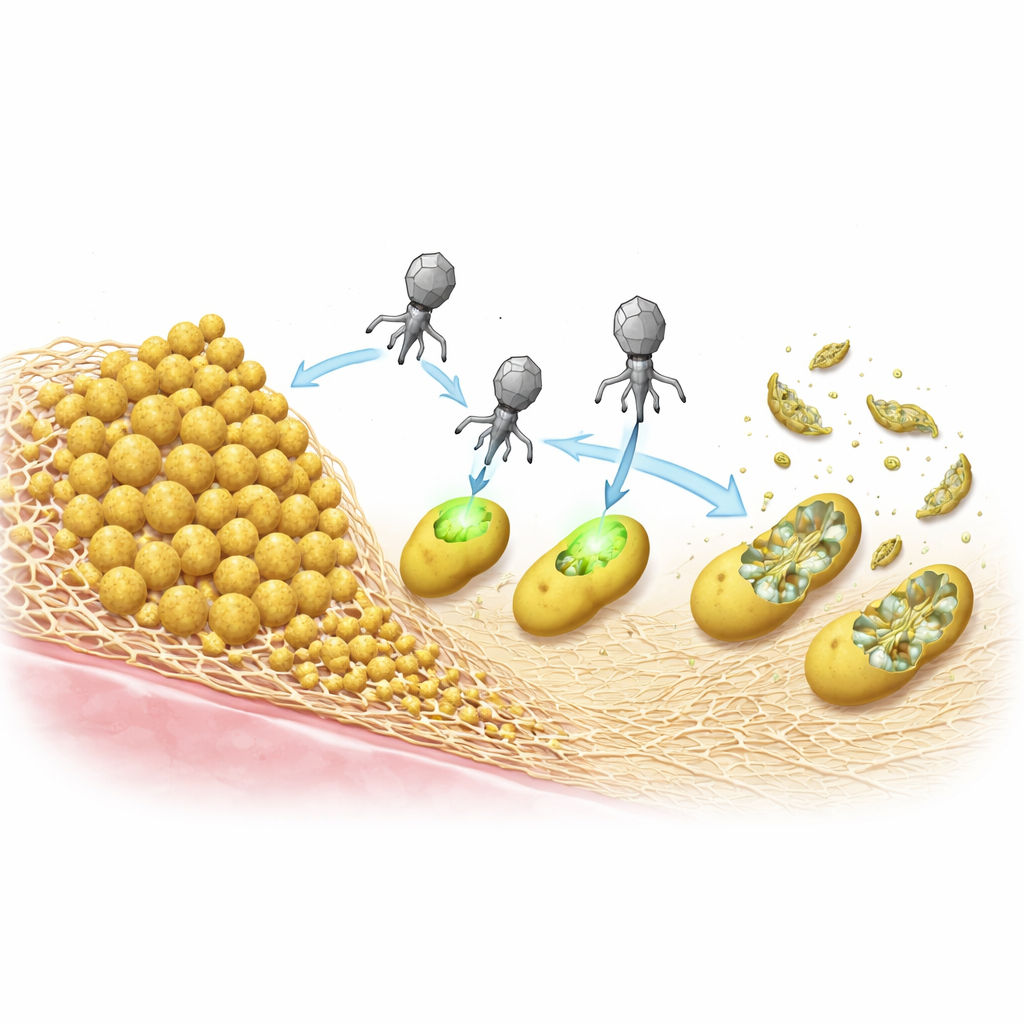
Zabijanie bakterii bez łączenia ich DNA
Po wejściu do komórki ePICI mogą zintegrować się z chromosomem bakterii, ale badacze sprawdzili, czy ten krok jest rzeczywiście niezbędny do zabicia. Stworzyli wersję, która nie mogła już integrować się, i wykazali, że o ile cząstka była prawidłowo wytworzona w szczepie źródłowym, była równie śmiercionośna dla S. aureus jak oryginał. Oznacza to, że system CRISPR może być wyrażony bezpośrednio z przychodzącego kolistego DNA, wykonać swoje zadanie, a następnie zostać utracony w miarę śmierci komórki. To działanie bez integracji dodatkowo zmniejsza szanse niezamierzonego transferu genów i odróżnia te cząstki od klasycznej terapii fagowej, która polega na replikacji wirusa i lizie komórek, by się rozprzestrzenić.
Z płytki Petriego do zakażonych gruczołów mlekowych
Ponieważ szczepy produkujące Bap są powszechne w mastitis krów, zespół przetestował swój najlepiej działający konstrukt, nazwany ePICIrsaE, w modelu myszy odwzorowującym zakażenie wymienia. W mleku i w hodowlach laboratoryjnych biofilmy bogate w Bap wyraźnie osłabiały aktywność ePICI. A jednak w gruczole mlekowym wielokrotne dawki ePICIrsaE ostro zmniejszyły liczbę bakterii dla wszystkich testowanych szczepów, w tym tych produkujących Bap. Jego skuteczność była porównywalna z wankomycyną, silnym antybiotykiem ostatniej linii. Wyniki sugerują, że warunki w żywej tkance — takie jak niższa produkcja Bap, obecność wolno pływających bakterii lub pomocnych składników w mleku — pozwalają zaprojektowanym cząstkom działać znacznie lepiej niż w statycznych biofilmach laboratoryjnych.
Co to może znaczyć dla gospodarstw i nie tylko
Badanie pokazuje, że niereplikujące się, zapakowane w osłonki fagowe systemy CRISPR mogą selektywnie eliminować S. aureus w trudnym zakażeniu związanym z biofilmem, nie rozprzestrzeniając się samodzielnie ani nie powodując jednoczesnego pęknięcia ogromnej liczby komórek. Choć potrzebne są wysokie dawki cząstek, a skalowanie od myszy do krów będzie wyzwaniem, te cząstki oferują obiecującą, kontrolowalną alternatywę dla antybiotyków w leczeniu lokalnych zakażeń, takich jak mastitis. W szerszym ujęciu praca podkreśla, że terapie, które wyglądają na nieskuteczne w prostych testach laboratoryjnych, mogą odnieść sukces w złożonym środowisku żywego organizmu, i otwiera drogę do bibliotek dostosowanych ePICI skierowanych przeciw różnym bakteriom, osłonkom wirusowym i sekwencjom prowadzącym.
Cytowanie: Garmendia-Antoñana, N., Dorado-Morales, P., Gil, C. et al. Targeted elimination of Staphylococcus aureus mastitis infections with synthetic phage-based CRISPR-Cas delivery systems. npj Biofilms Microbiomes 12, 67 (2026). https://doi.org/10.1038/s41522-026-00931-x
Słowa kluczowe: mastitis bydła, Staphylococcus aureus, terapia CRISPR, leczenie oparte na fagach, zakażenia biofilmowe