Clear Sky Science · pl
Szlak regulacyjny ppGpp–HpaR1–gum modyfikuje produkcję egzopolisacharydów u Xanthomonas campestris pv. campestris
Dlaczego „lepkie” bakterie mają znaczenie dla upraw
Wiele bakterii wywołujących choroby przetrwa i rozprzestrzenia się, otulając się śluzowymi powłokami cukrowymi, znanymi jako biofilmy. W uprawach warzywnych, takich jak kapusta czy brokuły, te powłoki mogą zatykać naczynia wodne roślin, powodując znaną „czarną zgniliznę” i poważne straty w plonach. W tym badaniu zajrzano do wnętrza jednej z takich bakterii, Xanthomonas campestris, aby pokazać, jak wewnętrzny system alarmowy reguluje produkcję jej cukrowej osłony. Zrozumienie tego ukrytego obwodu regulacyjnego może pomóc naukowcom opracować lepsze sposoby ochrony upraw lub nawet wykorzystać te cukry jako surowiec do przydatnych materiałów.
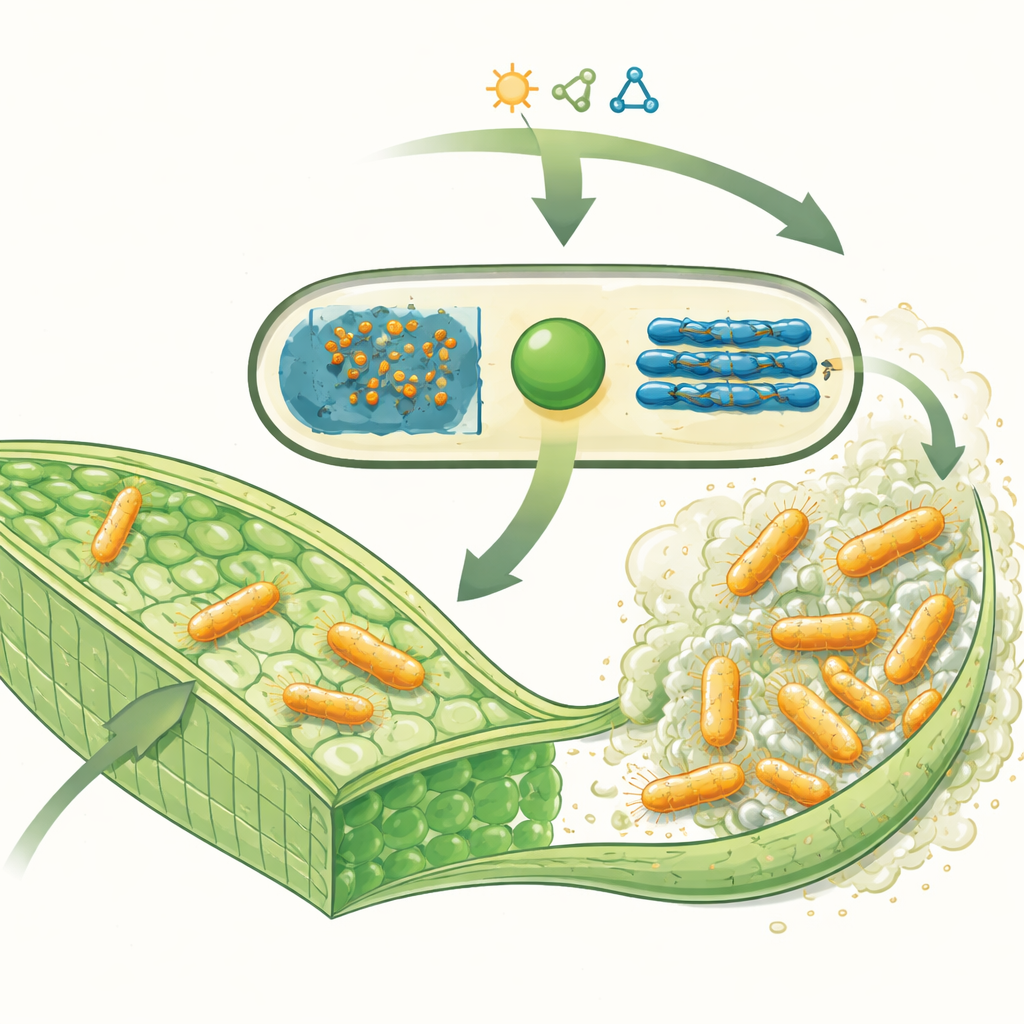
Patogen roślin i jego cukrowa zbroja
Xanthomonas campestris wnika do wiązek przewodzących warzyw kapustnych — roślin takich jak kapusta, kalafior czy gorczyca — i produkuje ogromne ilości lepkiej substancji zwanej gumą ksantanową. Materiał ten składa się z długich łańcuchów jednostek cukrowych i stanowi główną część biofilmu, który pomaga bakteriom przyczepiać się do tkanek roślinnych, opierać się obronie roślin i przetrwać w niesprzyjających warunkach. W roślinie te grube warstwy cukru mogą blokować przepływ wody, prowadząc do obumarcia tkanek i charakterystycznych, V‑kształtnych nekroz liści obserwowanych przy czarnej zgniliźnie. Co ciekawe, ta sama guma ksantanowa jest szeroko stosowana jako zagęstnik w żywności i innych produktach, przez co bakteryjny cukier jest jednocześnie rolniczym „złoczyńcą” i przemysłowym zasobem.
Wewnętrzny alarm kształtujący zachowanie bakterii
W wielu bakteriach drobnocząsteczkowy sygnał zwany ppGpp działa jak alarm awaryjny. Gdy brakuje składników odżywczych lub występuje inny stres, poziom ppGpp wzrasta i uruchamia szeroką „odpowiedź stringentną”, która przekształca wzrost, metabolizm i strategie przetrwania. Poprzednie prace wykazały, że ppGpp może sprzyjać tworzeniu biofilmów u kilku gatunków, a usunięcie go u Xanthomonas osłabia zdolność bakterii do tworzenia biofilmów i wywoływania choroby. Nadal nie było jednak jasne, w jaki sposób ta mała cząsteczka łączy się z maszynerią budującą grubą powłokę egzopolisacharydową (EPS) u tego konkretnego patogena roślin.
Śledząc drogę od sygnału do cukru
Naukowcy porównali bakterie dzikiego typu z mutantami, które nie potrafią wytwarzać ppGpp. Na pożywkach bogatych w cukry mutanci pozbawieni ppGpp tworzyli mniejsze, mniej śluzowate kolonie, a bezpośrednie pomiary wykazały, że produkowali znacznie mniej EPS. Jednak profilowanie chemiczne metodą spektroskopii w podczerwieni i obrazowanie mikroskopem elektronowym ujawniły, że podstawowy skład i wyższa struktura EPS pozostały takie same: mutanci po prostu wytwarzali jej mniej. Uwagę skierowano na klaster genów „gum”, grupę genów kodujących enzymy składające gumo ksantanową. Na podstawie pomiarów ekspresji genów i sekwencjonowania RNA zespół odkrył, że niemal wszystkie geny gum były obniżone w komórkach pozbawionych ppGpp, co wskazuje, że ppGpp działa powyżej tego klastra w hierarchii regulacyjnej.
Kluczowy pośrednik: przełącznik HpaR1
Pomiędzy alarmem ppGpp a genami gum znajduje się białko regulatorowe zwane HpaR1 — czynnik transkrypcyjny, który wiąże DNA i wzmacnia aktywność genów gum. Badanie wykazało, że ppGpp działa na dwóch poziomach. Po pierwsze, komórki pozbawione ppGpp wykazywały obniżoną aktywność genu hpaR1, co oznaczało mniej dostępnego białka HpaR1. Po drugie, w oczyszczonych testach in vitro dodanie ppGpp bezpośrednio wzmacniało przyczepność HpaR1 do regionów DNA kontrolujących geny gum, a nawet do jego własnego regionu kontrolnego. Przy umiarkowanych poziomach ppGpp to wiązanie wyraźnie się zwiększało, choć przy bardzo wysokich poziomach efekt ten częściowo słabł, co sugeruje precyzyjnie wyregulowaną równowagę. Gdy naukowcy sztucznie zwiększyli poziom HpaR1, produkcja EPS wzrosła ponownie — nawet u bakterii pozbawionych ppGpp — potwierdzając, że HpaR1 jest kluczowym pośrednikiem między sygnałem alarmowym a maszynerią wytwarzającą cukry.
Co ten obwód kontrolny oznacza dla upraw i nie tylko
Mówiąc prościej, praca ta odkrywa trzyetapowy przekaźnik wewnątrz patogena roślin: wewnętrzna cząsteczka alarmowa (ppGpp) zwiększa i wzmacnia działanie przełącznika wiążącego DNA (HpaR1), który z kolei zwiększa aktywność fabryki produkującej cukry (geny gum), prowadząc do grubszego ochronnego śluzowego płaszcza wokół bakterii. Mapując szczegółowo szlak ppGpp–HpaR1–gum, badanie wyjaśnia, jak sygnały środowiskowego stresu mogą być przekształcane w zmiany produkcji macierzy biofilmu. Dla rolników i naukowców zajmujących się roślinami te wnioski sugerują nowe cele do zakłócania zbroi bakterii i ograniczania szkód powodowanych czarną zgnilizną. Dla mikrobiologów szerzej, wyniki dodają ważny element do układanki dotyczącej tego, jak uniwersalne sygnały stresowe kontrolują formowanie złożonych wspólnot mikrobiologicznych.
Cytowanie: Bai, K., Xu, X., Yu, C. et al. The ppGpp-HpaR1-gum regulatory pathway modulates exopolysaccharides production in Xanthomonas campestris pv. campestris. npj Biofilms Microbiomes 12, 60 (2026). https://doi.org/10.1038/s41522-026-00926-8
Słowa kluczowe: bakteryjne biofilmy, patogeny roślin, guma ksantanowa, sygnalizacja stresowa, egzopolisacharydy