Clear Sky Science · pl
Charakterystyka metabolizmu żywych bakterii w czasie rzeczywistym i o wysokiej rozdzielczości za pomocą bezznacznikowego optycznego obrazowania metabolicznego
Obserwowanie reakcji zarazków w czasie rzeczywistym
Bakterie są wszędzie na nas i w nas, cicho wpływając na nasze zdrowie. Pomagają trawić pokarm, chronią skórę, a czasami wywołują uporczywe zakażenia odporne na antybiotyki. W tym badaniu przedstawiono metodę pozwalającą obserwować żywe bakterie reagujące na stres i leki w czasie rzeczywistym, na poziomie pojedynczych komórek, bez użycia barwników czy znaczników. Taka możliwość może w przyszłości pomóc lekarzom szybciej dobrać odpowiednie leczenie i pozwolić naukowcom zrozumieć, dlaczego niektóre infekcje są trudne do wyleczenia.
Światło jako okno do życia bakterii
Zamiast dodawać barwniki czy genetyczne znaczniki, badacze korzystają z faktu, że bakterie naturalnie emitują bardzo słabe światło, gdy pewne cząsteczki w ich wnętrzu są wzbudzane światłem laserowym. Dwie z tych cząsteczek, znane jako NAD(P)H i FAD, odgrywają kluczową rolę w przekształcaniu pokarmu w energię. Dzięki szybkiemu, wysokorozdzielczemu mikroskopowi laserowemu zespół może mierzyć zarówno jasność, jak i drobne opóźnienie tego świecenia, ujawniając, jak aktywny jest metabolizm komórki. Ponieważ metoda jest bezznacznikowa i niedestrukcyjna, te same żywe bakterie można śledzić przez sekundy i minuty, gdy zmienia się ich środowisko. 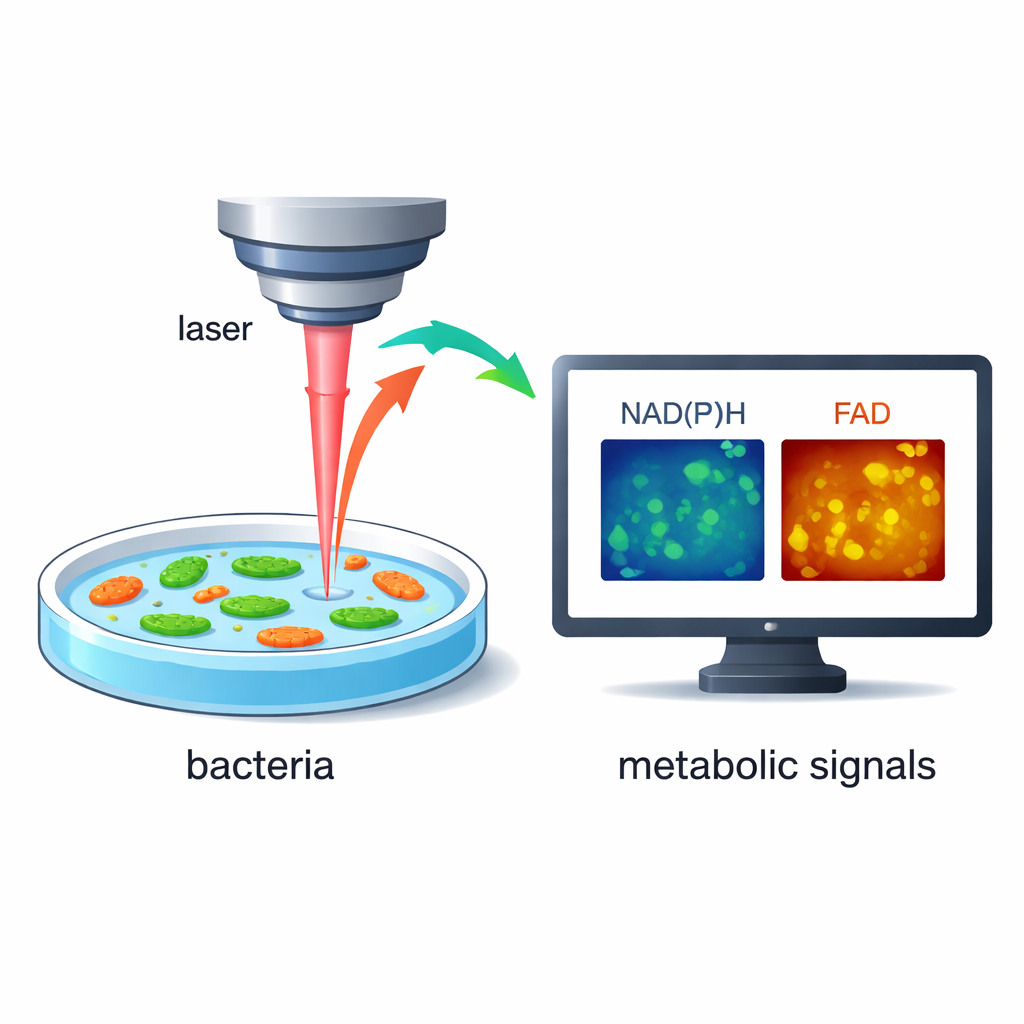
Widzenie różnic między pojedynczymi bakteriami
Większość standardowych testów laboratoryjnych łączy miliony bakterii i podaje tylko wartość średnią. Autorzy pokazują, że ich metoda obrazowania potrafi wyodrębnić pojedyncze komórki Staphylococcus aureus w hodowli płynnej i analizować każdą z nich osobno, nawet przy wysokim zagęszczeniu. Gdy porównali dwie kolonie S. aureus hodowane w tych samych warunkach, jeden kluczowy sygnał (pochodzący od FAD) różnił się między koloniami, a w każdej kolonii występowało rozproszenie wartości. Oznacza to, że nawet genetycznie podobne bakterie w tej samej probówce mogą znajdować się w bardzo różnych stanach metabolicznych — ukryta różnorodność, której standardowe testy zbiorcze mogą nie wykryć, a która może mieć znaczenie dla odpowiedzi zakażeń na leczenie.
Obserwowanie działania antybiotyków w ciągu sekund
Zespół następnie śledził pojedyncze komórki S. aureus podczas narażania ich na kilka środków antybakteryjnych, w tym powszechne antybiotyki i wybielacz domowy. Korzystając z szybkiego układu obrazowania, zarejestrowali zmiany od chwili zetknięcia roztworu leku z komórkami przez następne 30 minut. Silne środki powodowały spadek sygnałów NAD(P)H i wzrost sygnałów FAD, często w ciągu sekund, co odzwierciedla zahamowanie produkcji energii i przesunięcie w kierunku bardziej utlenionego stanu wewnątrz komórki. Dokładne tempo i wzorzec tych zmian zależały od typu i dawki leku: na przykład antybiotyki blokujące syntezę białek oraz te atakujące ścianę komórkową wywoływały krótkotrwały spadek i częściową regenerację, podczas gdy wybielacz powodował ostry, trwały skok. Te charakterystyczne „świetlne sygnatury” sugerują, że technika może wykrywać nie tylko, czy komórki są zestresowane lub umierają, ale także w jaki sposób są uszkadzane. 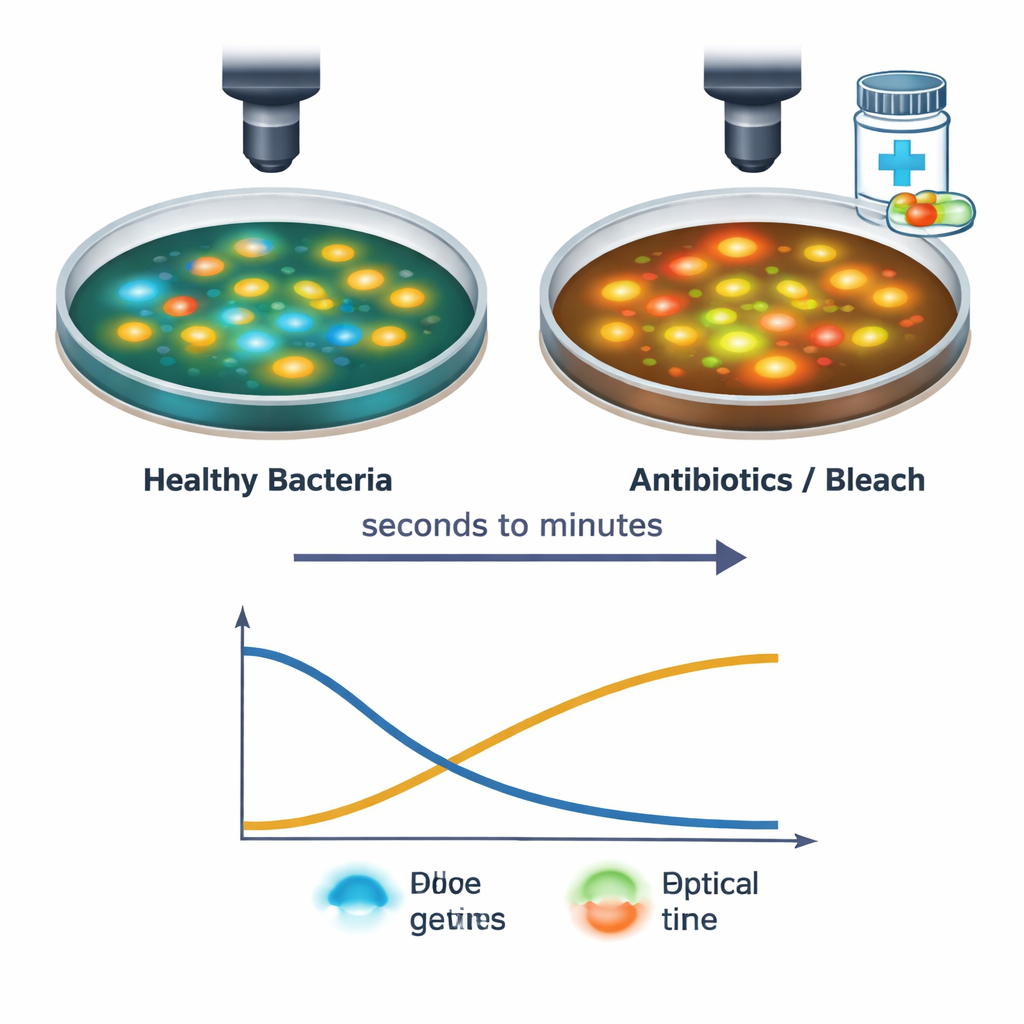
Zaglądanie w ukryty świat biofilmów
Bakterie rzadko żyją samotnie w naturze; zamiast tego tworzą śluzowate, ochronne społeczności zwane biofilmami na powierzchniach od implantów medycznych po zęby. W tych gęstych warstwach niektóre komórki mogą być bardzo aktywne, podczas gdy inne pozostają uśpione — mieszanka, która pomaga społeczności przetrwać działanie antybiotyków. Korzystając z dużych zszywanych obrazów, badacze zmapowali krajobraz metaboliczny wewnątrz biofilmów S. aureus i porównali go z komórkami swobodnie pływającymi. Odkryli jasne, metabolicznie aktywne kieszonki otoczone obszarami o niższej aktywności i wykazali, że w kilku gatunkach bakterii komórki w biofilmach miały tendencję do bardziej utlenionego profilu metabolicznego niż ich odpowiedniki wolno żyjące. Dodatkowe sygnały optyczne sugerowały obecność większej ilości lipidów i białek, co jest zgodne ze spoiwem utrzymującym biofilmy razem.
Dlaczego to ma znaczenie dla przyszłej medycyny
Łącznie wyniki pokazują, że bezznacznikowe optyczne obrazowanie metaboliczne może dostarczać szybkich, szczegółowych i nieinwazyjnych migawków tego, jak bakterie żyją, adaptują się i umierają. Dla czytelnika popularnonaukowego kluczowy przekaz jest taki, że naukowcy mogą teraz „podsłuchiwać” zużycie energii przez bakterie w czasie rzeczywistym, nie zakłócając komórek, używając jedynie odpowiednio dostrojonego światła. W dłuższej perspektywie tego rodzaju technologia mogłaby pomóc w identyfikacji trudnych do hodowli bakterii, wykrywaniu kieszeni komórek tolerujących leki w biofilmach lub szybkim testowaniu, jak zakażenie pacjenta reaguje na różne antybiotyki. To mogłoby wspierać szybsze, bardziej spersonalizowane leczenie i pogłębiać nasze rozumienie niewidzialnych światów mikroorganizmów, które codziennie wpływają na nasze zdrowie.
Cytowanie: Sorrells, J.E., Yang, L., Iyer, R.R. et al. Real-time, high-resolution metabolic characterization of live bacteria using label-free optical metabolic imaging. npj Biofilms Microbiomes 12, 55 (2026). https://doi.org/10.1038/s41522-026-00920-0
Słowa kluczowe: metabolizm bakterii, obrazowanie optyczne, biofilmy, odpowiedź na antybiotyki, mikrobiom