Clear Sky Science · pl
Antybiotykoterapia z dodatkiem enzymów redukuje biofilm do poziomu niewykrywalnego w modelu zakażenia związanego z implantem
Dlaczego uporczywe zakażenia implantów mają znaczenie
Endoprotezy biodra i kolana zmieniają życie, ale gdy bakterie skolonizują metalowe implanty, mogą tworzyć śliskie społeczności zwane biofilmami. Biofilmy działają jak opancerzone miasta, które chronią drobnoustroje zarówno przed układem odpornościowym, jak i antybiotykami, prowadząc do bolesnych, przewlekłych zakażeń trudnych do wyleczenia. W tym badaniu przedstawiono nową, dwutorową terapię, która najpierw pomaga rozmontować obronę biofilmu, a następnie miejscowo dostarcza wysokie dawki antybiotyków — podejście, które w przyszłości może pozwolić zachować więcej implantów zamiast je wymieniać.
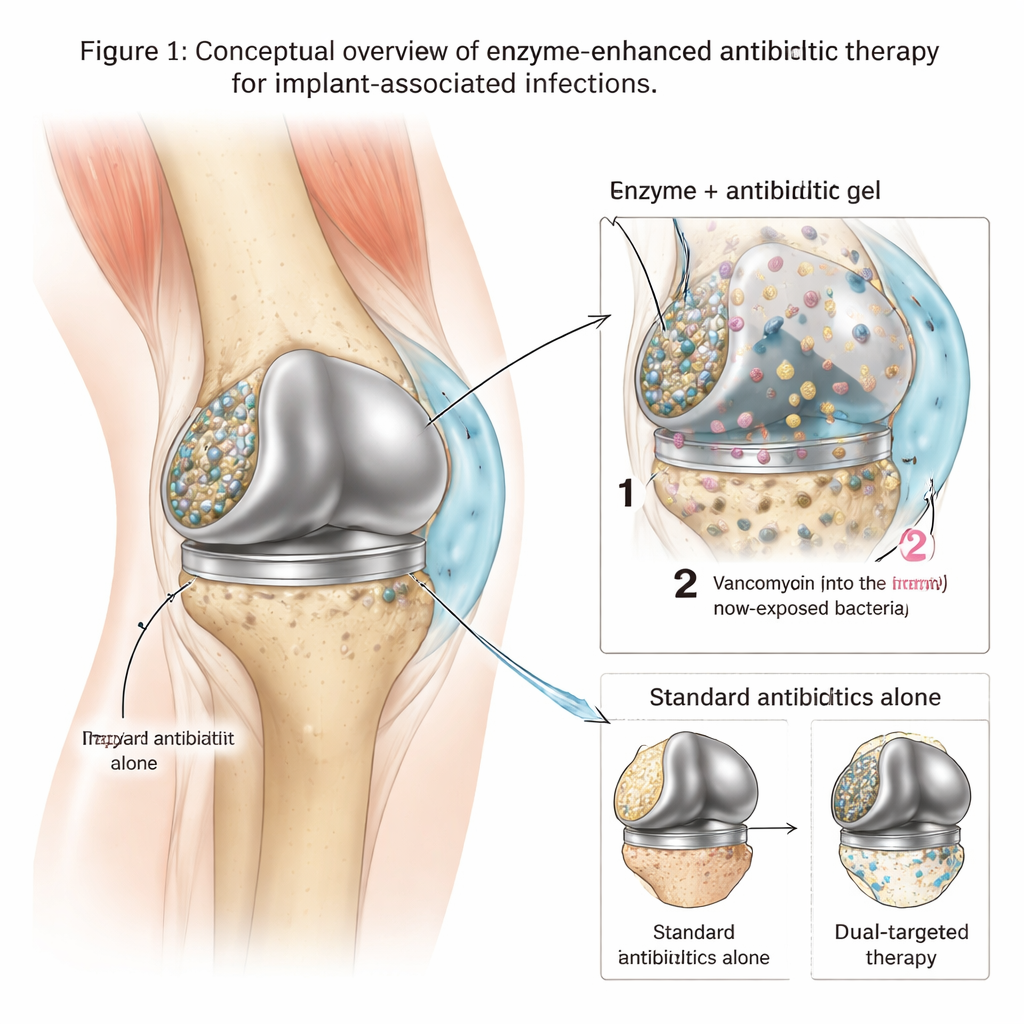
Ukryte twierdze na metalowych implantach
Gdy bakterie, takie jak metycylinooporny Staphylococcus aureus (MRSA), przyczepią się do sztucznego stawu, szybko tworzą lepką matrycę z DNA, cukrów i innych cząsteczek na powierzchni metalu. W obrębie tej osłoniętej warstwy bakterie rosną wolniej, zmieniają swoje zachowanie i mogą tolerować stężenia antybiotyków setki, a nawet tysiące razy wyższe niż te zabijające wolno pływające drobnoustroje. W efekcie standardowe terapie — nawet silne leki, takie jak wankomycyna — często nie usuwają zakażenia całkowicie, zmuszając pacjentów do kolejnych operacji lub całkowitej wymiany implantu. Lekarze potrzebują narzędzi, które nie tylko zabijają bakterie, lecz także rozbijają ich ochronną twierdzę, tak by leki mogły do nich dotrzeć.
Sprytny żel dostarczający enzymy i antybiotyki
Naukowcy zaprojektowali leczenie miejscowe oparte na termoczułym hydrożelu z polimeru poloksamer 407. Żel jest ciekły w niskiej temperaturze, co ułatwia wstrzyknięcie wokół implantu, ale przy ciepłocie ciała szybko przechodzi w miękkie ciało stałe, dzięki czemu utrzymuje się na miejscu. Do tego żelu zespół załadował dwa kluczowe składniki: silny antybiotyk (wankomycynę) oraz koktajl trzech enzymów rozcinających główne składniki matrycy biofilmu. W testach laboratoryjnych dostrojono uwalnianie tak, by enzymy były uwalniane najpierw — poluzowując i przerzedzając biofilm — podczas gdy wankomycyna uwalniana była wolniej przez kilka dni, utrzymując bardzo wysokie lokalne stężenia leku dokładnie tam, gdzie żyją bakterie.
Od naczyń laboratoryjnych po świnki morskie
Aby sprawdzić skuteczność strategii, badacze najpierw przetestowali ją na biofilmach wyhodowanych na kawałkach tytanu w laboratorium, a potem w modelu świnki morskiej imitującym zakażone implanty. In vitro dwie aplikacje żelu z enzymami i antybiotykiem w odstępie 48 godzin zmniejszyły liczbę żywych bakterii na powierzchniach metalowych o ponad 100 000 razy i niemal całkowicie zredukowały masę biofilmu. W badaniach na zwierzętach naukowcy chirurgicznie umieścili perforowane klatki z kuleczkami tytanowymi pod skórą, zakażali je MRSA, a następnie leczyl różnymi kombinacjami antybiotyków ogólnoustrojowych i żeli miejscowych. Najskuteczniejszy schemat łączył: (1) miejscowy żel zawierający zarówno enzymy, jak i wankomycynę, podany dwukrotnie, oraz (2) leczenie ogólnoustrojowe wankomycyną plus drugi antybiotyk, ryfampicyną, który szczególnie dobrze penetruje biofilmy.
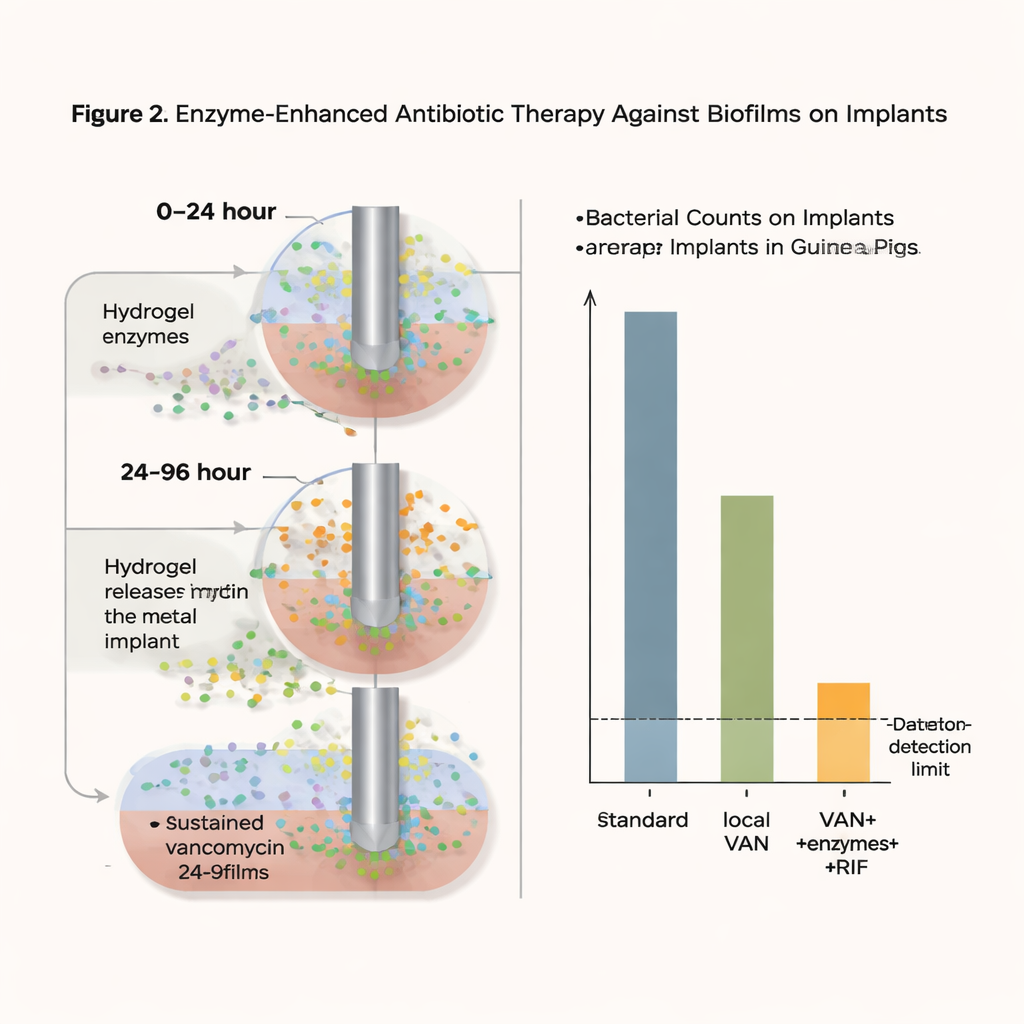
Co osiągnięto nowym podejściem
Dzięki intensywnej, ale zlokalizowanej strategii liczba bakterii na materiale implantacyjnym spadła do granicy wykrywalności — skutecznie „brak odzyskiwalnych bakterii” w tym modelu — w 75 procentach leczonych klatek jeden dzień po zakończeniu terapii, a w 37,5 procentach nawet pięć dni później. Co ważne, nie zaobserwowano wzrostu oporności na wankomycynę, a wysokie lokalne stężenia wankomycyny wydawały się zapobiegać pojawieniu się szczepów opornych na ryfampicynę. Testy bezpieczeństwa przy użyciu hodowanych komórek i odtworzonego modelu ludzkiej skóry nie wykazały oznak toksyczności ani podrażnień wywołanych formulacjami żelu. Choć w niektórych przypadkach odnotowano słaby nawrót bakterii, a okres leczenia był krótszy niż zazwyczaj stosowany u pacjentów, wyniki pokazują, że połączenie enzymów rozbijających biofilm z utrzymującym się miejscowym podawaniem antybiotyku może drastycznie zmniejszyć wyjątkowo uporczywe zakażenia.
Co to może znaczyć dla pacjentów
Dla osób z zakażeniami związanymi z implantami praca ta wskazuje na przyszłość, w której chirurdzy mogliby wstrzykiwać sprytny żel wokół zakażonego stawu, zamiast natychmiast usuwać lub wymieniać sprzęt. Poprzez najpierw osłabienie osłony biofilmu, a następnie zalanie obszaru wysokimi, utrzymującymi się dawkami antybiotyków — wspieranymi leczeniem ogólnoustrojowym — ta dwuetapowa strategia ma na celu zredukowanie liczby bakterii do poziomów niewykrywalnych i zmniejszenie ryzyka powstania oporności. Chociaż potrzebne są dalsze badania, dłuższe schematy leczenia i próby kliniczne u ludzi, podejście daje obiecujący wzorzec pozwalający przemienić niektóre z najbardziej uporczywych zakażeń ortopedycznych w bardziej opanowalne, a potencjalnie uleczalne problemy.
Cytowanie: Buzisa Mbuku, R., Poilvache, H., Maigret, L. et al. Enzymes-enhanced antibiotic therapy reduces biofilms to undetectable levels in an implant-associated infection model. npj Biofilms Microbiomes 12, 44 (2026). https://doi.org/10.1038/s41522-026-00910-2
Słowa kluczowe: zakażenie biofilmowe, implanty ortopedyczne, wankomycyna, terapia enzymatyczna, ryfampicyna