Clear Sky Science · pl
Teoretyczne badanie protokołów leczenia infekcji endoprotez kombinacjami antybiotyków i bakteriofagów
Dlaczego infekcje implantów stawowych mają znaczenie
Protezy biodra i kolana zmieniły życie milionów ludzi, przywracając możliwość chodzenia bez bólu. Gdy jednak bakterie zasiedlą te sztuczne stawy, mogą tworzyć śliskie społeczności zwane biofilmami, które silnie przylegają do powierzchni metalu i tworzyw sztucznych. Gdy biofilm się uformuje, zwykłe dawki antybiotyków i mechanizmy obronne organizmu często zawodzą w jego zwalczaniu, co niekiedy zmusza pacjentów do kolejnych operacji. Niniejsze badanie pyta, czy dodanie wirusów atakujących konkretne bakterie — zwanych bakteriofagami, lub fagami — do standardowej terapii antybiotykowej może dać lepszy sposób leczenia tych uporczywych infekcji.
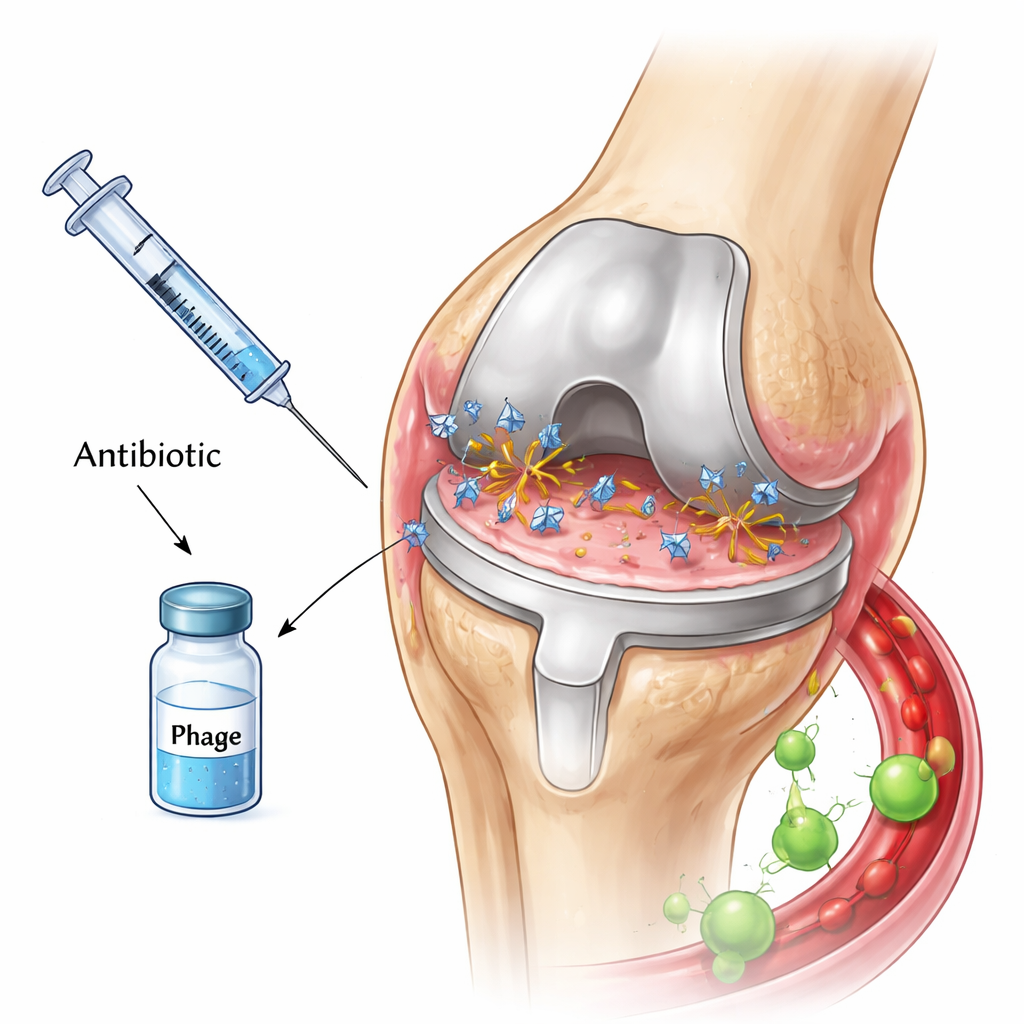
Maleńkie wirusy polujące na bakterie
Fagi są naturalnymi drapieżnikami bakterii. Przyczepiają się do komórki bakteryjnej, wstrzykują swój materiał genetyczny, przekształcają komórkę w fabrykę wirusów, a na końcu ją rozrywają, uwalniając nową falę fagów. Niektóre fagii niosą też enzymy mogące rozkładać lepką substancję otaczającą biofilmy, potencjalnie odsłaniając warstwy ochronne, które chronią bakterie przed lekami. Z tych powodów wielu badaczy liczyło, że połączenie fagów z antybiotykami mogłoby stanowić silne, skoordynowane uderzenie przeciw infekcjom endoprotez, zwłaszcza gdy bakterie stają się oporne na leki.
Budowanie infekcji w komputerze
Zamiast od razu przechodzić do eksperymentów na zwierzętach czy badań klinicznych, autorzy najpierw stworzyli szczegółowy model matematyczny i komputerowy infekcji endoprotezy. Ich wirtualny system miał dwie główne strefy: bakterie unoszące się swobodnie w płynach ustrojowych oraz bakterie osadzone w biofilmie na powierzchni implantu. Model śledził także komórki układu odpornościowego, substancje odżywcze niezbędne do wzrostu bakterii, antybiotyki i fagi, wszystkie przemieszczające się do wnętrza i na zewnątrz stawu. Zmieniając warunki takie jak dawka leków, czas podania i obecność bakterii opornych na antybiotyki, mogli badać wiele strategii leczenia, które w realnych pacjentach byłyby trudne, czasochłonne lub kosztowne do przetestowania.
Kiedy leki działają solo i razem
Symulacje wykazały, że ani układ odpornościowy, ani same antybiotyki nie radzą sobie łatwo z oczyszczeniem infekcji biofilmowych. Antybiotyki silnie zmniejszały liczbę bakterii unoszących się swobodnie, ale ledwie wpływały na populację w biofilmie. Fagi potrafiły początkowo skuteczniej kontrolować infekcję, lecz wprowadzały cykle boom-and-bust: gdy fagi zabijały bakterie, ich „ofiary” stawały się zbyt nieliczne, co powodowało spadek liczby fagów i pozwalało bakteriom odbudować populację. Gdy antybiotyki i fagi podawano jednocześnie, wynik zwykle dominował antybiotyk, a dodanie fagów często niewiele wnosiło ponad to, co sam antybiotyk mógł osiągnąć.
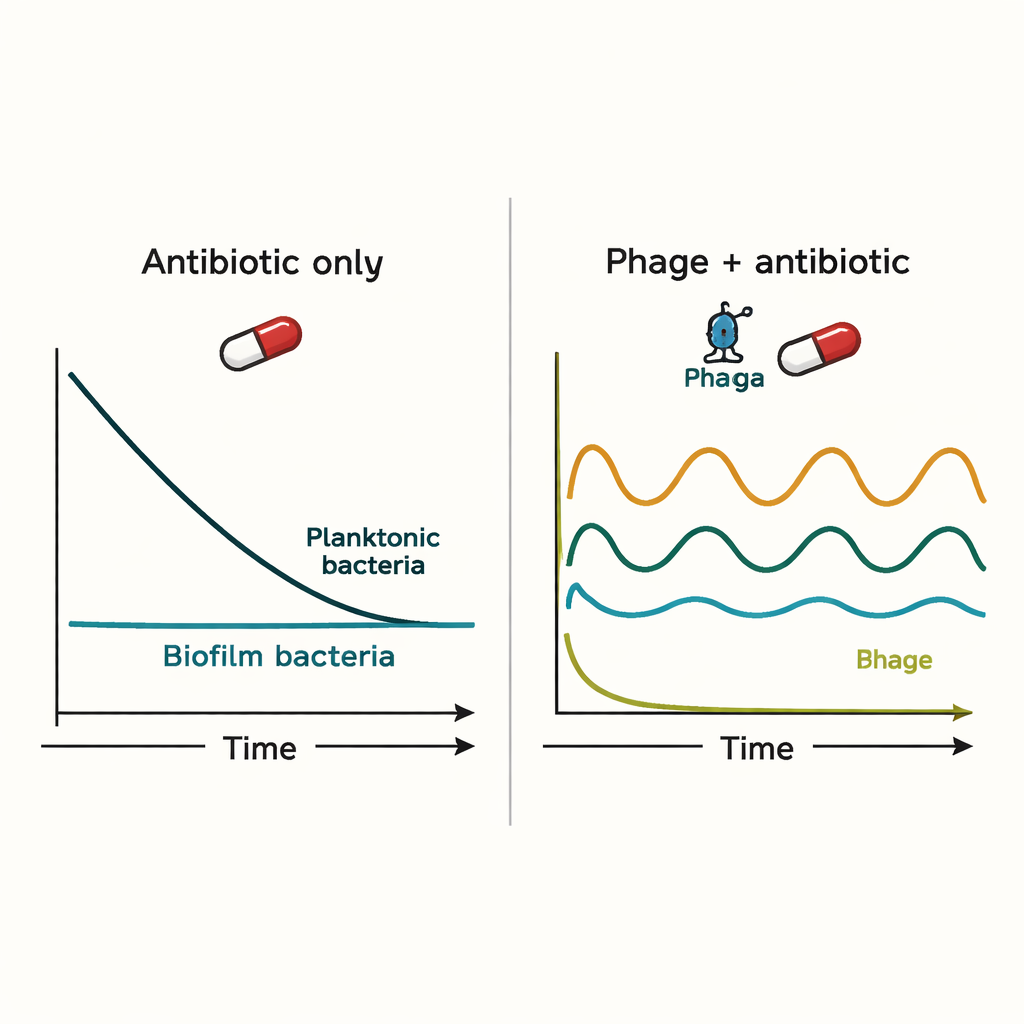
Szczególna rola czasu podania i oporności
Model okazał się bardziej obiecujący po uwzględnieniu bakterii opornych na antybiotyki. Fagi potrafiły atakować te oporne komórki, czasem usuwając je całkowicie. Jeśli terapię fagową rozpoczęto najpierw, a antybiotyki dodano kilka godzin później, strategia łączona w symulacjach zmniejszała liczbę bakterii unoszących się swobodnie o wiele rzędów wielkości i eliminowała oporne podpopulacje. Nawet wtedy bakterie związane z biofilmem nie były całkowicie usunięte; ich liczebność utrzymywała się na niższym poziomie, którym układ odpornościowy mógłby łatwiej zarządzać. Sugeruje to, że fagi mogą być najcenniejsze nie jako magiczne kule, lecz jako pomocnicy zapobiegający oporności i utrzymujący infekcje pod kontrolą.
Co to oznacza dla pacjentów i lekarzy
Dla osób z zakażoną endoprotezą to opracowanie niesie zarówno ostrzeżenie, jak i nadzieję. Model sugeruje, że samo dodanie fagów do standardowych antybiotyków raczej nie wyleczy głębokich infekcji biofilmowych. Jednak fagi wciąż mogą być przydatnym narzędziem: mogą pomóc wyeliminować bakterie oporne na antybiotyki i zmniejszyć ogólną liczbę drobnoustrojów do poziomu, z którym organizm poradzi sobie lepiej, zwłaszcza jeśli zastosuje się je przed lub starannie zsynchronizuje z antybiotykami. Autorzy podkreślają, że to są przewidywania teoretyczne, a nie dowody kliniczne. Ich główny przekaz jest taki, że potrzebne są przemyślane eksperymenty — kierowane modelami podobnymi do tego — aby odkryć, kiedy terapia fagowa rzeczywiście może poprawić wyniki leczenia pacjentów z infekcjami endoprotez.
Cytowanie: Levin, B.R., Gil-Gil, T., Berryhill, B.A. et al. A theoretical exploration of protocols for treating prosthetic joint infections with combinations of antibiotics and bacteriophage. npj Biofilms Microbiomes 12, 51 (2026). https://doi.org/10.1038/s41522-025-00908-2
Słowa kluczowe: infekcja endoprotezy, biofilm, terapia bakteriofagami, oporność na antybiotyki, modelowanie matematyczne