Clear Sky Science · pl
Etapy formowania kondensatów biomolekularnych w montażu pro-β-karboksosomu
Dlaczego małe fabryki węglowe mają znaczenie
Łańcuchy pokarmowe Ziemi zależą od fotosyntezy, a jednak kluczowy enzym wychwytujący dwutlenek węgla (CO2), Rubisco, jest wolny i łatwo myli się z tlenem. Cyjanobakterie – mikroskopijne mikroby fotosyntetyczne – dawno temu rozwiązały ten problem, budując białkowe „mikrofabryki” zwane karboksosomami, które koncentrują CO2 wokół Rubisco. To badanie rozplątuje sposób, w jaki jeden istotny kompleks adaptorowy, złożony z białek zwanych ApN i CM, samoorganizuje się etapami, aby pomóc w zbudowaniu działającego karboksosomu. Zrozumienie tej choreografii może pokierować wysiłkami nad instalacją podobnych systemów zwiększających CO2 w roślinach uprawnych i podnieść plony.
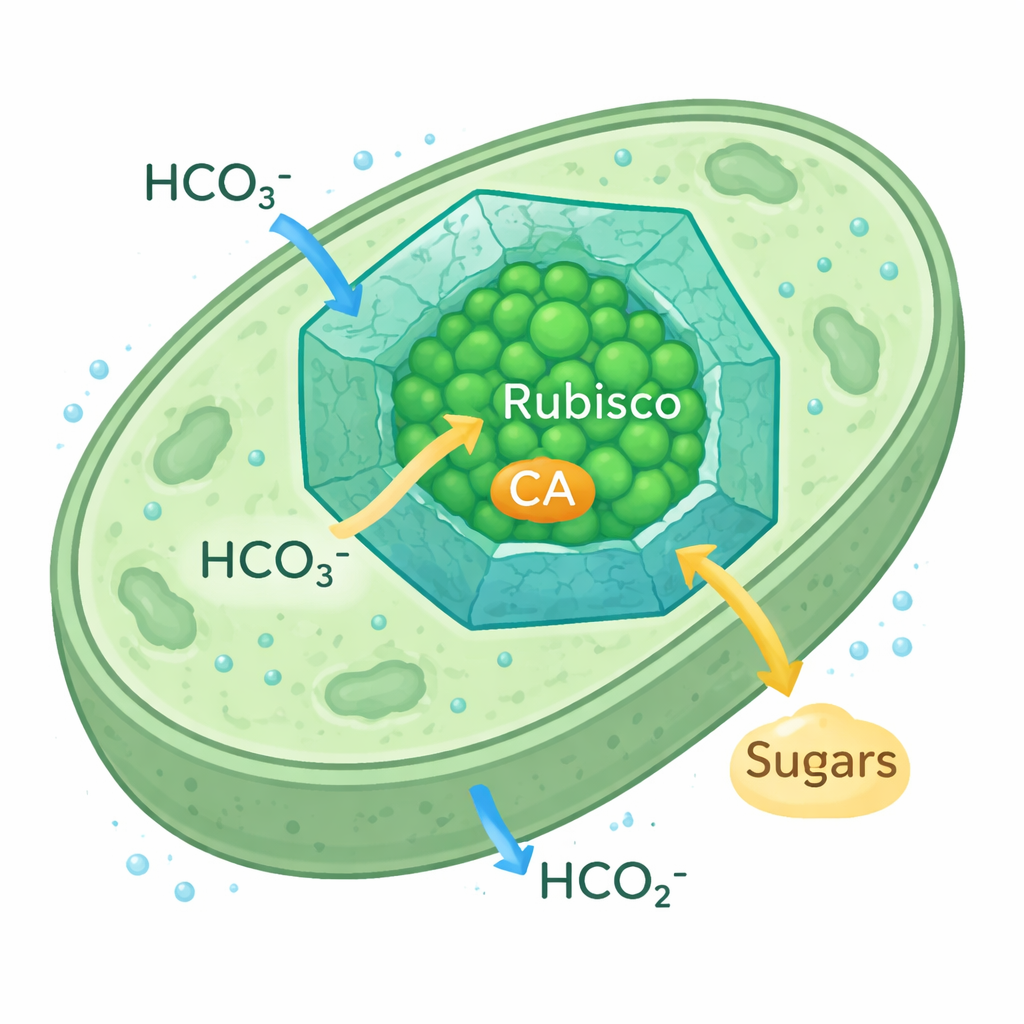
Jak mikroby wzmacniają wychwyt węgla
Cyjanobakteryjne karboksosomy to maleńkie, ikozaedryczne przegrody białkowe wewnątrz komórki. Ich białkowa powłoka przepuszcza jony wodorowęglanowe, a jednocześnie spowalnia ucieczkę CO2, tworząc bogatą w CO2 bańkę wokół Rubisco i jego partnera enzymatycznego, anhydrazy węglanowej (CA), która przekształca wodorowęglan w CO2. Ten mechanizm koncentracji CO2 pozwala cyjanobakteriom prosperować nawet wtedy, gdy CO2 w otoczeniu jest rzadki. Ponieważ forma Rubisco używana w tych karboksosomach przypomina roślinne Rubisco, naukowcy uważają je za realistyczny model do przeprojektowania chloroplastów roślinnych w celu skuteczniejszego wychwytu węgla.
Element układanki, który łączy się z powłoką
Zanim utworzy się twarda białkowa powłoka, cyjanobakterie najpierw budują miękki, przypominający kroplę „pro-karboksosom” — kondensat. Wcześniejsze badania wykazały, że szkieletowe białko CM gromadzi Rubisco i CA w tej kropli. Brakowało jednak ogniwa wyjaśniającego, jak adaptor powłoki ApN dołącza do tej struktury i później łączy ją z białkami powłoki. Autorzy odkryli, że gdy ApN jest produkowane samodzielnie, tworzy czterocząsteczkowy kompleks, który ignoruje pozostałe składniki karboksosomu. W tym stanie ApN nie zostaje wciągnięte do kropli z Rubisco, CM i CA, co sugeruje, że podczas rzeczywistego montażu karboksosomu musi występować inna forma ApN.
Współtworzone adaptery i redoksowy przełącznik
Analizując układ genetyczny w cyjanobakteriach, zespół zauważył, że apn znajduje się bezpośrednio za genem cm w tym samym operonie, więc oba białka są zwykle produkowane razem. Naśladując to w bakteriach, współwytwarzali ApN i CM z tego samego odcinka DNA. W tych warunkach ApN przestało tworzyć samodzielny tetramer. Zamiast tego trzy podjednostki ApN i jedna podjednostka CM złożyły się w określony czteroczęściowy kompleks adaptorowy oznaczony jako (ApN)3:CM. Ten heterokompleks chętnie wiązał się z Rubisco, CA i CM i mógł dołączać do kondensatów. Modelowanie strukturalne i krio‑elektronowa mikroskopia wykazały, że ApN i CM łączą się przez precyzyjnie dopasowany interfejs „język‑i‑wpust”; gdy kluczowe reszty ApN w tym interfejsie zostały zmutowane, adaptor nie powstawał, a komórki nie potrafiły zbudować prawidłowych karboksosomów.
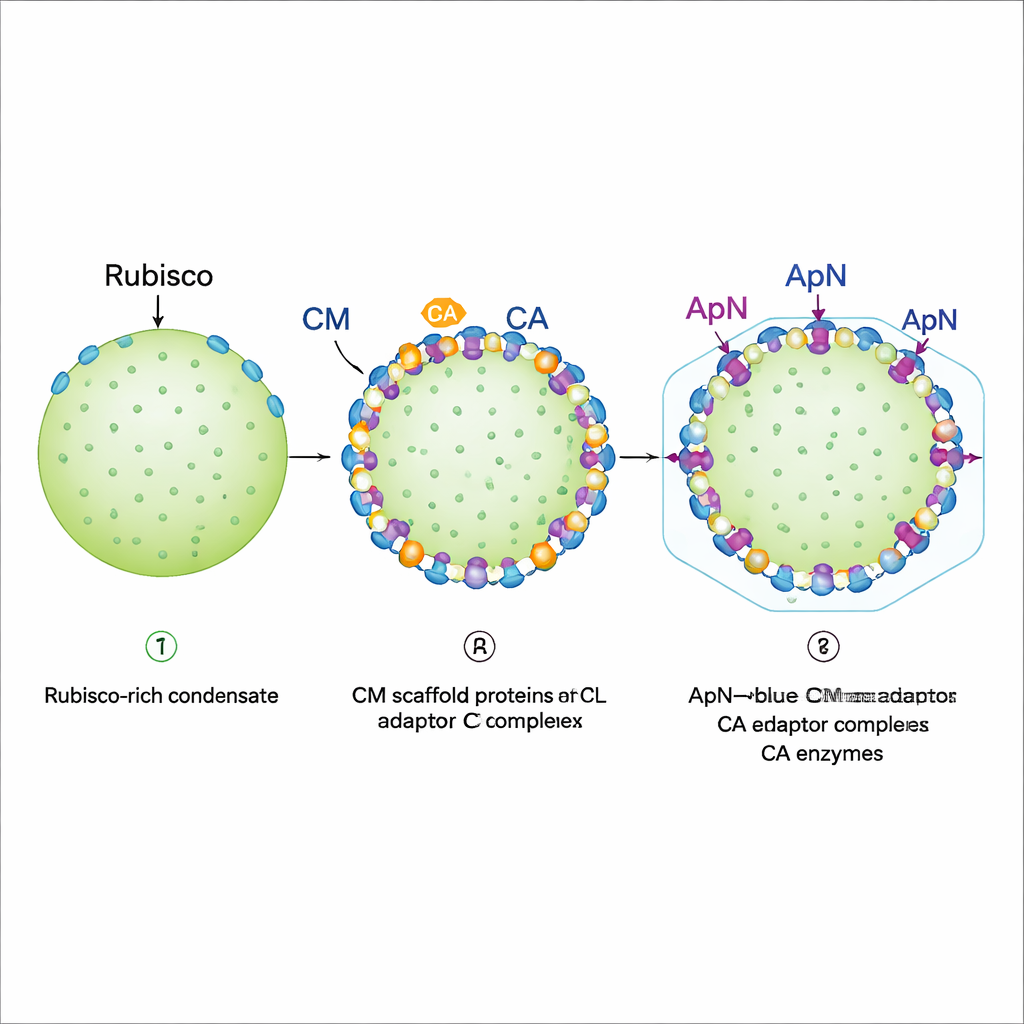
Pozycjonowanie na krawędzi i przygotowanie powłoki
Obrazowanie fluorescencyjne zrekonstytuowanych kropli ujawniło etapowy program składania. Najpierw Rubisco, pełnej długości CM i krótszy wariant CM tworzą gęsty kondensat zachowujący się jak żel: Rubisco jest praktycznie unieruchomione. Następnie dodawane są CA i kompleks (ApN)3:CM. Oba elementy preferencyjnie osiadają przy zewnętrznym obrzeżu istniejącej kropli, pod warunkiem że CA pojawi się przed lub razem z (ApN)3:CM. To lokalizowanie na krawędzi jest kluczowe, ponieważ ogon ApN niesie „peptyd enkapsulacyjny”, który wiąże białka powłoki. Autorzy odkryli także wbudowany redoksowy przełącznik: w miarę jak wnętrze dojrzewającego karboksosomu staje się bardziej utleniające, dwie konserwowane reszty cysteiny w ApN mogą ulec utlenieniu, przesuwając adaptor z tetrameru (ApN)3:CM w kierunku trimera (ApN)2:CM. W żywych komórkach cyjanobakterii zmiany tych cystein spowalniały wzrost i prowadziły do powstawania zbyt dużych, lecz wciąż funkcjonalnych karboksosomów, podkreślając ich rolę w dopracowywaniu dojrzewania.
Wnioski dla budowy lepszych upraw
Dla osoby niespecjalistycznej te molekularne detale mogą brzmieć arcynaukowo, ale sprowadzają się do prostego przesłania: czas i współpraca mają znaczenie. Praca pokazuje, że ApN musi być współwytwarzane z CM, aby uniknąć tworzenia bezużytecznych samodzielnych skupisk i zamiast tego stać się adaptorom, który lokuje się na powierzchni pro-karboksosomu, gotowym do rekrutacji powłoki. Czuły na redoks etap pomaga następnie przeprojektować ten adaptor, gdy przegroda się zamyka i zmienia się jej wewnętrzna chemia. Dla inżynierów roślinnych, którzy chcą przeszczepić cyjanobakteryjne mechanizmy koncentracji CO2 do upraw, badanie podkreśla, że nie wystarczy przenieść pojedynczych części; trzeba również uszanować porządek, proporcje i chemiczne sygnały, które kierują montażem karboksosomu w naturze.
Cytowanie: Zang, K., Hong, X., Nguyen, N.D. et al. Stages of biomolecular condensate formation in pro-β-carboxysome assembly. Nat. Plants 12, 447–464 (2026). https://doi.org/10.1038/s41477-026-02227-6
Słowa kluczowe: montaż karboksosomu, cyjanobakteryjny mechanizm koncentracji CO2, kondensaty Rubisco, kondensaty biomolekularne, syntetyczna fotosynteza