Clear Sky Science · pl
Wielowarstwowe profilowanie molekularne informuje rozpoznanie i terapię ukierunkowaną desmoplastycznego guza z małych okrągłych komórek
Rzadka choroba nowotworowa potrzebująca lepszych rozwiązań
Desmoplastyczny guz z małych okrągłych komórek (DSRCT) to niezwykle rzadki i agresywny nowotwór, który głównie dotyka dzieci, nastolatków i młodych dorosłych. Ze względu na rzadkość i fakt, że pod mikroskopem może przypominać inne guzy, lekarze często mają trudności z prawidłowym rozpoznaniem i doborem skutecznego leczenia. W badaniu zadano proste, lecz istotne pytanie: czy dogłębna analiza guzów DSRCT na wielu poziomach molekularnych — nie tylko DNA, lecz także RNA, wzorców białkowych i chemicznych znaków na DNA — pozwoli zarówno doprecyzować diagnozę, jak i odkryć nowe, bardziej precyzyjne opcje leczenia dla pacjentów, którym skończyły się standardowe terapie?
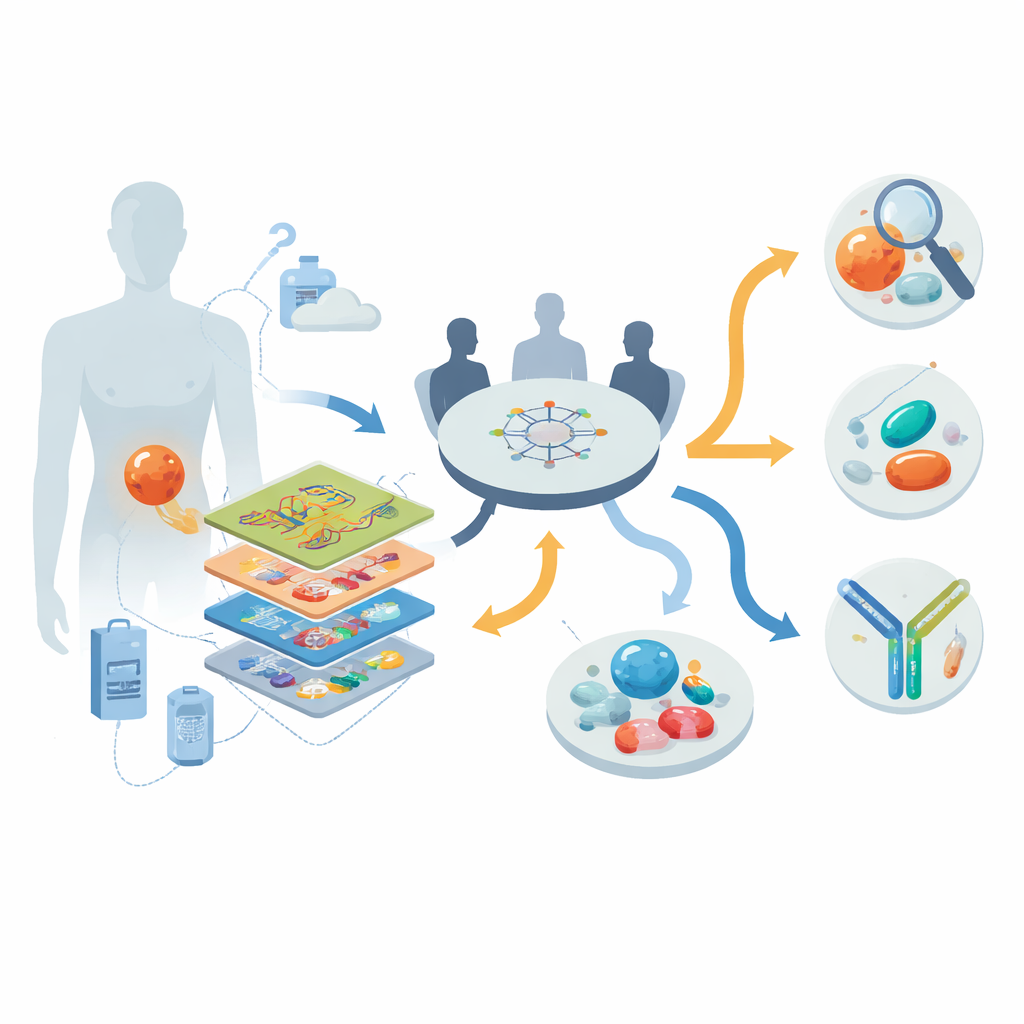
Patrząc do wnętrza guza warstwa po warstwie
Naukowcy pracowali w ramach krajowego programu onkologii precyzyjnej w Niemczech, rekrutując 30 osób z zaawansowanym, przeważnie opornym na leczenie DSRCT w latach 2013–2022. U każdego pacjenta zastosowano zestaw narzędzi „multi-omicznych”: sekwencjonowanie całego genomu lub eksomu do analizy DNA; sekwencjonowanie RNA, aby zobaczyć, które geny są aktywne; profilowanie metylacji DNA w celu uchwycenia epigenetycznych odcisków palców; oraz u dziewięciu pacjentów szczegółowe pomiary białek i fosfoprotein, które pokazują, które szlaki sygnałowe są rzeczywiście aktywne. Wielodyscyplinarny zespół ekspertów następnie przeanalizował te dane razem z historią kliniczną każdego pacjenta, aby przygotować spersonalizowane zalecenia dotyczące wyjaśnienia rozpoznania, leków ukierunkowanych i badań klinicznych.
Poprawianie błędnych rozpoznań i ujawnianie ukrytych celów
Jednym z uderzających odkryć była częstotliwość, z jaką dogłębne profilowanie korygowało pierwotne rozpoznanie. U ośmiu z 30 pacjentów guzy pierwotnie oznaczone jako inne jednostki — takie jak nowotwory o nieznanym pochodzeniu czy niedookreślone mięsaki — zostały przeklasyfikowane jako DSRCT po wykryciu charakterystycznej fuzji genów (EWSR1::WT1) i typowego wzorca metylacji. Jednocześnie DNA tych guzów okazało się stosunkowo „ciche”: było niewiele mutacji i tylko sporadyczne zmiany liczby kopii, więc klasyczne podejście „zmutowany gen = cel terapeutyczny” dawało niewiele możliwości. Najwięcej wskazówek pochodziło zamiast tego z warstw RNA i białek. Porównując aktywność genów w DSRCT z setkami innych mięsaków, zespół wykrył powtarzające się przewyższenie ekspresji kilku cząsteczek powierzchniowych i enzymów sygnałowych, które w praktyce mogłyby być atakowane istniejącymi lub rozwijanymi lekami.
Z sygnałów molekularnych do dopasowanych terapii
Na podstawie tych wzorców zespół ekspertów wydał 107 zaleceń opartych na danych molekularnych dla 28 z 30 pacjentów. Większość rekomendacji dotyczyła leków blokujących kinazy tyrozynowe — kluczowe enzymy napędzające wzrost komórek i tworzenie naczyń — lub nowocześniejszych strategii przyczepiających się do wysoce eksprymowanych białek powierzchniowych. Przykłady obejmowały małocząsteczkowe inhibitory kinaz, takie jak pazopanib; terapię peptydową z promieniowaniem celującą w receptory somatostatynowe; eksperymentalne komórki CAR-T kierowane przeciwko cząsteczce adhezji CLDN6; oraz sprzężone z przeciwciałem leki cytotoksyczne dostarczające toksyny do komórek wyrażających receptor ERBB2 (HER2). Siedemnastu pacjentów uznano za kwalifikujących się do badań klinicznych dopasowanych do biomarkerów, co podkreśla, jak szczegółowe dane molekularne mogą otworzyć drzwi do badań trudnych do uzyskania dla osób z ultra-rzadką chorobą.
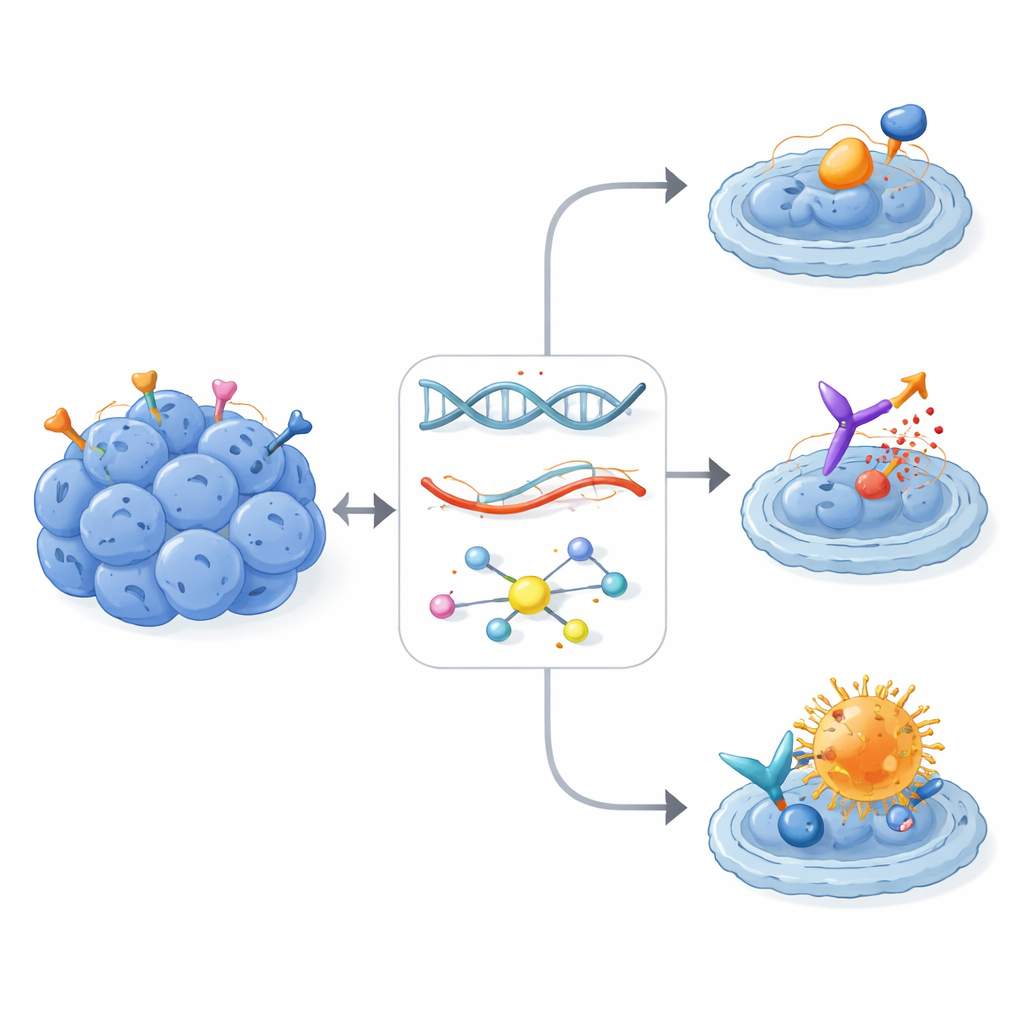
Rzeczywisty wpływ u silnie wcześniej leczonych pacjentów
Ze wszystkich zalecanych terapii spersonalizowanych 16 zostało faktycznie podanych 13 pacjentom, wszystkie kierowane sygnałami na poziomie RNA i czasem doprecyzowane danymi o fosfoproteinach. Mimo że osoby te przeszły już wielokrotnie chemioterapie i leczenie miejscowe, u ośmiu z 13 uzyskano kontrolę choroby — u pięciu częściową regresję guza, a u trzech stabilizację choroby. Wielocelowe inhibitory kinaz tyrozynowych, najczęściej pazopanib, przyniosły istotne i czasem długotrwałe korzyści u kilku pacjentów, zwłaszcza gdy znane cele leku były wyraźnie nadaktywne w guzie. Być może najbardziej godne uwagi były dwa przypadki pacjentów z wysoką ekspresją ERBB2, którzy otrzymali sprzężone z przeciwciałem trastuzumab derukstekan (T-DXd). Oboje doświadczyli przedłużonych odpowiedzi trwających do dwóch lat lub dłużej, mimo że wyczerpali wiele wcześniejszych linii terapii i mimo że receptor ERBB2 nie wykazywał silnego wzorca aktywacji typowego dla klasycznych leków blokujących ERBB2.
Co to oznacza dla pacjentów i przyszłej opieki
Dla osób z DSRCT badanie niesie ostrożnie optymistyczny przekaz. Chociaż ten nowotwór ma niewiele oczywistych mutacji DNA, które można by wykorzystać, analiza wielu warstw molekularnych może zarówno poprawiać błędne rozpoznania, jak i ujawniać podatności możliwe do zaatakowania, niewidoczne w standardowych badaniach. Praca ta pokazuje, że nawet w rzadkiej i agresywnej chorobie podejście oparte na biologii może przynieść rzeczywiste korzyści kliniczne, w tym trwałe odpowiedzi na leki takie jak pazopanib i trastuzumab derukstekan. Szerzej, sugeruje to, że pacjenci z DSRCT — a przez to także z innymi ultra-rzadkimi nowotworami — zyskają na rutynowym dostępie do kompleksowego profilowania molekularnego i ekspertowej oceny, torując drogę do przyszłych badań, w których terapie są wybierane nie tylko według typu guza, lecz według unikalnych molekularnych odcisków palców nowotworu każdej osoby.
Cytowanie: Renner, M., Oleś, M., Paramasivam, N. et al. Multi-layered molecular profiling informs the diagnosis and targeted therapy of desmoplastic small round cell tumor. Nat Commun 17, 3397 (2026). https://doi.org/10.1038/s41467-026-71636-0
Słowa kluczowe: desmoplastyczny guz z małych okrągłych komórek, onkologia precyzyjna, profilowanie multi-omiczne, terapia ukierunkowana, sprzężone z przeciwciałem leki cytotoksyczne