Clear Sky Science · pl
Interakcja zależnej i niezależnej od SLC33A1 O-acetylacji kwasu sjalowego w Golgi w katalizie przez CASD1
Jak drobne modyfikacje cukrów mogą kształtować zdrowie i chorobę
Nasze komórki są pokryte złożonymi łańcuchami cukrowymi, które działają jak molekularne dowody tożsamości, kierując odpowiedzią immunologiczną, rozwojem i nawet sposobem, w jaki wirusy przyczepiają się do komórek. W badaniu tym przeanalizowano subtelną, lecz wpływową modyfikację tych cukrów — dodawanie małych „czapek” chemicznych zwanych grupami acetylowymi do końcowego cukru o nazwie kwas sjalowy — i odkryto zaskakujący, dwuetapowy mechanizm molekularny kontrolujący ten proces w aparacie Golgiego. Zrozumienie tego ukrytego systemu pomaga wyjaśnić pewne ciężkie zaburzenia neurologiczne i daje wskazówki, jak komórki precyzyjnie dostrajają swoją powierzchnię w zdrowiu i chorobie. 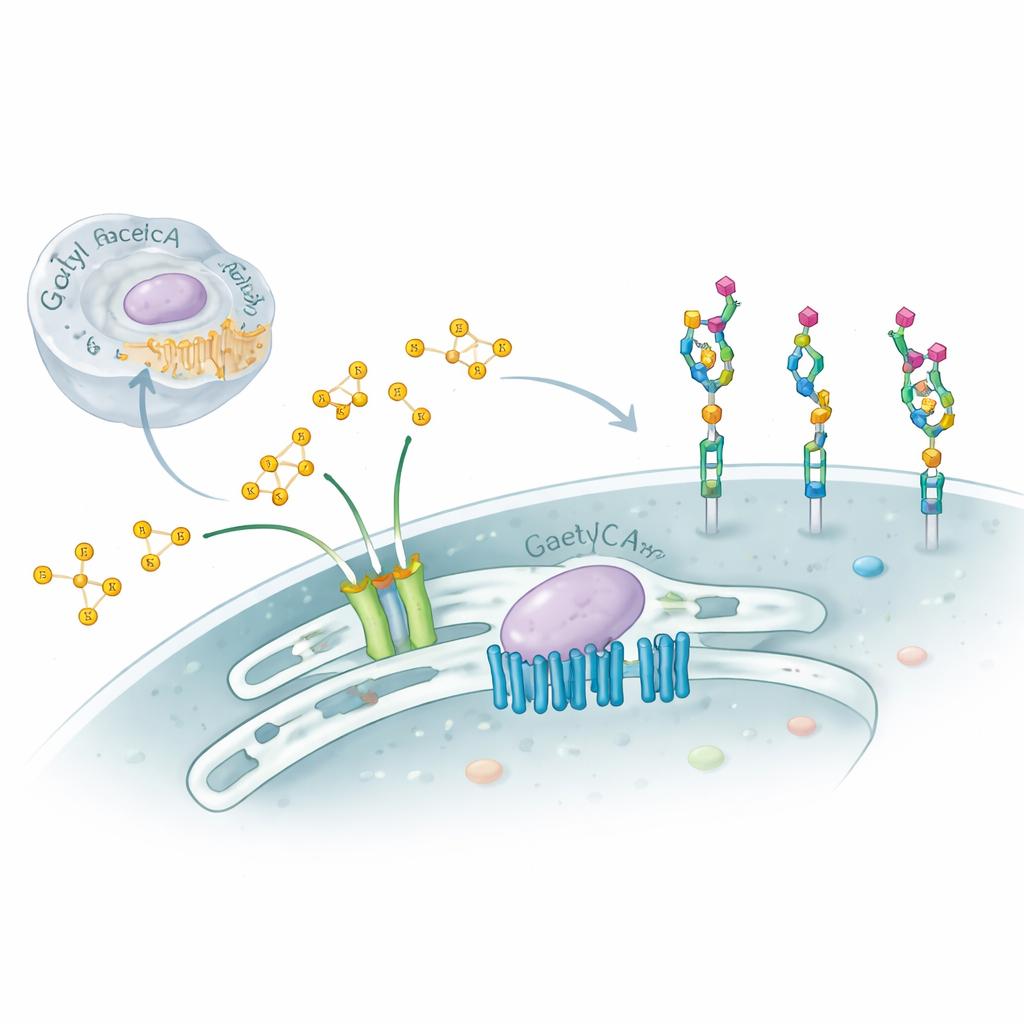
Specjalne cukry na powierzchni komórek
Kwas sjalowy znajduje się na zewnętrznych końcach wielu cukrów powierzchniowych białek i lipidów, szczególnie na cząsteczkach zwanych gangliozydami w mózgu. Poprzez drobne zmiany kwasu sjalowego — na przykład dodanie jednej lub dwóch grup acetylowych w określonych pozycjach — komórki mogą maskować istniejące miejsca rozpoznawcze lub tworzyć nowe. Wirusy takie jak grypa typu C i niektóre koronawirusy specyficznie rozpoznają te zmodyfikowane cukry, a acetylowane gangliozydy mogą wpływać na to, czy neurony przeżyją, czy umrą, oraz na rozwój nowotworów. Mimo ich znaczenia, mechanizmy komórkowe umieszczające te grupy acetylowe w Golgi pozostawały słabo poznane.
Transporter i enzym działają wspólnie
Badacze skupili się na dwóch białkach zlokalizowanych w Golgi lub w jego sąsiedztwie: SLC33A1, transporterze przenoszącym acetylo-CoA (główny donor grup acetylowych w komórce) przez błony, oraz CASD1, enzymie znanym z przenoszenia grup acetylowych na kwasy sjalowe. Przy użyciu edycji genów w ludzkich i chomich liniach komórkowych usunęli SLC33A1 i obserwowali, co dzieje się z konkretnymi gangliozydami. Komórki bez SLC33A1 wciąż potrafiły syntetyzować podstawowe gangliozydy GD3 i GD2, lecz całkowicie straciły formy 9-O-acetylowane, charakterystyczną modyfikację związaną z nowotworami i funkcjami nerwowymi. Ponowne wprowadzenie ludzkiego SLC33A1 przywróciło te acetylowane gangliozydy, co pokazuje, że SLC33A1 jest kluczowym dostawcą acetylo-CoA dla tej ścieżki. 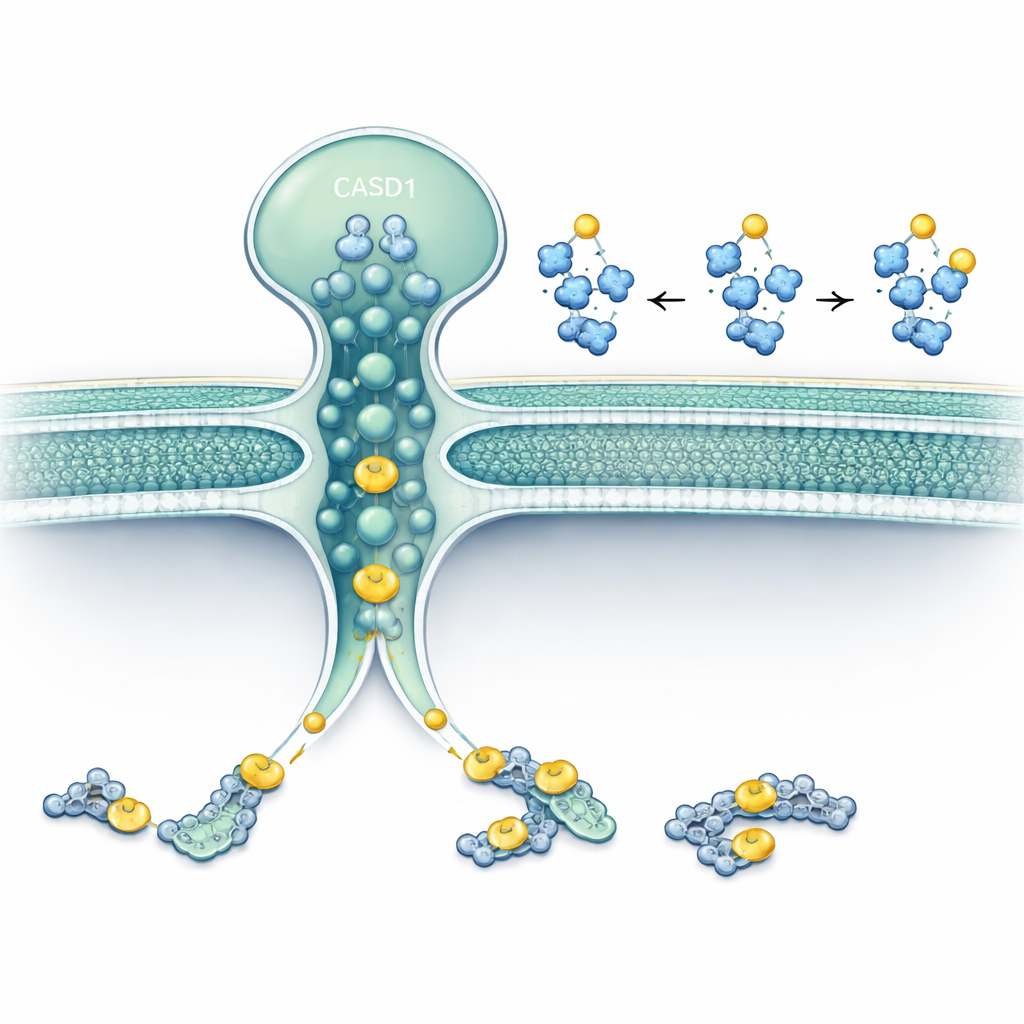
Mutacje u pacjentów ujawniają znaczenie medyczne
SLC33A1 został powiązany z kilkoma rzadkimi schorzeniami neurologicznymi, w tym ciężkim zaburzeniem dziecięcym (zespół Huppke–Brendel), pewną postacią dziedzicznej spastycznej paraplegii oraz późno-nawracającą ataksją móżdżkową. Zespół odtworzył cztery warianty SLC33A1 pochodzące od pacjentów w komórkach pozbawionych normalnego transportera i sprawdził, czy zmienione białka mogą przywrócić acetylację gangliozydów. Wszystkie cztery wykazywały zmniejszoną funkcję, a najcięższe mutacje o początku w dzieciństwie ledwie przywracały jakąkolwiek acetylację. Korzystając z niedawno rozwiązanego trójwymiarowego modelu SLC33A1, autorzy nanieśli te mutacje na strukturę białka i pokazali, jak prawdopodobnie zaburzają jego architekturę lub zdolność wiązania acetylo-CoA. To mocno sugeruje, że upośledzona acetylacja gangliozydów przyczynia się do objawów neurologicznych obserwowanych u pacjentów.
Ukryte drugie miejsce aktywne w CASD1
Praca ujawniła także niespodziewany zwrot akcji: CASD1 wydaje się być enzymem o podwójnym zastosowaniu. Jego znana część w świetle Golgiego wykorzystuje acetylo-CoA dostarczone przez SLC33A1. Jednak gdy SLC33A1 został usunięty, komórki wciąż potrafiły umieścić pojedynczą grupę acetylową na niektórych kwasach sjalowych w określonych warunkach, chociaż nie dodawały drugiej grupy potrzebnej do bardziej złożonych wzorców. Korzystając z zaawansowanych metod predykcji struktury i symulacji molekularnych, autorzy pokazali, że część transbłonowa CASD1 przypomina znany transbłonowy acetylotransferaz z lizosomów. Zlokalizowali kluczowe aminokwasy w tym regionie, które wiążą acetylo-CoA po stronie cytosolowej i przekazują jego grupę acetylową przez błonę bezpośrednio do kwasu sjalowego. Gdy te reszty zostały zmienione, CASD1 tracił tę drugą aktywność zarówno w testach in vitro, jak i w żywych komórkach.
Dwie drogi, jeden precyzyjny kod cukrowy
Łącznie dane wspierają model „dwóch miejsc katalitycznych”. Jedna droga polega na SLC33A1 przynoszącym acetylo-CoA do światła Golgiego, gdzie luminalna domena CASD1 dodaje grupę acetylową do kwasu sjalowego, umożliwiając zarówno proste, jak i podwójne wzorce acetylacji. Druga droga jest zintegrowana z rdzeniem transbłonowym CASD1, który sięga bezpośrednio do cytosolowego acetylo-CoA i może wykonać podstawowy poziom acetylacji nawet gdy SLC33A1 jest nieobecny. Dla laika oznacza to, że pojedynczy enzym, zasilany przez dwa różne źródła acetyli, zapisuje subtelne „znaki interpunkcyjne” na cukrach powierzchni komórek. Gdy transporter lub którakolwiek część enzymu jest uszkodzona, te znaki są źle umiejscowione lub ich brakuje, co może pomóc wyjaśnić niektóre choroby neurodevelopmentalne i neurodegeneracyjne oraz podkreśla nową warstwę regulacji w sposobie, w jaki komórki kształtują swoją zewnętrzną tożsamość.
Cytowanie: Albers, M., Bosse, L., Schröter, L. et al. Interplay of SLC33A1-dependent and -independent Golgi sialic acid O-acetylation in CASD1 catalysis. Nat Commun 17, 3156 (2026). https://doi.org/10.1038/s41467-026-71333-y
Słowa kluczowe: kwas sjalowy, acetylacja w Golgi, gangliozydy, SLC33A1, CASD1