Clear Sky Science · pl
Dynamiczna struktura midnolin-proteasomu podczas degradacji substratów niezależnej od ubikwityny
Jak komórki szybko wyrzucają śmieci
W każdej komórce białka są nieustannie wytwarzane i rozkładane. Wiele z nich jest najpierw znakowanych małymi cząsteczkami zwanymi ubikwityną, zanim trafią do głównej maszynerii recyklingowej komórki — proteasomu. Jednak niektóre białka jądrowe muszą zostać usunięte tak szybko, że nie ma czasu na znakowanie. Badanie to ujawnia, jak mało poznane białko pomocnicze, midnolina, wpina się bezpośrednio w proteasom, aby usuwać te pilne cele, dając wskazówki, jak komórki utrzymują aktywność genów pod ścisłą, szybką kontrolą.
Skrót do komórkowego niszczarki
Proteasom 26S jest kompleksem o kształcie baryłki, który rozdrabnia białka na małe fragmenty. Tradycyjnie rozpoznaje cele poprzez łańcuchy ubikwityny do nich przyczepione. Ostatnie badania odkryły alternatywną drogę: „skrót”, w którym midnolina eskortuje pewne białka jądrowe — zwłaszcza produkty genów natychmiastowej odpowiedzi, które szybko włączają i wyłączają geny — prosto do proteasomu bez żadnych znaków ubikwitynowych. Te białka, na przykład czynniki transkrypcyjne zaangażowane w reakcje na stres i zapalenie, muszą pojawiać się i znikać w ciągu minut. Nowa praca łączy wysokorozdzielczą kriomikroskopię elektronową z eksperymentami biochemicznymi, aby niemal klatka po klatce odwzorować, jak midnolina zaczepia się o proteasom i ustawia swój ładunek do zniszczenia.
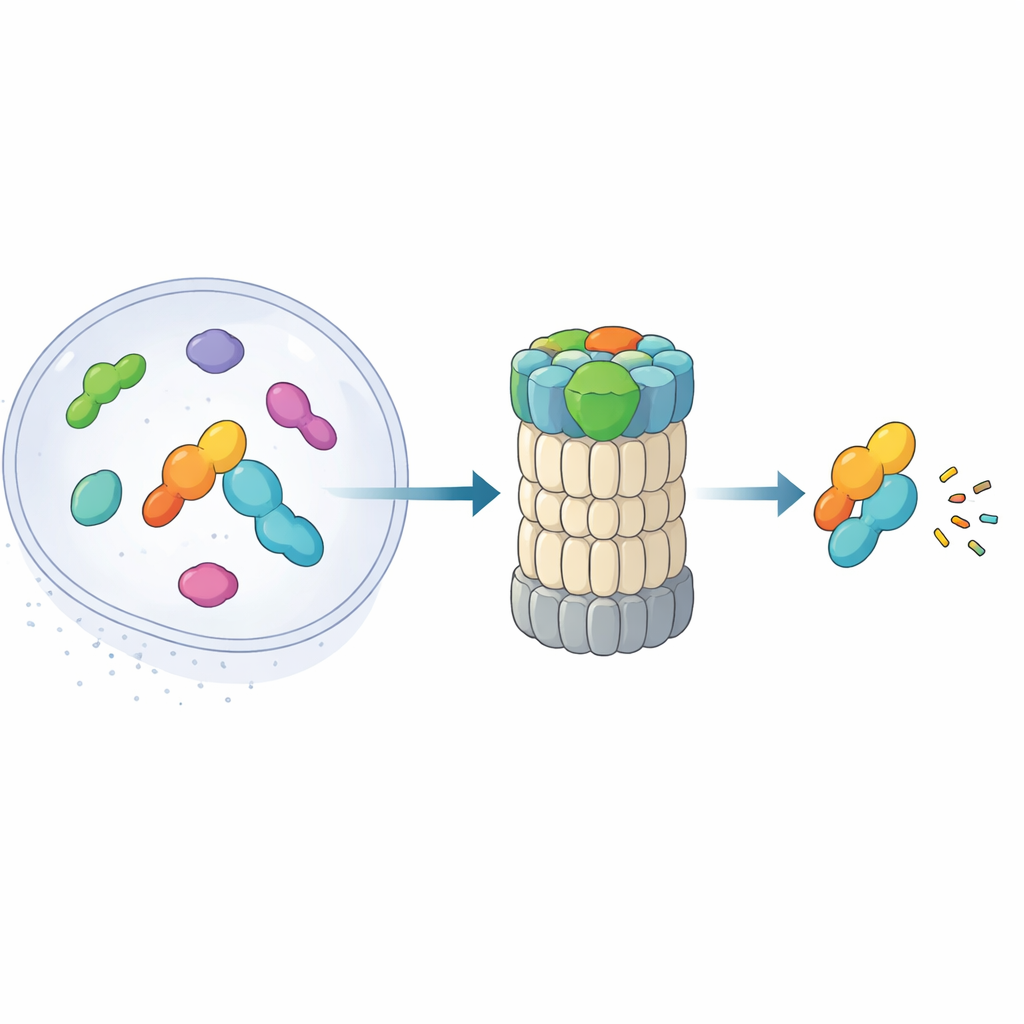
Trzyczęściowy pomocnik, który chwyta i ukierunkowuje cele
Midnolina działa jak narzędzie wielofunkcyjne z trzema kluczowymi modułami. Jeden koniec, helisa C-terminalna, wpina się w miejsce dokujące na składniku proteasomu zwanym RPN1, kotwicząc midnolinę przy maszynie recyklingowej. Centralny obszar „Catch” rozpoznaje i zaciska się na specyficznej, nitkowatej cesze (degronie) w białkach docelowych. Na przeciwnym końcu znajduje się domena podobna do ubikwityny. Zaskakująco, domena ta nie służy przede wszystkim do wiązania proteasomu, jak ma to miejsce w podobnych shuttle’ach. Autorzy pokazują zamiast tego, że przytula ona RPN11, enzym, który zwykle zdejmuje ubikwitynę z substratów. W tym kontekście RPN11 działa bardziej jak stelaż: obejmując ubikwitynopodobny fragment midnoliny, pomaga utrzymać domenę Catch i jej związany ładunek bezpośrednio nad wąskim wejściem do proteasomu.
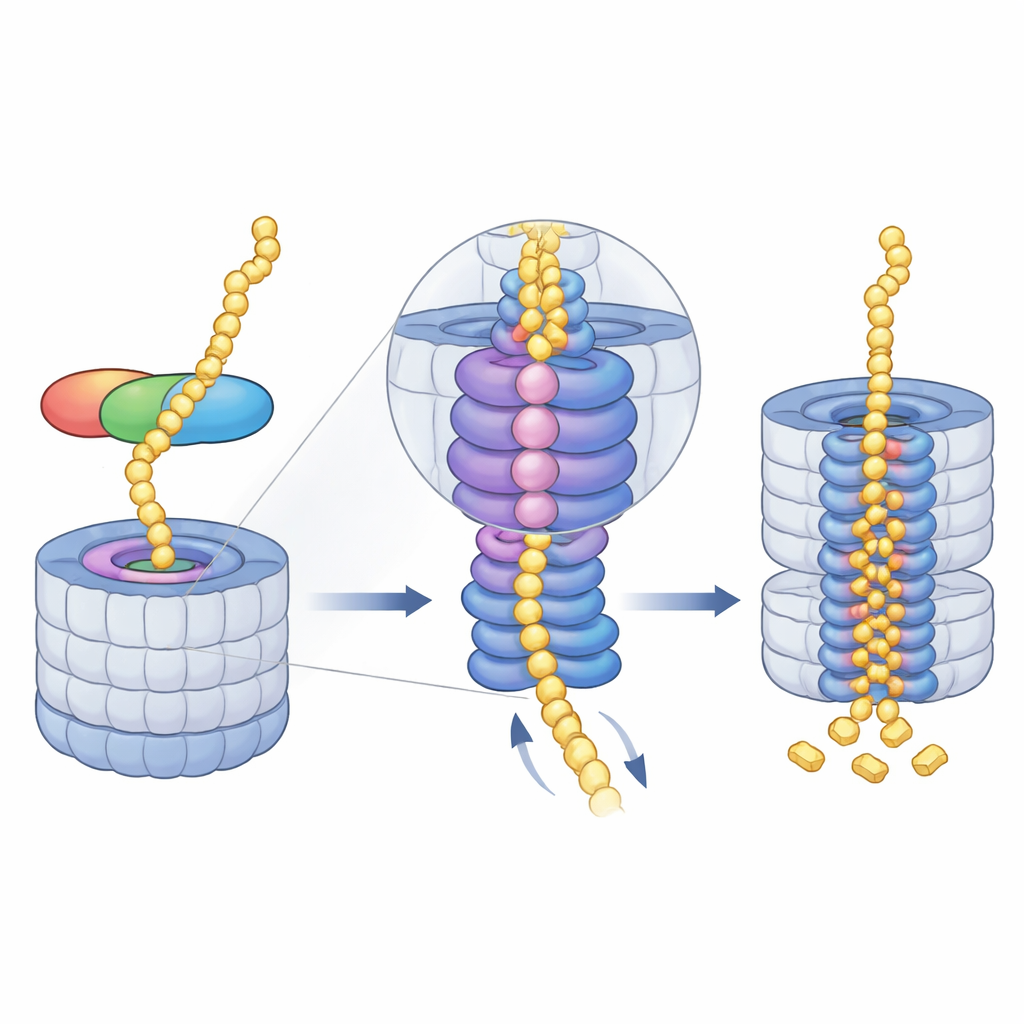
Ukierunkowanie białka do mielącego rdzenia
Gdy midnolina się zadokuje, przejmuje napęd energochłonny — pierścień ATPaz AAA+. Pierścień ten leży tuż pod otworem wejściowym i krok po kroku wciąga rozwinięte łańcuchy białkowe do rdzenia. Zrzuty kriomikroskopii ukazują serię pozycji w układzie „spiralnych schodów”, które przyjmują sześć podjednostek napędu, chwytając i przekazując substrat przez centralny kanał. Autorzy zarejestrowali cztery kolejne etapy tego cyklu, wszystkie z materiałem związanym przez midnolinę przewleczonym przez otwór, i nawet zaobserwowali, jak uwolnienie jonu magnezu w jednej podjednostce pokrywa się z przesunięciem całego pierścienia w dół. Sugeruje to, że skoordynowane użycie ATP i uwalnianie magnezu pomagają „nakręcać” białko głębiej do komory, gdzie znajdują się miejsca cięcia.
Dlaczego pozycjonowanie i współwytwarzanie mają znaczenie
Zespół sprawdził, jak każdy moduł midnoliny przyczynia się do wydajności. Sama helisa kotwicząca może wiązać RPN1, ale nie zwiększa znacząco aktywności proteasomu. Usunięcie domeny Catch pozostawia wiele proteasomów w stanie bezczynności, bez substratu, mimo że midnolina nadal może przyłączać się; zastąpienie Catch trwale związanym substratem również nie przywraca pełnej aktywności. Wyniki te wskazują, że Catch robi więcej niż tylko chwyta cel — musi również precyzyjnie ustawić białko przy wejściu do poru. Dane biochemiczne i transkryptomiczne guzów pokazują ponadto, że midnolina ma tendencję do współwytwarzania ze swoimi substratami. Przy jednoczesnej ekspresji midnolina lepiej się fałduje i tworzy stabilne kompleksy, tworząc gotowy pakiet „zdegradować mnie”, który można szybko dostarczyć do proteasomu, gdy komórce potrzeba zresetować ekspresję genów.
Autooczyszczanie i przyszłe możliwości medyczne
Po tym, jak białko docelowe zostanie wciągnięte i pocięte, midnolina sama nie zostaje oszczędzona. Jej własne nieuporządkowane regiony mogą zostać przewleczone przez napęd i wprowadzone do tej samej komory destrukcji, co zapobiega nadmiernemu nagromadzeniu białka pomocniczego. Oświetlając tę drogę do proteasomu wolną od ubikwityny, badanie rozszerza nasze rozumienie, jak komórki zarządzają czasem życia białek na bardzo ciasnych harmonogramach. Sugeruje też nowe strategie terapeutyczne: poprzez inżynierię cząsteczek opartych na midnolinie, które przyłączają chorobotwórcze białka jądrowe bezpośrednio do proteasomu, badacze mogą pewnego dnia być w stanie szybciej i bardziej selektywnie eliminować „niedrogowalne” cele, w tym niektóre czynniki napędzające rozwój nowotworów.
Cytowanie: Zhu, C., Qin, L., Dai, Z. et al. Structural dynamics of the midnolin-proteasome during ubiquitin-independent substrate turnover. Nat Commun 17, 2800 (2026). https://doi.org/10.1038/s41467-026-71002-0
Słowa kluczowe: proteasom, midnolina, degradacja białek, szlak niezależny od ubikwityny, geny natychmiastowej odpowiedzi