Clear Sky Science · pl
Kompetencja transkrypcyjna determinuje zdolność izolowanych jednostek MSR do inicjowania heterochromatyny
Ukryte przełączniki w naszym DNA
Nasze genomy są upakowane w jądrze komórkowym w dwóch głównych stanach: aktywnych regionach zawierających geny oraz silnie upakowanych fragmentach długo uważanych za „ciemną materię” genetyczną. To badanie stawia pozornie proste pytanie: co powoduje, że fragment DNA staje się tym ściśle upakowanym, wyciszającym geny materiałem — znanym jako heterochromatyna? Analizując konkretną klasę powtarzalnego DNA u myszy, autorzy pokazują, że nie wszystkie powtórzenia są takie same: tylko te zdolne do podtrzymania szczególnego rodzaju transkrypcji potrafią przełączyć mechanizm budujący i utrzymujący te ciche sąsiedztwa DNA.
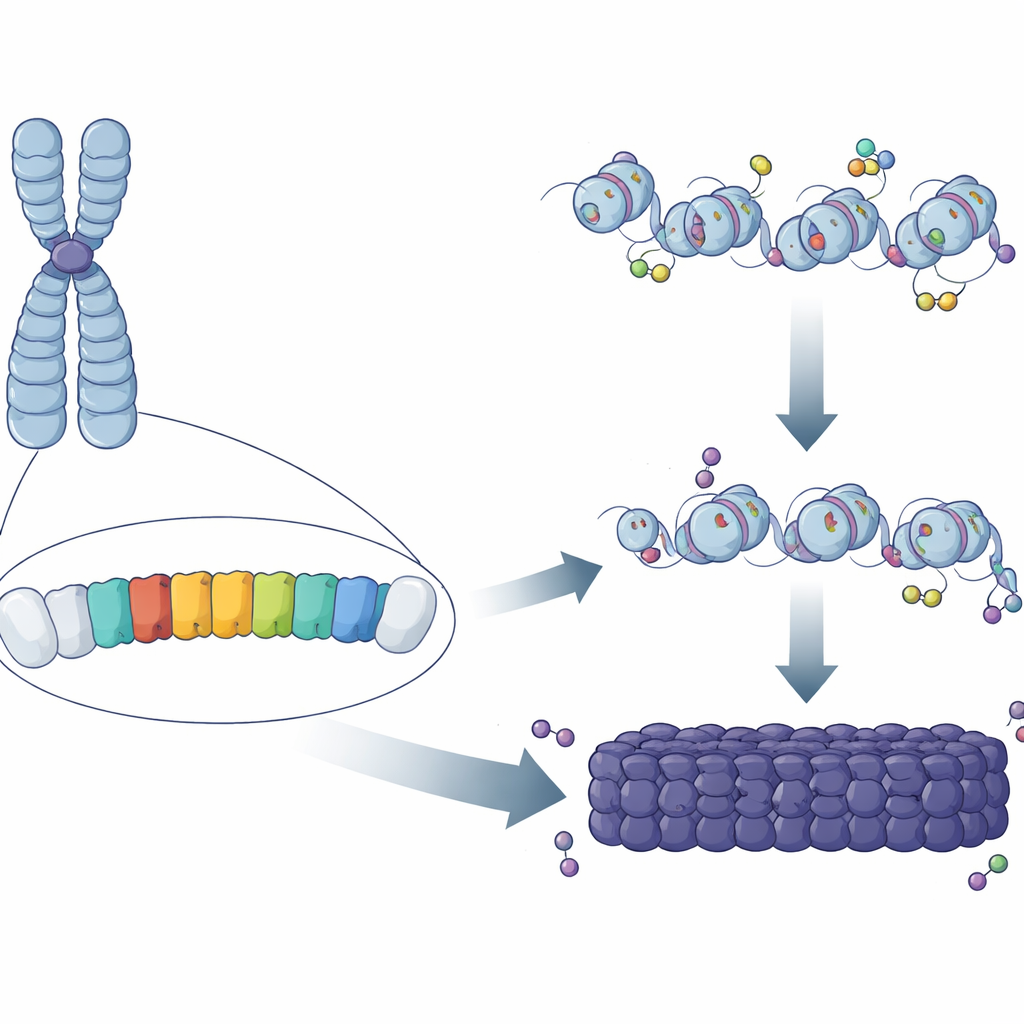
Powtarzające się wzorce w genomie
Prawie połowa DNA ssaków składa się z sekwencji powtarzalnych, z których wiele skupia się w regionach wokół centromeru. U myszy jedną z głównych składowych tych obszarów jest „major satellite repeat” (MSR) — krótka bogata w A/T sekwencja kopiowana setki tysięcy razy. Klasyczne badania wykazały, że te regiony są pokryte chemicznymi znakami i białkami, które zamykają DNA w kompaktowy, ochronny stan. Nadal jednak pozostawało zagadką, dlaczego niektóre kopie MSR stają się w pełni heterochromatynowe, podczas gdy inne, rozproszone w genomie, nie. Autorzy założyli, że drobne różnice w sekwencji lub zachowaniu poszczególnych jednostek MSR mogą decydować o tym, czy mogą one zaszczepić, czyli „nukleować”, płat heterochromatyny.
Budowa miejsca testowego w genomie
Aby przetestować ten pomysł w sposób czysty, zespół zmodyfikował mysie komórki macierzyste embrionalne, tworząc sztuczne miejsce dokowania w cichym fragmencie chromosomu 2 — obszarze bez pobliskich genów czy powtórzeń i bez wykrywalnej aktywności. Do tego neutralnego miejsca wstawili różne fragmenty DNA: niezmienione jednostki MSR, mocno porysowane warianty MSR oraz elementy kontrolne, takie jak wirusowe promotory czy fragmenty elementów mobilnych. Pozwoliło to sprawdzić, jednostka po jednostce, które sekwencje potrafią przyciągnąć cechy charakterystyczne dla heterochromatyny: specyficzny znak chemiczny na histonach (H3K9me3), wiązanie białek HP1 oraz włączenie histonu łącznikowego H1 — wszystkie te składniki razem zagęszczają i stabilizują miejscową chromatynę.
Tylko powtórzenia gotowe do transkrypcji inicjują cichą chromatynę
Wyniki okazały się wyraźnie selektywne. Pojedyncza, niezmieniona jednostka MSR wstawiona w miejsce testowe nie wystarczyła, by zmienić chromatynę. Natomiast trzy lub więcej tandemowych kopii niezmienionej sekwencji MSR przekształcały otaczający region w wyspę heterochromatyny, z silnym H3K9me3, obecnością HP1 i histonu H1. Dla porównania, jednakowo długie odcinki porysowanej sekwencji MSR lub innego typu powtórzenia (region 5' UTR LINE-1) nie zdołały tego zrobić, choć mogły napędzać silną transkrypcję. Kluczową różnicą było to, że wielokrotne niezmienione jednostki MSR wspierały umiarkowaną, dwukierunkową transkrypcję produkującą krótkie, niestandardowe cząsteczki RNA ściśle związane z chromatyną. To właśnie ten wzorzec, a nie wysoka, genopodobna transkrypcja, korelował ze zdolnością do nukleowania heterochromatyny.
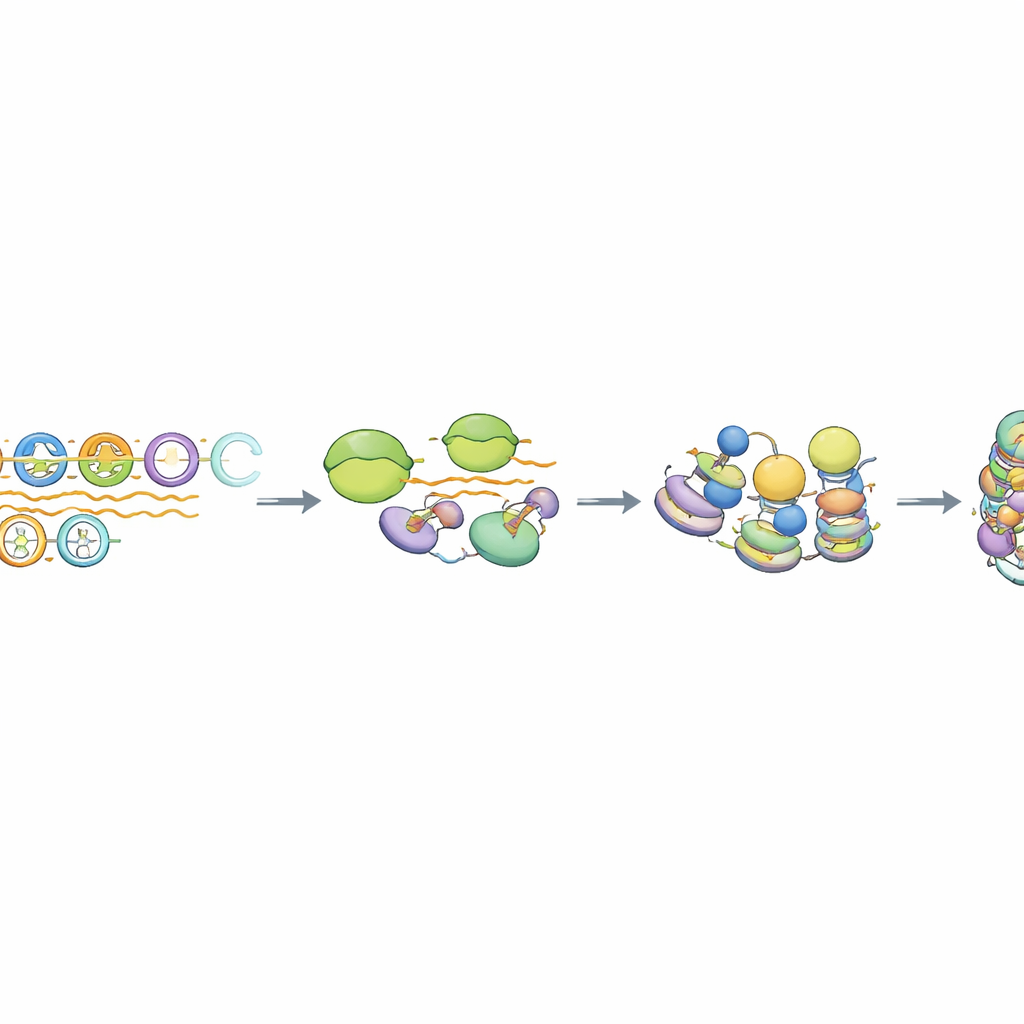
Szczególny rodzaj transkrypcji i przetwarzania RNA
Głębsza analiza wykazała, że polimeraza RNA II — enzym zwykle produkujący mRNA — krótko angażuje się na tablicach MSR, ale nie przechodzi efektywnie w długie transkrypty. Powstające RNA pozbawione są typowych cech mRNA, takich jak ochronna czapka 5' i długie ogony poli‑A, i pozostają blisko DNA, które je stworzyło. Kompleks białkowy o nazwie Integrator, znany z przycinania i terminacji niektórych RNA niekodujących, był specyficznie wzbogacony przy niezmienionych jednostkach MSR. Gdy aktywność tnąca Integratora została zmniejszona, poziomy RNA pochodzącego z MSR wzrosły znacząco, ale kluczowy represyjny znak histonowy utrzymał się, podczas gdy wiązanie HP1 zmieniło się subtelnie. Analiza obejmująca cały genom wykazała, że tylko najbardziej niezmienione ~10–15% kopii MSR zachowuje się w ten sposób, podkreślając podzbiór „kompetentnych” powtórzeń zaprogramowanych do tej ścieżki wyciszania sprzężonej z transkrypcją.
Rozplecione DNA jako imitacja promotora
Zespół badał także, jak samo DNA MSR sprzyja tej nietypowej transkrypcji. Wielokrotne tablice MSR, ale nie pojedyncze czy podwójne kopie, wykazywały wyraźne ślady lokalnie rozpleconego DNA i hybryd RNA:DNA — strukturalne cechy często spotykane w pobliżu aktywnych promotorów i miejsc zatrzymywania polimerazy. Konfiguracje te nasilały się po zahamowaniu topoizomeraz i pokrywały się z większą transkrypcją MSR oraz silniejszymi cechami heterochromatyny. Autorzy proponują, że trzy lub więcej tandemowych jednostek MSR tworzy fizyczną topologię DNA przypominającą promotor, zapraszając polimerazę i czynniki transkrypcyjne do zaangażowania się na tyle, by wygenerować krótkie RNA, które wraz ze specyficznymi białkami wzmacniają zwartą architekturę chromatyny.
Dlaczego to ma znaczenie dla zdrowia genomu
Dla laika ta praca ujawnia, że części naszej „śmieciowej” DNA działają jak precyzyjnie dostrojone przełączniki, wykorzystując mieszankę kształtu DNA, niskopoziomowej transkrypcji i przetwarzania RNA do budowy ochronnej powłoki genomu. Tylko jednostki MSR zdolne do podtrzymania kontrolowanej, niemessengerowej transkrypcji mogą zapoczątkować nową heterochromatynę, podczas gdy porysowane lub nadmiernie aktywne elementy nie potrafią. Ta logika oparta na DNA/RNA pomaga wyjaśnić, jak komórki rozróżniają regiony przeznaczone do wyciszenia od tych, w których dopuszczone jest występowanie genów, oraz dlaczego zaburzenia w regulacji RNA satelitarnych wiążą się z rakiem i problemami rozwojowymi. W istocie badanie pokazuje, że powtarzalne „tło” genomu nie jest biernym wypełniaczem, lecz aktywnym inżynierem architektury jądrowej i stabilności.
Cytowanie: Lo, YH., Shukeir, N., Erikson, G. et al. Transcriptional competence defines the heterochromatin nucleating potential of isolated MSR units. Nat Commun 17, 2653 (2026). https://doi.org/10.1038/s41467-026-70991-2
Słowa kluczowe: heterochromatyna, DNA satelitarny, RNA niekodujący, struktura chromatyny, stabilność genomu