Clear Sky Science · pl
Timosaponin AIII zwiększa skuteczność komórek CAR‑T i zapobiega nawrotom przez upośledzenie CAR‑Tregów
Wyłączanie hamulców odpornościowych, by wzmocnić terapię przeciwnowotworową
Dla osób z agresywnymi nowotworami krwi terapia komórkami CAR‑T może być przełomowa: własne komórki pacjenta są przeprogramowywane, by tropić komórki nowotworowe. Mimo to wielu pacjentów doświadcza nawrotów, gdy te zmodyfikowane komórki tracą siłę. W badaniu tym badano molekułę pochodzenia roślinnego — Timosaponinę AIII — która pomaga komórkom CAR‑T zachować aktywność dłużej, selektywnie dezaktywując kluczowy hamulec w układzie odpornościowym, co może uczynić te terapie trwalszymi i skuteczniejszymi.
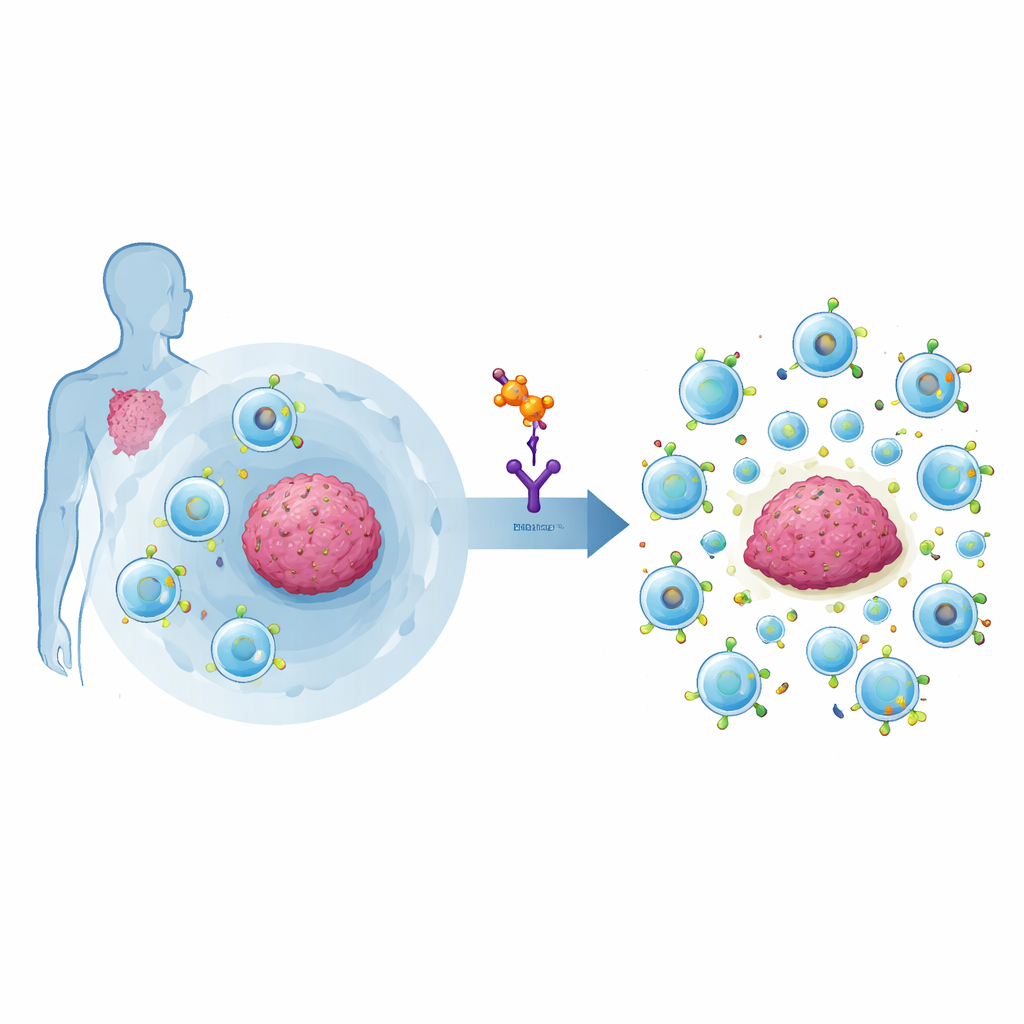
Dlaczego potężni wojownicy przeciwnowotworowi czasem ustają
Komórki CAR‑T to komórki odpornościowe skonstruowane tak, by niosły sztuczny sensor rozpoznający cele nowotworowe, np. CD19 na złośliwych limfocytach B. U prawdziwych pacjentów tylko około połowa doświadcza długotrwałych remisji. Jednym z głównych winowajców jest specjalna podgrupa komórek odpornościowych zwana limfocytami T regulatorowymi, czyli Tregami. Komórki te normalnie zapobiegają atakom układu odpornościowego na zdrowe tkanki, ale w nowotworach mogą tłumić odpowiedzi przeciwnowotworowe, w tym działanie komórek CAR‑T. Ostatnie badania kliniczne wykazały, że gdy produkty CAR‑T zawierają zbyt wiele Tregów, pacjenci częściej wykazują oporność na leczenie lub doświadczają nawrotu. Niestety istniejące leki usuwające Tregi często działają nieprecyzyjnie, uszkadzając też pożyteczne komórki odpornościowe.
Delikatny pomocnik z rośliny leczniczej
Naukowcy opracowali system przesiewowy, który informuje, gdy centralny przełącznik kontroli Tregów, białko FoxP3, wyłącza aktywację odporności. Przetestowali ponad 3 000 związków naturalnych i zatwierdzonych leków i wyselekcjonowali te, które mogły osłabić wpływ FoxP3 bez zabijania komórek. Wyjątkowo wyróżnił się jeden kandydat: Timosaponina AIII (TAIII), steroidopodobna molekuła z tradycyjnego chińskiego zioła Anemarrhena asphodeloides, już badana klinicznie jako miejscowy lek przeciwzapalny do skóry. W ludzkich komórkach T hodowanych w warunkach sprzyjających przekształceniu w Tregi, TAIII wyraźnie zmniejszał powstawanie i aktywność tych supresyjnych komórek, jednocześnie pozostawiając inne typy limfocytów T w dużej mierze nienaruszone. Sugerowało to, że TAIII może przesunąć układ odpornościowy od stanu supresji ku reakcji skutecznej.
Jak mała molekuła uwalnia komórki CAR‑T
W pogłębieniu mechanizmu zespół zastosował sondy chemiczne, testy wiązania białek i modelowanie komputerowe, by odkryć, że TAIII przyłącza się do receptora adenozynowego A2A (A2AR), dobrze znanego «wyłącznika» odporności reagującego na wysokie stężenia adenozyny w guzach. Zamiast blokować główne miejsce wiązania, TAIII wciska się w region receptora w błonie komórkowej wrażliwy na cholesterol, działając jako inhibitor allosteryczny. Przesuwając lipidy podobne do cholesterolu i tłumiąc łańcuch sygnałowy kończący się białkiem CREB, TAIII obniża produkcję FoxP3 i narusza program Tregów. Gdy A2AR usunięto z komórek T lub komórek CAR‑T, TAIII tracił swój efekt, co potwierdza, że to właśnie ten receptor jest jego kluczowym celem.
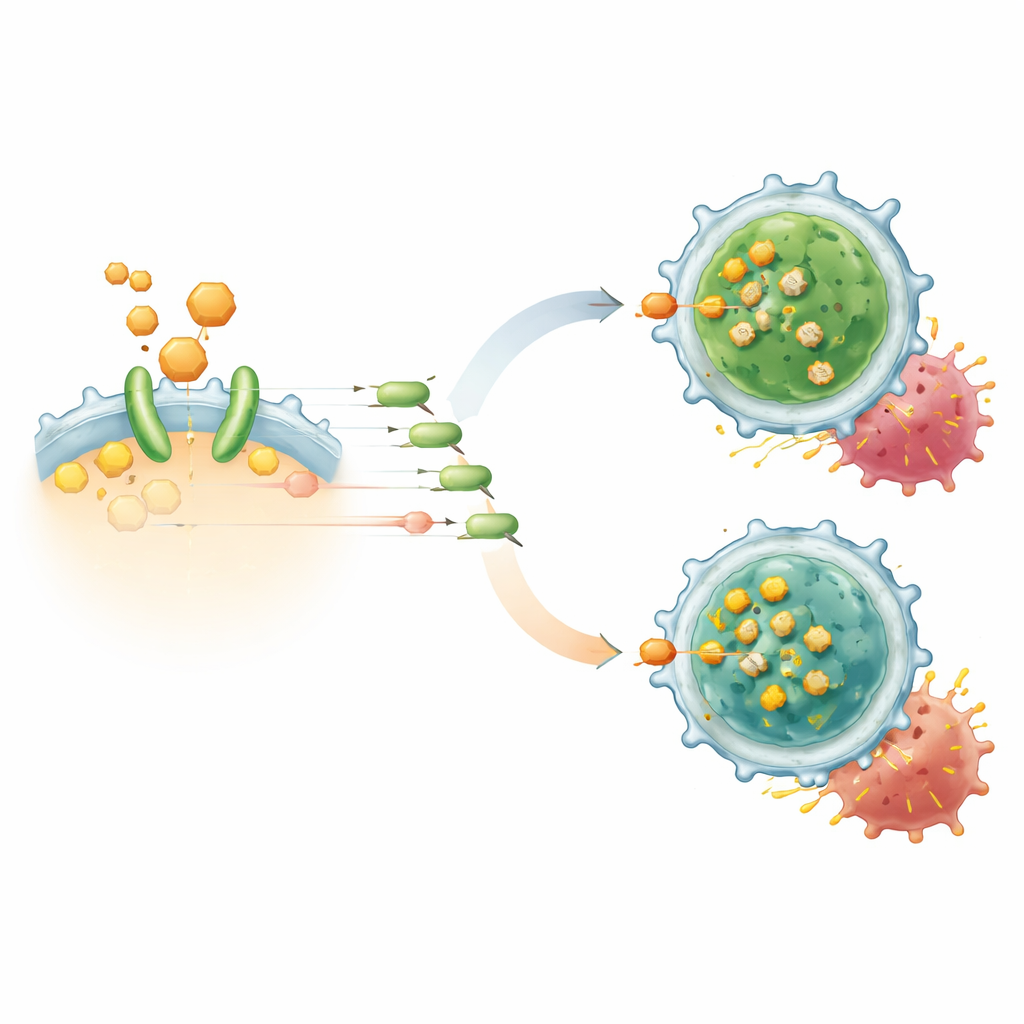
Mocniejsze, dłużej trwające odpowiedzi CAR‑T w modelach
W laboratoryjnych eksperymentach współhodowlanych dodanie TAIII do ludzkich komórek CD19 CAR‑T zwiększało ich zdolność do zabijania komórek chłoniaka i nasilało uwalnianie molekuł ataku, takich jak interferon‑gamma i IL‑2. Równocześnie zmniejszało odsetek komórek CAR‑T o cechach podobnych do Tregów i sprzyjało powstawaniu komórek pamięci centralnej, podzbioru związanego z długotrwałą ochroną. Sekwencjonowanie RNA pojedynczych komórek wykazało, że populacje CAR‑T traktowane TAIII zawierały mniej regulacyjnych komórek z wysoką ekspresją FoxP3 i więcej żywotnych komórek zabójczych. W kilku modelach mysich nowotworów krwi i guzów litych połączenie TAIII z terapią CAR‑T spowolniło wzrost guza, pogłębiło odpowiedź i radykalnie zredukowało późne nawroty. Gdy produkty CAR‑T eksperymentalnie pozbawiono Tregów, TAIII nie dawało dodatkowej korzyści, co podkreśla, że jego główna rola polega na rozbrajaniu tej supresyjnej podgrupy, a nie na nadmiernym pobudzaniu wszystkich komórek T.
Ponad CAR‑T: przebudowa immunologicznego otoczenia guza
Efekty TAIII nie ograniczały się do komórek inżynierskich. U immunokompetentnych myszy z guzami litymi codzienne dawki TAIII zmniejszały liczbę Tregów w guzach, zwiększały napływ komórek CD8 «zabójczych» i podwyższały poziomy cytokin przeciwnowotworowych, bez widocznej toksyczności czy utraty masy ciała. W połączeniu z terapią anty‑PD‑1 — kolejną powszechnie stosowaną formą immunoterapii — TAIII wzmacniało kontrolę nad guzem i rozszerzało populacje korzystnych komórek pamięciopodobnych. Co istotne, TAIII wykazywało niewielki efekt u silnie immunodeficientnych myszy pozbawionych funkcjonalnych komórek T, co wskazuje, że jego aktywność przeciwnowotworowa zależy od przekształcenia odpowiedzi immunologicznej, a nie od bezpośredniego działania toksycznego na komórki nowotworowe.
Co to może znaczyć dla przyszłej opieki onkologicznej
Dla przeciętnego czytelnika przesłanie jest takie: autorzy znaleźli sposób na selektywne poluzowanie jednego z wewnętrznych hamulców układu odporności bez odcinania dopływu paliwa czy nadmiernego przyspieszania. Poprzez wyciszenie limfocytów regulatorowych dzięki precyzyjnej interakcji z receptorem A2A, Timosaponina AIII pomaga komórkom CAR‑T zachować aktywność, tworzyć dłużej żyjące populacje pamięciowe i unikać wyciszenia przez mikrośrodowisko guza. W badaniach przedklinicznych i testach z komórkami CAR‑T pochodzącymi od pacjentów przekładało się to na silniejsze zabijanie guza i mniej nawrotów. Chociaż będą potrzebne badania kliniczne, by potwierdzić bezpieczeństwo i skuteczność u ludzi, TAIII jawi się jako obiecujące, roślinne uzupełnienie, które może uczynić nowoczesne immunoterapie trwalszymi i bardziej skutecznymi.
Cytowanie: Hou, M., Zhang, W., Qi, Z. et al. Timosaponin AIII enhances CAR-T cell potency and prevents relapse through impairing CAR-Tregs. Nat Commun 17, 3045 (2026). https://doi.org/10.1038/s41467-026-70867-5
Słowa kluczowe: terapia komórkami CAR‑T, limfocyty T regulatorowe, receptor adenozynowy A2A, Timosaponin AIII, immunoterapia nowotworów