Clear Sky Science · pl
Przestrzenna heterogeniczność MDSC indukowana sygnalizacją ANXA1‑FPRs napędza immunosupresję w progresji OSCC
Dlaczego obrona organizmu słabo radzi sobie z niektórymi nowotworami jamy ustnej
Płaskonabłonkowy rak jamy ustnej, powszechna postać raka ustnej, często opiera się najskuteczniejszym współczesnym terapiom onkologicznym: immunoterapii uwalniającej własne mechanizmy obronne organizmu. W badaniu zadano podstawowe, lecz kluczowe pytanie: dlaczego potężne komórki odpornościowe, które powinny rozpoznawać i niszczyć nowotwór, tak często zawodzą w tych guzach? Mapując położenie różnych komórek wewnątrz guza i sposób, w jaki się komunikują, badacze odkrywają przesuwającą się „zabawę w kotka i myszkę” między komórkami nowotworowymi, komórkami supresorowymi a cytotoksycznymi limfocytami T, co pomaga wyjaśnić niepowodzenia terapii — i sugeruje sposób na ich naprawę. 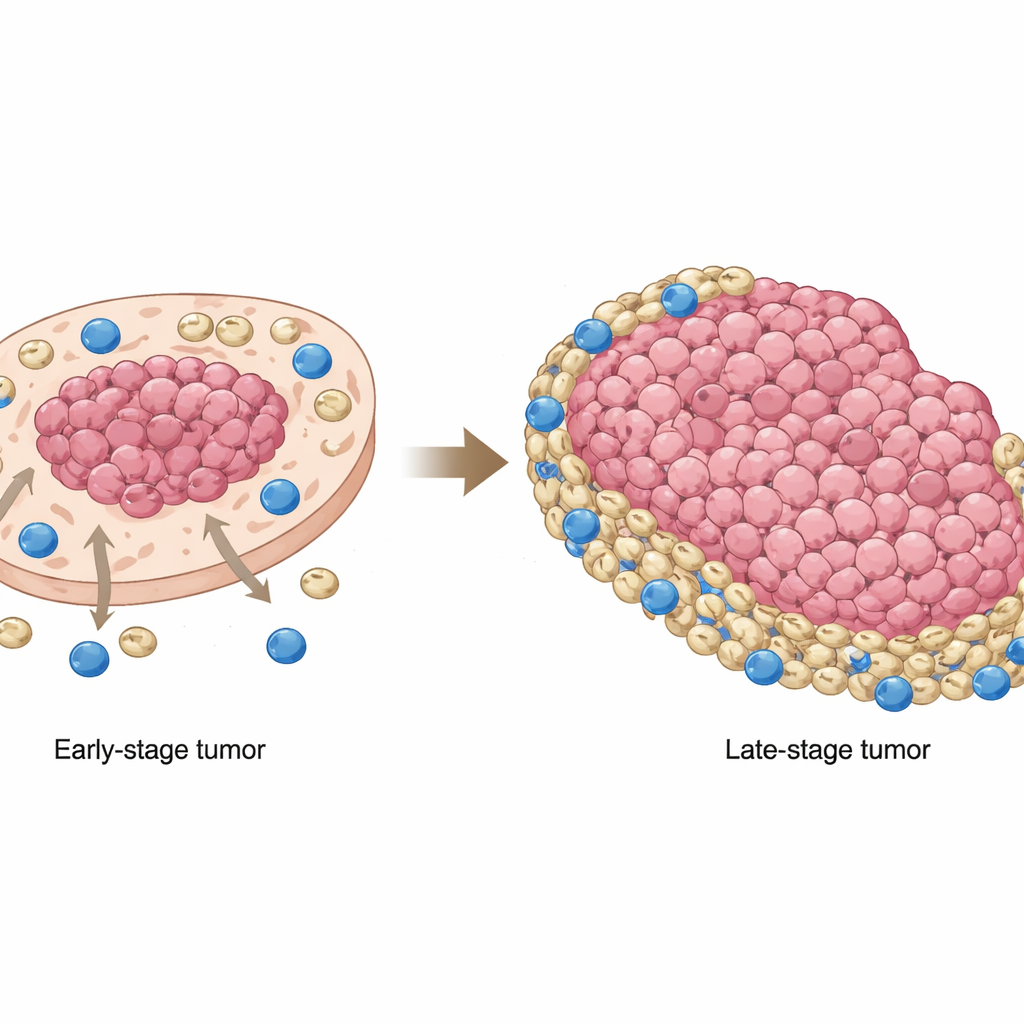
Ukryty krajobraz wewnątrz guza
Autorzy połączyli dwa zaawansowane podejścia: sekwencjonowanie RNA pojedynczych komórek, które odczytuje aktywność poszczególnych komórek, oraz transkryptomikę przestrzenną, która pokazuje lokalizację tych komórek w rzeczywistych przekrojach tkanek guza. Analizując guzy od pacjentów z wczesnymi i zaawansowanymi stadami raka jamy ustnej, zidentyfikowali główne typy komórek: komórki nabłonkowe nowotworu, cytotoksyczne limfocyty CD8, inne komórki T i B, fibroblasty tworzące podporę strukturalną oraz wyspecjalizowane komórki odpornościowe zwane komórkami supresorowymi pochodzenia mieloidalnego (MDSC). Podczas gdy w guzach we wczesnym stadium było więcej aktywnych limfocytów CD8, w zaawansowanych stadiach obserwowano słabsze sygnalizowanie komórek T i silniejsze sygnały tłumiące pochodzące od komórek mieloidalnych, co wskazuje na stopniowo coraz bardziej nieprzyjazne środowisko dla odpowiedzi przeciwnowotworowej.
Przemieszczające się komórki supresorowe
Jednym z najbardziej uderzających odkryć był sposób, w jaki pozycja MDSC zmieniała się wraz z postępem guza. W nowotworach we wczesnym stadium te komórki supresorowe miały tendencję do grupowania się w obszarach bogatych w komórki nowotworowe, blisko jądra guza. W późniejszych stadiach przesuwały się na zewnątrz, gromadząc się w obszarach ubogich w komórki nowotworowe i na obrzeżach, gdzie limfocyty CD8 występowały częściej. Oznaczało to, że w zaawansowanych guzach cytotoksyczne komórki T były w dużej mierze wypychane na krawędzie i tam spotykały pas MDSC, które tłumiły ich zdolność do atakowania komórek nowotworowych. Próbki pacjentów i modele mysie potwierdziły, że ta redystrybucja nie była tylko ciekawostką: gdy nachodzenie się MDSC z komórkami nowotworowymi było mniejsze, a MDSC osiadły w regionach pozagnatowych, pacjenci mieli gorsze przeżycie ogólne. 
Przełącznik sygnalizacyjny między komórkami nowotworowymi a supresorowymi
Badanie przyjrzało się molekularnej „konwersacji” między komórkami nowotworowymi a MDSC obejmującej białko annexin A1 (ANXA1) na komórkach guza i rodzinę receptorów zwanych FPR na komórkach mieloidalnych. W początkowej fazie choroby ANXA1 na komórkach nowotworowych silnie angażowało FPR1 i FPR3, szczególnie na MDSC i makrofagach związanych z guzem, pomagając rekrutować i utrzymywać te komórki supresorowe w centrum guza. W miarę postępu raka poziomy ANXA1 na komórkach nowotworowych spadały, osłabiając te pierwotne połączenia. Jednocześnie coraz więcej MDSC zaczęło wyrażać inny receptor, FPR2, i sygnalizacja ANXA1–FPR2 wyłoniła się jako kompensacyjna droga utrzymująca zaangażowanie MDSC. Konkretna podpopulacja komórek nowotworowych o wysokim poziomie ANXA1, która wykazywała także cechy przypominające komórki macierzyste, wydawała się działać jak „przynęta”, przyciągając MDSC we wczesnej fazie; gdy ANXA1 malało, MDSC przestawały być zakotwiczone w centrum i przesuwały się ku obszarom bogatym w limfocyty CD8.
Wyłączenie tarczy, by poprawić działanie immunoterapii
Aby sprawdzić, czy przerwanie tej komunikacji może poprawić leczenie, badacze użyli mysiego modelu raka jamy ustnej i zablokowali FPR2 małocząsteczkowym inhibitorem WRW4. Samo zahamowanie FPR2 zmniejszyło obecność MDSC i zwiększyło liczbę limfocytów CD8 w mikrośrodowisku guza, lecz nie spowolniło wystarczająco wzrostu guza. Podobnie leczenie przeciwciałem przeciwko punktowi kontrolnemu immunologicznemu anty–PD‑1 przyniosło tylko skromne korzyści, ponieważ MDSC wciąż tworzyły barierę supresyjną. Jednak gdy zastosowano obie terapie łącznie, wzrost guza został zdecydowanie powstrzymany, a myszy żyły dłużej. U tych zwierząt infiltracja MDSC spadła gwałtownie, podczas gdy limfocyty CD8 penetrowały głębiej obszary bogate w komórki nowotworowe, co sugeruje, że zablokowanie FPR2 usuwa kluczową tarczę, która normalnie chroni komórki nowotworowe przed atakiem immunologicznym.
Co to oznacza dla przyszłej opieki onkologicznej
Łącznie praca pokazuje, że nie tylko typy komórek, lecz także ich przestrzenne rozmieszczenie i partnerskie sygnalizowanie decydują o tym, czy immunoterapia może odnieść sukces w raku jamy ustnej. W miarę postępu guza MDSC przemieszczają się ze środka na obrzeża, gdzie przechwytują cytotoksyczne komórki T, a sygnalizacja ANXA1–FPR2 pomaga utrzymać tę supresyjną organizację. Zakłócając tę ścieżkę — szczególnie w połączeniu z istniejącymi lekami punktów kontrolnych — może być możliwe przeprojektowanie środowiska guza tak, by własne komórki odpornościowe organizmu znów rozpoznawały i niszczyły nowotwór. To sugeruje konkretną strategię: łączenie blokerów FPR2 z immunoterapią może poprawić wyniki u pacjentów, których nowotwory jamy ustnej obecnie opierają się najlepszym dostępnym terapiom.
Cytowanie: Li, F., Han, Y., Ou, F. et al. Spatial heterogeneity of MDSCs mediated by ANXA1-FPRs signaling drives immune suppression in OSCC progression. Nat Commun 17, 2535 (2026). https://doi.org/10.1038/s41467-026-70861-x
Słowa kluczowe: płaskonabłonkowy rak jamy ustnej, mikrośrodowisko guza, komórki supresorowe pochodzenia mieloidalnego, transkryptomika przestrzenna, immunoterapia nowotworów