Clear Sky Science · pl
Sygnałowanie FGFR tworzy gradienty przestrzenne tożsamości komórek wydzielniczych wzdłuż osi proksymalno-dystalnej dróg oddechowych
Jak nasze drogi oddechowe cicho sortują i chronią powietrze, które wdychamy
Każdy oddech przepływa powietrze po milionach komórek wyściełających tchawicę i płuca. Te komórki robią znacznie więcej niż tworzą powierzchnię biernie przepuszczającą powietrze: detoksykują zanieczyszczenia, zwalczają drobnoustroje i pomagają zapobiegać zapadaniu się drobnych pęcherzyków płucnych. W niniejszym badaniu wykazano, że komórki wydzielnicze w drogach oddechowych myszy nie są jednorodne. Zamiast tego są zorganizowane w płynne gradienty od części bliższej gardłu (proksymalnej) do głębokich partii płuca (dystalnej), a kluczowa ścieżka sygnałowa, nazwana FGFR2b, pomaga tworzyć i utrzymywać te stopniowe różnice w tożsamości i funkcji komórek. Zrozumienie tego ukrytego porządku daje wgląd w to, jak płuca pozostają zdrowe i co może pójść nie tak w przewlekłych chorobach płuc.
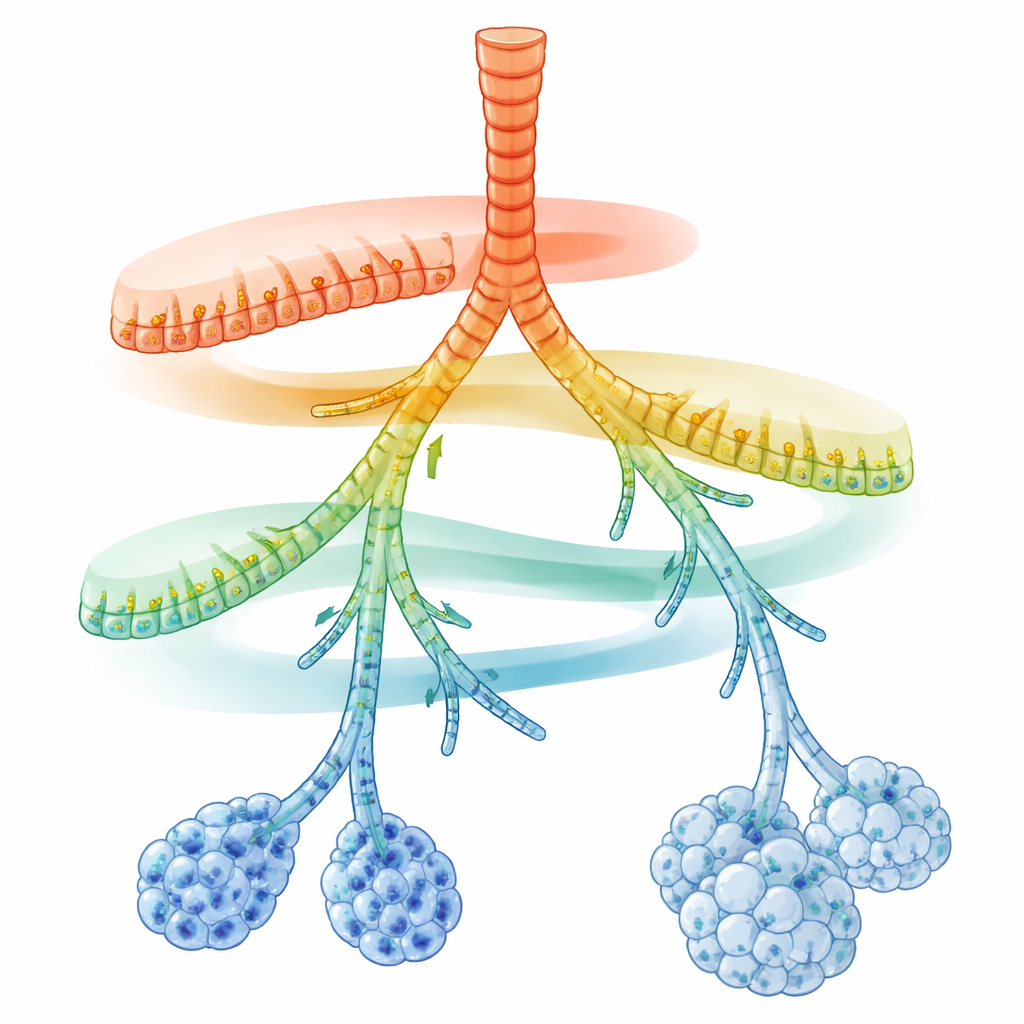
Ukryta mapa wzdłuż rur oddechowych
Naukowcy skupili się na komórkach wydzielniczych, które wyściełają przewody oddechowe i wydzielają śluz, peptydy przeciwdrobnoustrojowe oraz surfaktant. Korzystając z pojedynczokomórkowego sekwencjonowania RNA, odczytali aktywne geny w tysiącach pojedynczych komórek z dorosłych płuc mysich. Po odwzorowaniu tych komórek na mapie podobieństw molekularnych komórki wydzielnicze nie rozdzieliły się na kilka sztywnych typów. Zamiast tego utworzyły ciągły łańcuch stanów łączący duże drogi oddechowe z drobnymi pęcherzykami. Obok wspólnego programu do detoksykacji wdychanych chemikaliów pojawiły się dwa przeciwstawne gradienty aktywności genów: w pobliżu większych dróg oddechowych najsilniejsze były geny związane z szybką, wrodzoną obroną immunologiczną; w kierunku najbardziej odległych rozgałęzień i pęcherzyków dominowały geny związane z gospodarką lipidową, produkcją surfaktantu i prezentacją antygenów.
Od jednego punktu wyjścia do wielu wyspecjalizowanych stanów komórkowych
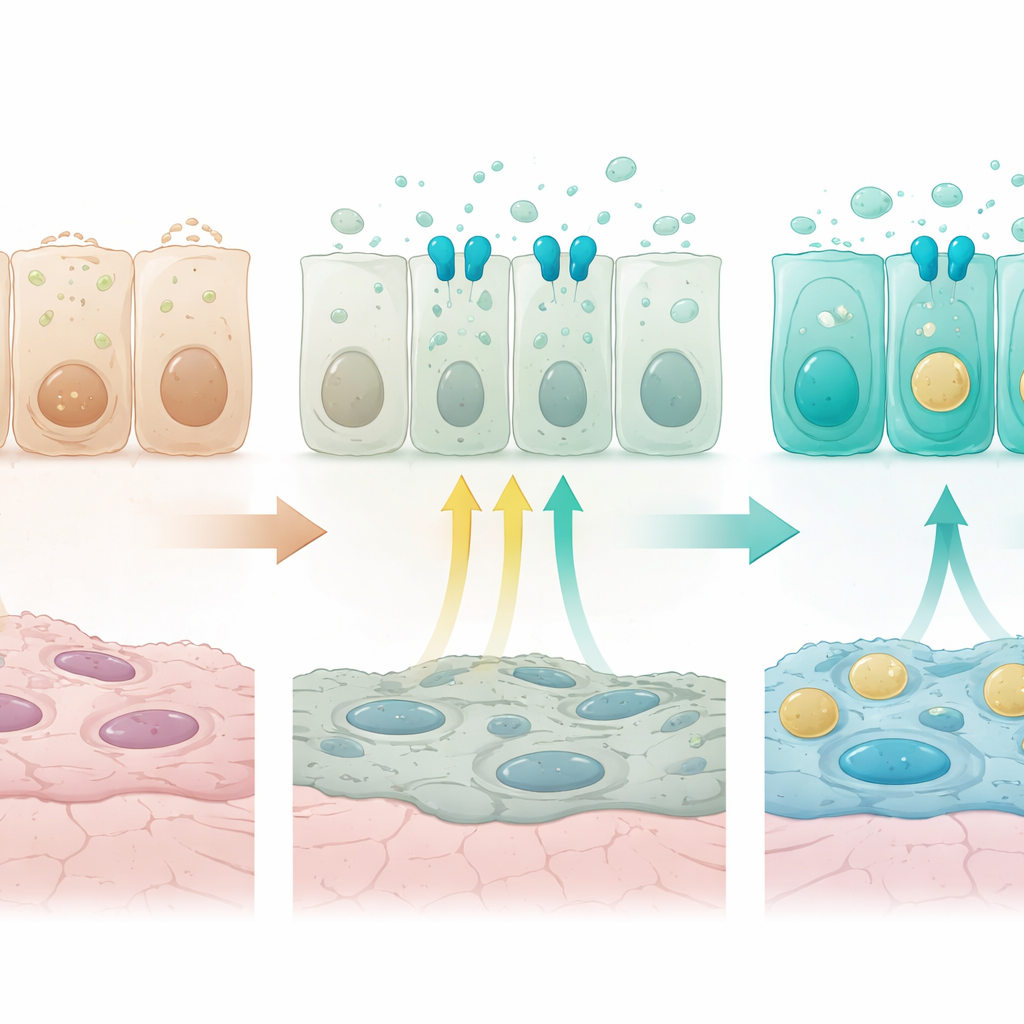
Aby sprawdzić, jak powstaje ten wzór, zespół znakował prekursorowe komórki wydzielnicze pod koniec życia płodowego i śledził ich potomstwo we wczesnym okresie po urodzeniu, używając znakowania linii komórkowych i analizy pojedynczych komórek. Te oznakowane komórki początkowo tworzyły niematuracyjny pulk z silnym aparatem do syntezy białka i genami związanymi z budową tkanki. Po urodzeniu, gdy zaczęło się oddychanie i kontakt ze środowiskiem zewnętrznym, komórki te stopniowo różnicowały się w kilka dojrzałych grup: proksymalne komórki wydzielnicze bogate w geny obrony wrodzonej, komórki bardziej centralne o sygnaturach rozwojowych i regulacyjnych, komórki podwójnie dodatnie łączące tożsamości oskrzelowe i pęcherzykowe oraz komórki typu II pęcherzyków wyspecjalizowane w produkcji surfaktantu. Program detoksykacji włączał się wcześnie i szeroko, podczas gdy programy odpowiedzialne za odporność wrodzoną i prezentację antygenów pojawiały się później i w określonych regionach, co wskazuje, że cechy komórek wydzielniczych są nabywane w zdefiniowanej sekwencji w czasie.
Jak sygnał wzrostowy kształtuje dystalną tożsamość dróg oddechowych
Główną wskazówką dotyczącą tego, co napędza te gradienty, był receptor zwany FGFR2b, będący częścią ścieżki sygnałowej czynników wzrostu, już wcześniej uznanej za niezbędną dla komórek typu II pęcherzyków. FGFR2b i jego geny docelowe były bardziej aktywne w dystalnych komórkach dróg oddechowych i pęcherzyków niż w komórkach proksymalnych. Gdy badacze wyłączyli FGFR2b specyficznie w komórkach wydzielniczych tuż po urodzeniu, normalny program dystalny osłabł. Spadła ekspresja genów wymaganych do produkcji surfaktantu i transportu pęcherzykowego, podczas gdy wzrosły geny typowe dla płaskich komórek typu I pęcherzyków, składników mitochondrialnych, kanałów jonowych i czynników przeżycia pod stresem. Niektóre komórki pośrednie zaczęły współekspresję umiarkowanych poziomów markerów obrony proksymalnej i dystalnej, skutecznie rozmywając normalny wzorzec przestrzenny. W hodowlach organoidów pochodzących z komórek dróg oddechowych dodanie ligandów FGFR tłumiło markery proksymalnej obrony wrodzonej i zwiększało geny związane z surfaktantem w sposób zgodny z obserwacjami in vivo, potwierdzając, że aktywacja FGFR2b jest wystarczająca, by przesunąć komórki w kierunku dystalnej tożsamości wydzielniczej.
Dostrajanie przez interakcję z innymi sygnałami
Zespół badał także, jak sygnałowanie FGFR2b współdziała z inną ścieżką napędzaną przez VEGFA, znaną przede wszystkim z kształtowania naczyń krwionośnych. W organoidach sam VEGFA mógł osłabić niektóre geny obrony wrodzonej, a blokada jego receptora zmieniała pewne dystalne markery, lecz nie była w stanie w pełni zastąpić FGFR2b. W rzeczywistości utrata FGFR2b in vivo obniżała ekspresję Vegfa, a jednoczesna stymulacja obu ścieżek wywoływała sprzężenie zwrotne obniżające poziomy FGFR2b, co wskazuje na złożony dialog między tymi systemami sygnalnymi. U dorosłych myszy wyłączenie FGFR2b nie przekształcało już dramatycznie gradientów odporności wrodzonej, ale nadal było potrzebne do utrzymania ekspresji kluczowych dystalnych markerów, takich jak gen surfaktantowy Sftpb i klasyczny marker wydzielniczy dróg oddechowych Scgb1a1, oraz do zachowania hybrydowych komórek oskrzelowo–pęcherzykowych.
Dlaczego te gradienty mają znaczenie dla zdrowia płuc
Wyłaniający się obraz przedstawia wyściółkę dróg oddechowych jako precyzyjnie stopniowany krajobraz, a nie mozaikę izolowanych stref. Regiony proksymalne są nastawione na szybką, śluzową obronę, podczas gdy regiony dystalne łączą produkcję surfaktantu z wyspecjalizowaną komunikacją immunologiczną. Sygnałowanie FGFR2b pomaga ustanowić i podtrzymywać tę organizację, szczególnie w kompartmentach dystalnych, promując programy związane z lipidami i pęcherzykami oraz powstrzymując nieodpowiednie cechy przypominające proksymalne. Zakłócenie tych gradientów, czy to przez czynniki genetyczne, środowiskowe, czy chorobowe, może przesunąć równowagę między obroną, detoksykacją i wsparciem wymiany gazowej, przyczyniając się do stanów, w których dystalne drogi oddechowe przyjmują cechy bardziej proksymalne. Ta rama pojęciowa oferuje nowe spojrzenie na choroby płuc polegające na „reorganizacji” drzewa oskrzelowego i może ukierunkować przyszłe strategie przywracania właściwej organizacji komórkowej.
Cytowanie: Sountoulidis, A., Theelke, J., Liontos, A. et al. FGFR signaling establishes spatial gradients of secretory cell identities along the airway proximal-distal axis. Nat Commun 17, 2651 (2026). https://doi.org/10.1038/s41467-026-70842-0
Słowa kluczowe: nabłonek dróg oddechowych, komórki wydzielnicze, sygnałowanie FGFR2b, rozwój płuc, gradienty przestrzenne