Clear Sky Science · pl
Pojedynczy skup molekuł polimerazy RNA II jest trwale związany z aktywnymi genami
Jak komórki włączają geny w silnych seriach
Każda komórka w twoim ciele musi zdecydować, których genów używać i kiedy — często włączając je w krótkich, intensywnych seriach. Przez dekady naukowcy podejrzewali, że enzymy odpowiedzialne za odczyt DNA gromadzą się w maleńkich „ogniskach” w jądrze, by zwiększyć wydajność tego procesu, lecz mechanizm działania tych skupień pozostawał przedmiotem sporów. W tym badaniu, wykorzystując zaawansowane mikroskopy, zajrzano do żywych embrionów muszki owocowej i pokazano, że każdy aktywny gen współdziała z pojedynczym, stabilnym skupiskiem enzymu przepisującego DNA na RNA, a te skupiska zachowują się raczej jak zatłoczone miejsca pracy niż egzotyczne krople „rozdzielonych fazowo” struktur komórkowych.
Małe maszyny czytające genom
Enzym będący w centrum tej historii to polimeraza RNA II, molekularna maszyna przesuwająca się po DNA i kopiująca geny na RNA — pierwszy etap w kierunku syntezy białek. Wcześniejsze badania dawały sprzeczne obrazy: niektóre sugerowały, że polimerazy grupują się w duże, trwałe „fabryki” obsługujące wiele genów naraz, inne zaś obserwowały jedynie krótkotrwałe zgromadzenia kilku cząsteczek. Autorzy skupili się na dramatycznym momencie w wczesnym rozwoju muszki — aktywacji genomu zygotycznego — kiedy cichy embrion nagle włącza tysiące własnych genów. Ten naturalny wzrost aktywności stanowił mocny test do obserwacji, jak cząsteczki polimerazy poruszają się, gromadzą i współdziałają z genami w czasie rzeczywistym.
Obserwowanie pojedynczych cząsteczek w żywym embrionie
Aby śledzić pojedyncze cząsteczki polimerazy, zespół genetycznie znakował jeden z jej rdzeniowych składników białkami fluorescencyjnymi, a następnie użył mikroskopii typu lattice light-sheet i śledzenia pojedynczych cząsteczek, rejestrując ich ruch w 3D z dużą szybkością i łagodnym oświetleniem. Stwierdzili, że w miarę jak embrion wchodzi w główną fazę aktywacji, coraz więcej cząsteczek polimerazy staje się ściśle związanych z DNA, co odpowiada większej liczbie włączanych genów. Poprzez krótkotrwałe blokowanie różnych etapów cyklu transkrypcji za pomocą leków mogli rozdzielić cząsteczki dopiero rozpoczynające pracę przy genie od tych aktywnie przemieszczających się wzdłuż niego. Analiza wykazała, że tworzenie się skupisk zależy od pierwszych kroków włączania genu, podczas gdy aktywne wydłużanie transkryptu ma tendencję do osłabiania i skracania czasu trwania skupisk.
Skupiska zmieniające charakter w toku rozwoju
Obrazowanie całych jąder w czasie ujawniło dziesiątki małych skupisk polimerazy na długo przed falą aktywacji obejmującą cały genom, przy czym ich liczba i rozmieszczenie zmieniały się, gdy podziały jądrowe zwalniały. Wczesne stadia rozwoju cechowały się tym, że wiele skupisk utrzymywało się niemal tak długo, jak przerwa między podziałami komórkowymi, co sugeruje, że dominowały w nich polimerazy w wczesnym, „zaczepionym” stanie, które często nie doprowadzały do powstania pełnych cząsteczek RNA. Później, gdy transkrypcja przyspiesza, skupiska stają się bardziej dynamiczne: ich żywotność przestaje prostolinijnie podążać za cyklem komórkowym, a ich wewnętrzny skład przesuwa się w stronę polimeraz faktycznie elongujących geny. Inne pomiary ruchu molekuł wewnątrz i na zewnątrz skupisk wskazują, że w pobliżu aktywnych genów cząsteczki polimerazy są bardziej ograniczone i częściej wracają do tych samych miejsc, co wspiera obraz lokalnie zatłoczonego pola pracy, a nie luźnej, płynnej kropli.
Jedno skupisko, jeden gen podczas impulsu transkrypcyjnego
Aby powiązać skupiska bezpośrednio z produkcją genu, badacze śledzili konkretne geny raportowe, które świecą tam, gdzie powstaje nowy RNA, jednocześnie rejestrując polimerazę. Dla kilku różnych genów konsekwentnie obserwowano tylko jedno skupisko polimerazy przy każdej aktywnej kopii genu w trakcie impulsu transkrypcyjnego. Intensywność skupiska rosła i malała synchronicznie z ilością świeżo powstającego RNA, a gdy możliwe było rozdzielenie zdublowanych kopii siostrzanych, każda miała własne, odrębne skupisko, zamiast współdzielić jedno. Symulacje komputerowe, dopasowane do warunków obrazowania, pokazały, że geny z silnym załadunkiem polimerazy tworzą widoczne skupiska, podczas gdy słabsze geny mogą wciąż rekrutować polimerazę, ale pozostawać zbyt słabe sygnałowo, by je wykryć — co tłumaczy, dlaczego tylko mniejszość aktywnych genów pokazuje wyraźne skupiska w mikroskopie.
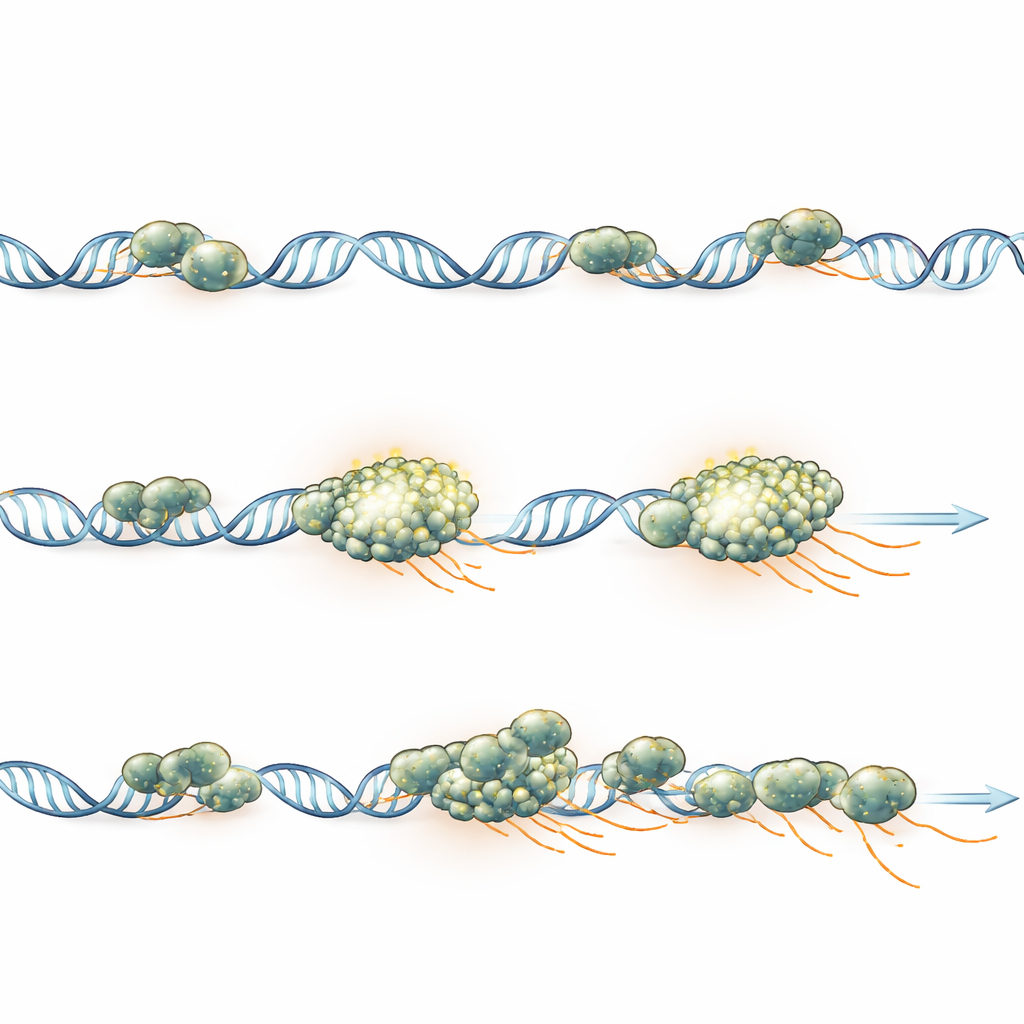
Co to oznacza dla kontroli genów
Praca ta sugeruje, że w tych embrionach skupiska polimerazy głównie odzwierciedlają liczbę enzymów aktywnie zaangażowanych przy pojedynczym genie, a nie istnienie odrębnej „fabryki” czy specjalnej kropli, która musiałaby powstać, by dopuścić transkrypcję. Skupisko pojawia się, gdy wiele polimeraz zostaje załadowanych w krótkim czasie, pozostaje trwale związane z tym jednym genem przez cały okres aktywności i stopniowo się rozprasza, gdy polimerazy kończą kopiowanie i odchodzą. Dla czytelnika nietechnicznego kluczowy wniosek jest taki, że włączanie genów organizuje się przez skupione, gen-po-genie centra aktywności: każdy aktywny gen tymczasowo gromadzi własny zespół maszyn kopiujących, a rozmiar i czas trwania tego zespołu odzwierciedlają bezpośrednio siłę włączenia genu.
Cytowanie: Mukherjee, A., Kapoor, M., Shankta, K. et al. A single cluster of RNA Polymerase II molecules is stably associated with active genes. Nat Commun 17, 2580 (2026). https://doi.org/10.1038/s41467-026-70775-8
Słowa kluczowe: agregacja polimerazy RNA II, aktywacja genomu zygotycznego, przerywana transkrypcja, regulacja genów w embrionach, mikroskopia pojedynczych cząsteczek