Clear Sky Science · pl
Syntetyczne mechanoreceptory aptamerowe pozwalają na rozpoznawanie sił specyficznych dla komórek i kontrolę czasową za pomocą układów DNA
Słuchanie komórek przez delikatne pociągnięcia
W naszych ciałach komórki nieustannie popychają i ciągną otoczenie, wykorzystując drobne siły do decydowania, kiedy rosnąć, przemieszczać się lub zmieniać funkcję. W tej pracy opisano nowy sposób podsłuchu tych sił za pomocą urządzeń opartych na DNA, które można dostroić do konkretnych typów komórek i włączać bądź wyłączać w czasie. Taka technologia mogłaby w przyszłości pomóc inżynierom prowadzić wzrost tkanek, zrozumieć zachowanie nowotworów albo projektować inteligentne materiały reagujące na żywe komórki w czasie rzeczywistym.
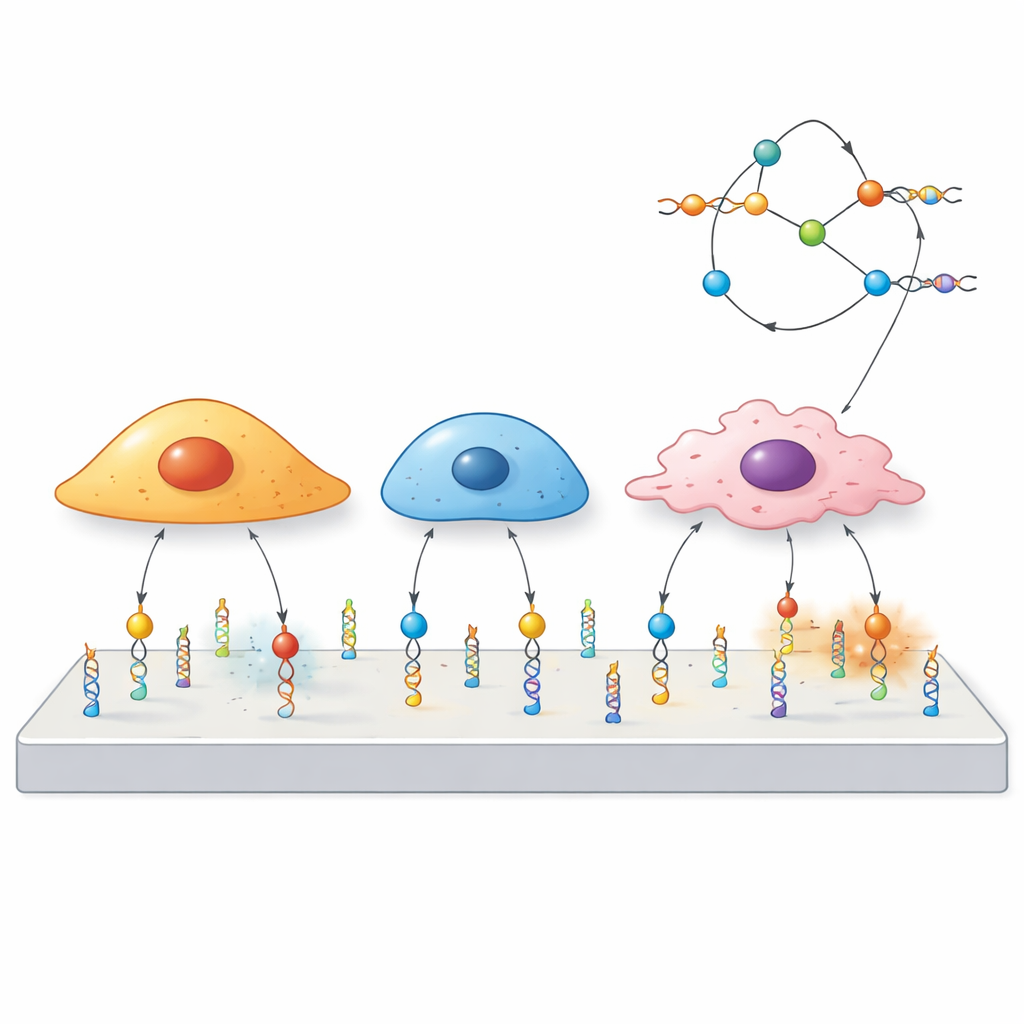
Wykorzystanie DNA jako maleńkiego przełącznika mechanicznego
Naukowcy zbudowali „mechanopróbki” z DNA — tej samej cząsteczki, która przenosi informację genetyczną. Każda sondka składa się z trzech części: krótkiego odcinka DNA zwanego aptamerem, który wiąże wybrany białkowy receptor na powierzchni komórki; sparowanego fragmentu DNA działającego jak sprężyna, zaprojektowanego tak, by rozrywać się przy określonej sile; oraz barwnika fluorescencyjnego, który zaczyna świecić, gdy ta sprężyna pęknie. Gdy komórka pociągnie za receptor związany przez aptamer wystarczająco mocno, helisa DNA się otwiera i sygnał się pojawia. Ponieważ różne aptamery przyczepiają się do różnych receptorów, zespół może z góry zdecydować, które komórki lub białka będą mogły uruchomić sondę.
Odnajdywanie ukrytych dróg przekazywania sił na powierzchni komórek
Większość istniejących sensorów siły koncentruje się na integrynach — dobrze znanych białkach pomagających komórkom chwytać otoczenie, które jednak występują w wielu typach komórek, ograniczając selektywność. W tej pracy zespół zamiast tego celował w „niekanoniczne” receptory, które zwykle nie są uważane za mechaniczne. U pokazali, że aptamer AS1411, który wiąże białko nukleolinę powszechne w komórkach nowotworowych, dawał sygnał tylko wtedy, gdy specyficznie rozpoznawał swój cel. Projektując sondy wymagające słabszych lub silniejszych sił do otwarcia, odkryli, że nukleolina przenosi umiarkowane siły w porównaniu z integrynami i sama w sobie nie pomaga komórkom w rozprzestrzenianiu się po powierzchni. Dla kontrastu aptamer Sgc8, rozpoznający receptor PTK7, mógł raportować siły nawet wtedy, gdy komórki ledwie przylegały, tworząc pierścieniowe wzory sugerujące inny źródło ruchu.
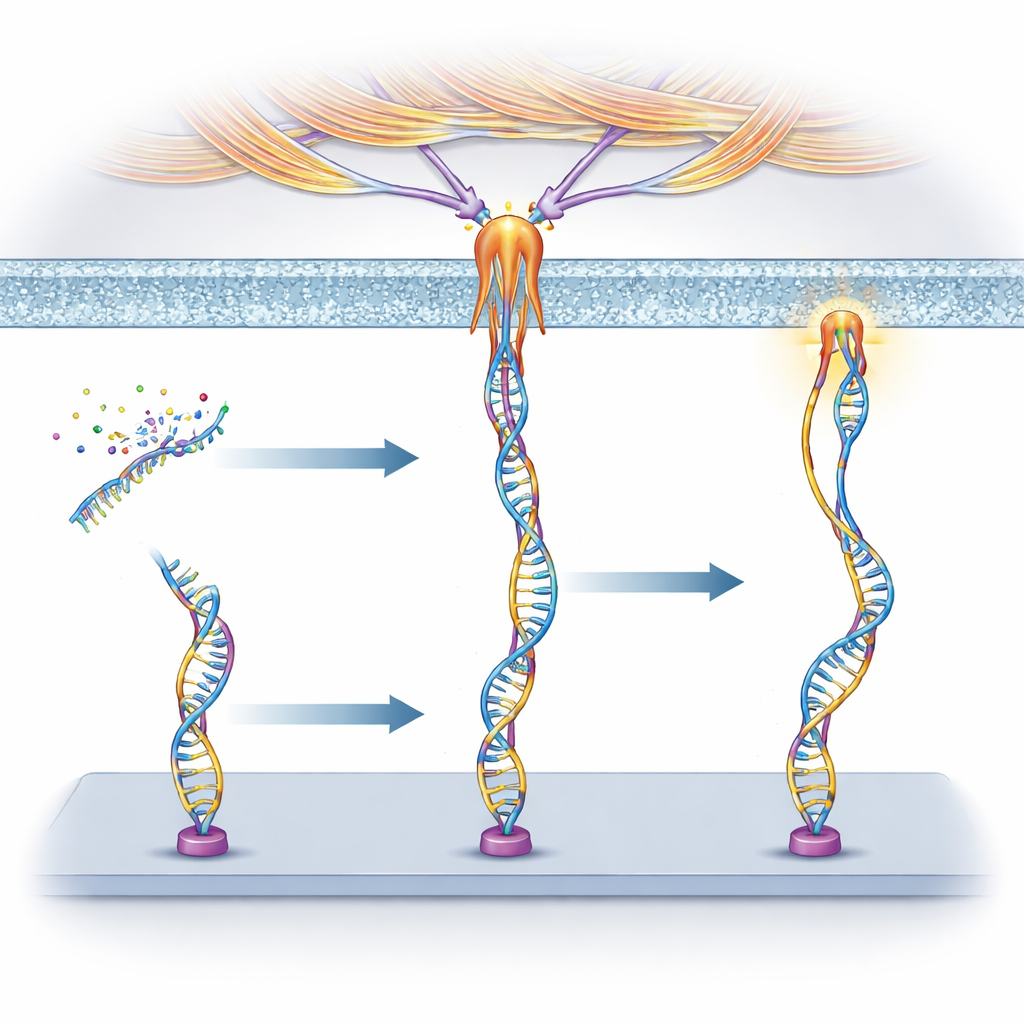
Śledzenie, skąd pochodzą siły
Aby zrozumieć, co ciągnęło te urządzenia DNA, badacze zastosowali leki selektywnie blokujące różne procesy komórkowe. Dla nukleoliny odkryli, że jej siły silnie zależą od miozyny — tego samego białka motorowego, które wspomaga kurczenie mięśni — i pojawiają się w miejscach, gdzie komórka tworzy ogniska adhezyjne — specjalne punkty kontaktu używane do chwytania i wyczuwania sztywności. Sugeruje to, że nukleolina jest pośrednio powiązana z wewnętrznym aparatem aktyna–miozyna komórki i może dzielić jego siły kurczliwe. W przypadku PTK7 jednak blokowanie procesu zwanego makropinocytozą — gdy komórki marszczą błony i zasysają płyn — znacznie zmniejszało sygnały. Siły pochodziły głównie z wczesnego marszczenia się błony napędzanego wzrostem aktyny, a nie z późniejszych etapów zamykania pęcherzyków, co ujawnia odmienną ścieżkę mechaniczną.
Strojenie selektywności komórek z precyzją molekularną
Ponieważ każdy aptamer rozpoznaje konkretny receptor powierzchniowy, ta sama rusztowanie DNA może zostać przeprogramowane po prostu przez zamianę jednego aptameru na inny. Zespół zademonstrował to, stosując sondy dla trzech różnych celów — PTK7, mucyn-1 i EpCAM — w panelu linii komórek nowotworowych o wysokim lub niskim poziomie każdego białka. Komórki bogate w dany receptor generowały silne sygnały, podczas gdy te z niewielką ilością receptora słabo reagowały, nawet gdy były wymieszane w tym samym naczyniu. Co uderzające, komórki dzielące ten sam receptor mogły nadal wykazywać różne wzory przestrzenne sił, podkreślając, że przepływ siły przez receptor zależy nie tylko od jego obecności, ale też od wewnętrznego okablowania każdego typu komórki.
Programowanie, kiedy komórkom wolno ciągnąć
Wykorzystując fakt, że aptamery są zbudowane z DNA, badacze połączyli swoje sondy z sieciami reakcji DNA, które kontrolują, czy aptamer w ogóle może się związać. Komplementarne nici „blokujące” mogą tymczasowo ukryć aptamer, a nici „aktywujące” mogą następnie usunąć blokery przez reakcję wymiany nici, przywracając czułość na siłę. Zaprojektowali też blokera opartego na RNA, który może być przecięty przez enzym RNaza H, i dalszo spowolnili to cięcie za pomocą cząsteczek wabików konkurujących o enzym. W ten sposób przemienili mechanoczułość w program z opóźnieniem: komórki mogły generować sygnały dopiero po wbudowanym czasie opóźnienia lub w wybranych oknach czasowych.
Dlaczego to ma znaczenie dla przyszłych materiałów żywych
Mówiąc prościej, ta praca przemienia DNA w inteligentny zamek mechaniczny, który otwiera się tylko dla określonych komórek, tylko przy określonych siłach i tylko w wybranych momentach. Pokazując, że mniej oczywiste receptory, takie jak nukleolina i PTK7, mogą przekazywać informacje mechaniczne przez bardzo różne szlaki wewnątrz komórek, poszerza nasz obraz tego, jak komórki „czują” swoje otoczenie. Ponieważ cały system zbudowano z kwasów nukleinowych, można go bezpośrednio podłączyć do szybko rozwijającego się zestawu narzędzi układów DNA i nanourządzeń. Tworzy to fundament dla materiałów i inżynierowanych tkanek, które nie tylko wykrywają, kiedy komórki popychają lub ciągną, ale także reagują starannie zaprogramowanymi działaniami biochemicznymi, potencjalnie kierując gojeniem, wzrostem lub leczeniem nowotworów w wysoce programowalny sposób.
Cytowanie: Xu, T., Sethi, S., Drees, C. et al. Synthetic aptamer mechanoreceptors enable cell-specific force sensing and temporal control via DNA circuits. Nat Commun 17, 2492 (2026). https://doi.org/10.1038/s41467-026-70765-w
Słowa kluczowe: mechanotransdukcja, aptamery DNA, mechanika komórek, biologia syntetyczna, sieci reakcji DNA