Clear Sky Science · pl
Frazzled/DCC kieruje przestrzenną integracją progenitorów, zapewniając stały obrót jelit
Jak jelito cicho się odnawia
Każdego dnia komórki wyściełające nasze jelita ulegają zużyciu i muszą zostać wymienione, a mimo to narząd zachowuje kształt i rozmiar z niezwykłą precyzją. To badanie, wykorzystujące muszkę owocową jako model, ujawnia ukryty system kierowania, który mówi nowo powstałym komórkom jelita dokładnie, dokąd mają się udać, by załatać drobne ubytki w nabłonku. Zrozumienie tej „kontroli ruchu komórek” nie tylko wyjaśnia, jak zdrowe tkanki utrzymują swoje funkcje, lecz także rzuca światło na to, jak podobne sygnały kierunkowe mogą zostać wykorzystane podczas rozprzestrzeniania się nowotworu.
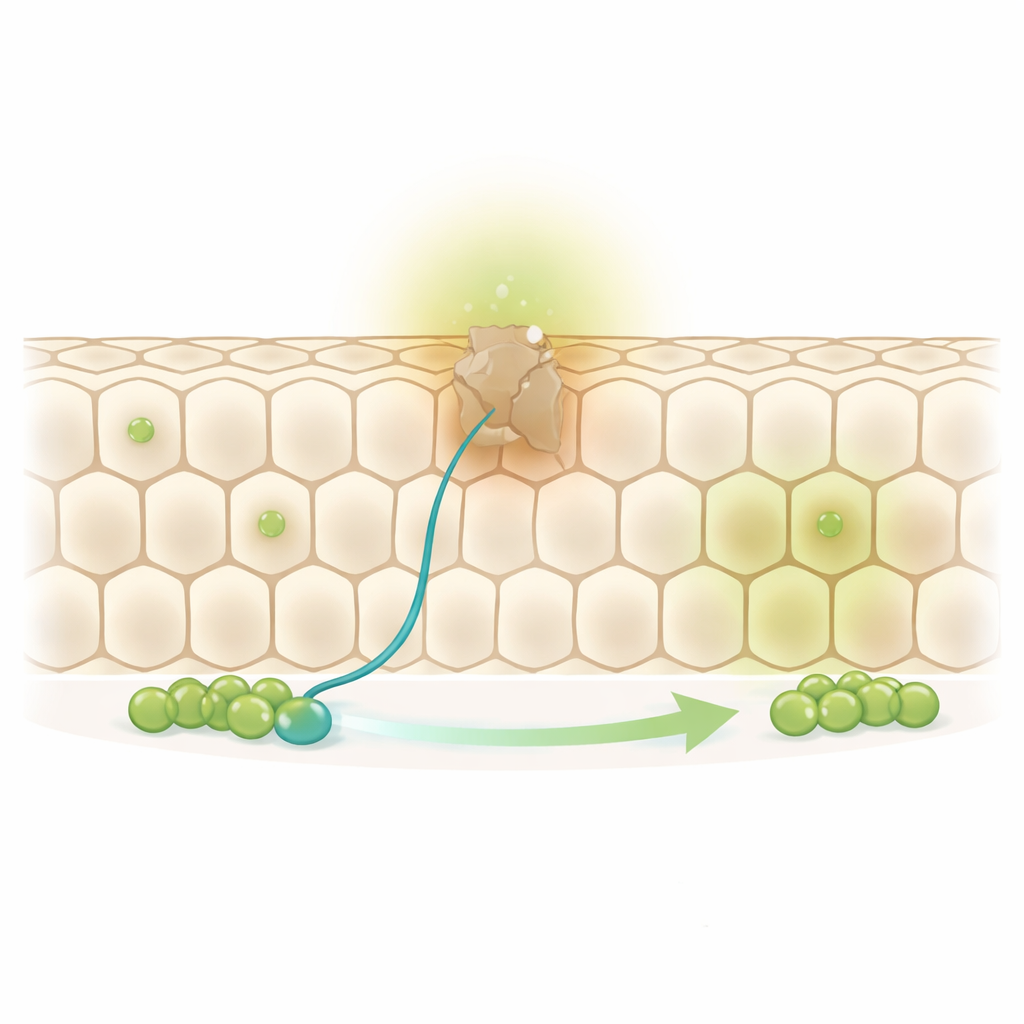
Plaster miodu w ciągłym ruchu
Środkowe jelito muszki jest pokryte pojedynczą warstwą dużych komórek wchłaniających ułożonych jak plaster miodu. U podstawy tego arkusza leżą rozproszone komórki macierzyste i ich bezpośrednie córki, zwane progenitorami. Gdy stara komórka wchłaniająca dobiega końca życia, komórka macierzysta dzieli się, a jej córka-progenitor ostatecznie zastępuje zużytą sąsiadkę. Autorzy zauważyli jednak, że około jednej trzeciej komórek w tym „plastrze” nie ma bezpośrednio obok siebie komórki macierzystej ani progenitora. Rodziło to pytanie: jak te „poza zasięgiem” komórki są odnawiane bez pozostawiania dziur w barierze?
Nowe komórki w ruchu
Śledząc pojedyncze zdarzenia wymiany przez tydzień, badacze stwierdzili, że te odległe komórki są odnawiane równie często jak te położone tuż obok komórki macierzystej. To sugeruje, że progenitory muszą się przemieszczać. Zgodnie z tym zespoł zaobserwował, że progenitory wydłużają długie, cienkie wypustki—czuciowe „wąsy”—częściej i dalej niż same komórki macierzyste. Te wypustki nie są losowe: w normalnych warunkach wskazują głównie w kierunku starszych, nieodnawianych sąsiadów, a nie świeżo odnowionych, co sugeruje aktywne zachowanie poszukiwawczo-ratunkowe skierowane ku komórkom najbardziej potrzebującym wymiany.
Neuronowy sygnał przewodzenia wykorzystany w jelicie
Aby zrozumieć, jak te wypustki są sterowane, autorzy zwrócili się ku rodzinie cząsteczek najlepiej znanej z prowadzenia połączeń nerwowych: netrynom i ich receptorom Frazzled/DCC oraz Unc-5. W układzie nerwowym netryny działają jak długozasięgowe sygnały przyciągające lub odpychające rosnące włókna nerwowe. W jelicie muchy zespół wykazał, że receptory Frazzled/DCC i Unc-5 znajdują się specyficznie na komórkach progenitorowych, skoncentrowane w ich wypustkach. Z kolei zużyte komórki wchłaniające zaczynają produkować i uwalniać netrynę nazwaną Netrin-B. Gdy badacze zwiększyli poziom Netrin-B w wybranych komórkach, pobliskie progenitory wydłużyły wypustki skierowane w stronę źródła, a następnie przemieściły się, by zająć to miejsce. Gdy zablokowali Netrin-B lub wyłączyli Frazzled, wypustki się skróciły, odległe komórki nie były już efektywnie zastępowane, a muchy umierały wcześniej, co podkreśla wagę tego mechanizmu dla zdrowia jelita.
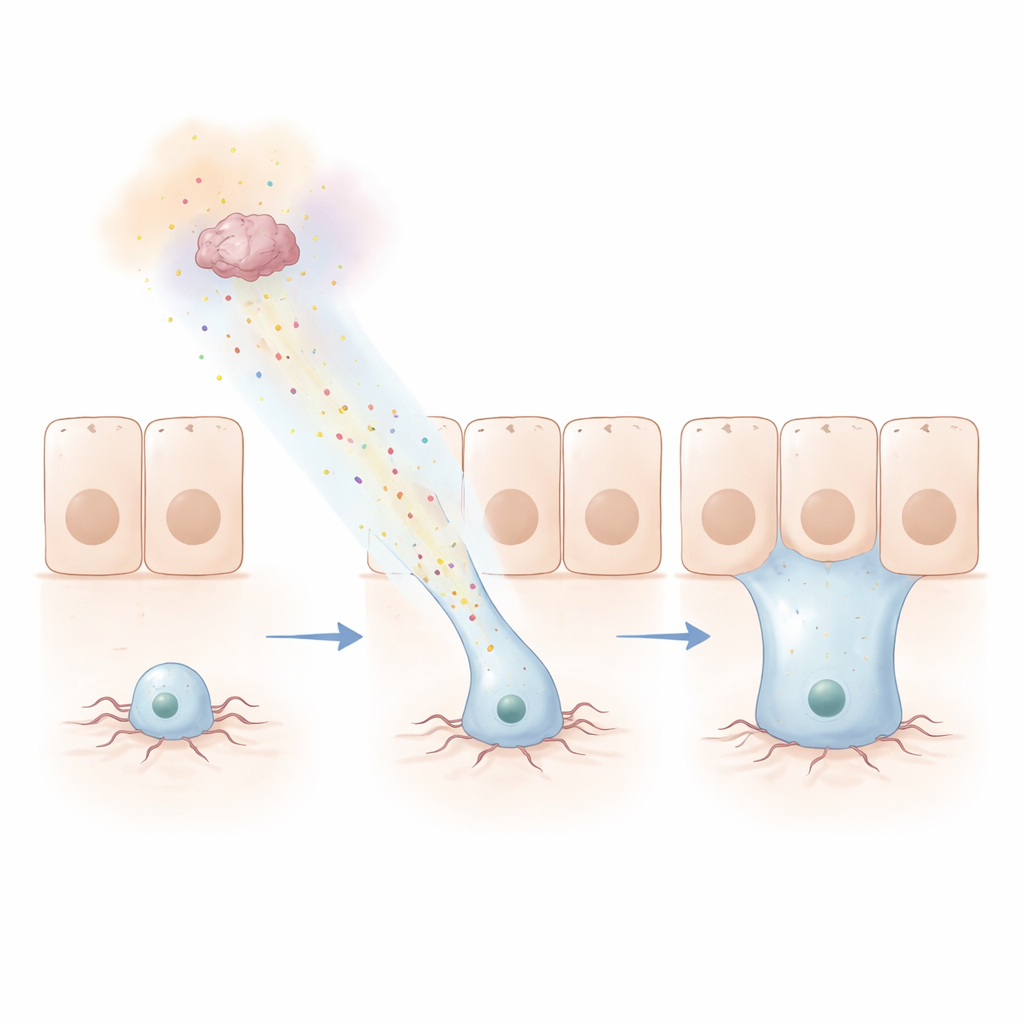
Podążając za chemicznym śladem
Aby zbadać, jak daleko ten sygnał może docierać, zespół skonstruował sprytne sito „Hamelin”, nazwane na cześć Szczurołapa z Hameln. Stworzyli pierścień komórek na styku regionów jelita wydzielających netryny, jednocześnie fluorescencyjnie znakując progenitory w pewnej odległości. W ciągu kilku dni progenitory migrowały na odległość sięgającą dziesiątek mikrometrów w kierunku źródła, przekraczając nawet ostry graniczny pas i integrując się w innej warstwie tkanki. Ludzkie wersje netryn i receptora DCC mogły zastąpić muchowe odpowiedniki i nadal kierować tymi ruchami, co pokazuje, że mechanizm jest głęboko zachowany ewolucyjnie. Ten sam aparat aktyny, który napędza ruch komórek w innych częściach ciała, okazał się niezbędny: po usunięciu kluczowych elementów wypustki i dalekozasięgowe odnawianie zawodziły.
Dlaczego to ma znaczenie dla zdrowia i chorób
Mówiąc prosto, praca ta ukazuje, że jelito nie polega jedynie na lokalnym ciśnieniu podziałów komórkowych, by odnawiać wyściółkę. Zamiast tego umierające komórki wysyłają chemiczny sygnał „pomocy”, Netrin-B, który przyciąga specyficzne progenitory wyposażone w receptory Frazzled/DCC. Te progenitory wydłużają czuciowe wypustki wzdłuż gradientu, pełzają w stronę starzejącej się komórki i wpasowują się na jej miejsce, utrzymując barierę nienaruszoną. Ponieważ ten sam system Netrin–DCC działa u ssaków i wiązany jest z inwazją oraz przerzutami nowotworowymi, obserwacje z muchy dostarczają konkretnego mechanistycznego wsparcia dla postrzegania tych cząsteczek jako posiadających dwie strony: niezbędnych do uporządkowanej naprawy w zdrowej tkance, lecz potencjalnie niebezpiecznych, gdy są źle regulowane w guzach, które uczą się poruszać i kolonizować nowe narządy.
Cytowanie: Zipper, L., Ramon-Cañellas, P., Akkas-Gazzoni, F. et al. Frazzled/DCC directs spatial progenitor integration ensuring steady-state intestinal turnover. Nat Commun 17, 2491 (2026). https://doi.org/10.1038/s41467-026-70704-9
Słowa kluczowe: komórki macierzyste jelita, migracja komórek, sygnalizacja netrynowa, homeostaza tkankowa, przerzuty nowotworowe