Clear Sky Science · pl
Miocyfrowy aktywator z zaprojektowaną biofizyką dla wszczepialnych systemów biohybrydowych
Przekształcanie mięśni w inteligentne żywe maszyny
Wyobraźcie sobie, że lekarze mogliby przekształcić własny mięsień pacjenta w żywy napęd, który nigdy się nie męczy, można nim sterować za pomocą komputera i który bezpiecznie może leżeć obok wrażliwych narządów przez lata. W tym badaniu opisano sposób, by to osiągnąć. Naukowcy konstruują „mioneuralny aktywator” u szczurów — mięsień, którego okablowanie nerwowe zostało celowo przearanżowane tak, by można nim było kierować elektroniką, by odporność na zmęczenie była zwiększona, a jednocześnie by zachowywał się jak naturalna tkanka. Takie żywe aktywatory mogłyby w przyszłości przywracać ruch, wspierać niewydolne narządy lub dostarczać realistyczne odczucia z zaawansowanych protez kończyn.
Dlaczego żywe mięśnie są lepszymi silnikami
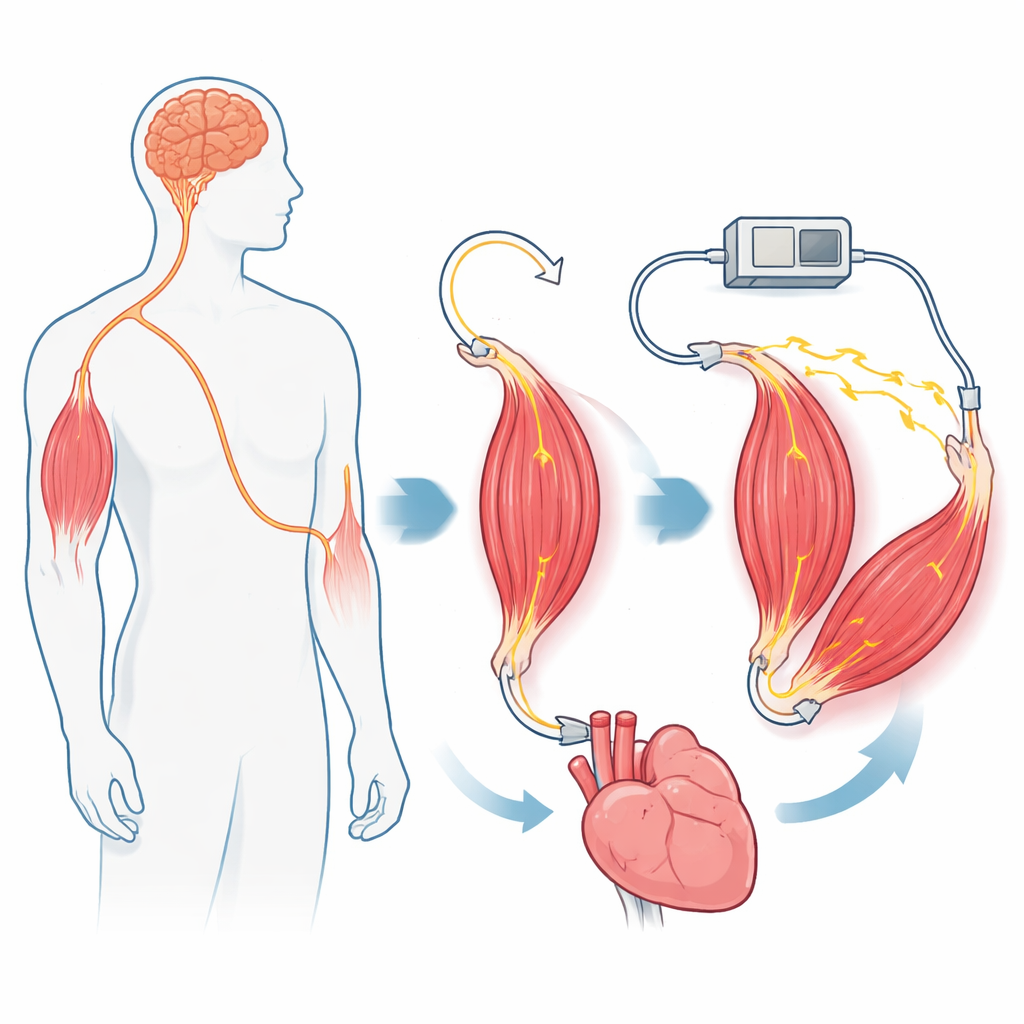
Sztuczne silniki zasilane prądem, sprężonym powietrzem czy płynami są wydajne, lecz są ciężkie, trudno je zmniejszyć do rozmiarów kompatybilnych z ciałem i wykonane z materiałów, które słabo integrują się z tkanką żywą. W przeciwieństwie do nich mięsień szkieletowy jest lekki, energooszczędny, samoregenerujący się i już zaprojektowany do pracy wewnątrz ciała. Może rosnąć, adaptować się i reagować na maleńkie sygnały nerwowe. Jednak gdy mięśnie są bezpośrednio sterowane impulsami elektrycznymi z wszczepionego urządzenia, szybko się męczą. To zmęczenie wynika z faktu, że standardowa stymulacja elektryczna zwykle najpierw rekrutuje największe, najszybsze, ale najmniej trwałe włókna. Aby wykorzystać mięsień jako niezawodny, wszczepialny napęd, zespół musiał zmienić to, jak jego włókna nerwowe są zorganizowane i rekrutowane — nie rezygnując przy tym ze zdrowia i trwałości mięśnia.
Zmiana dróg nerwowych, by przepisać kontrolę
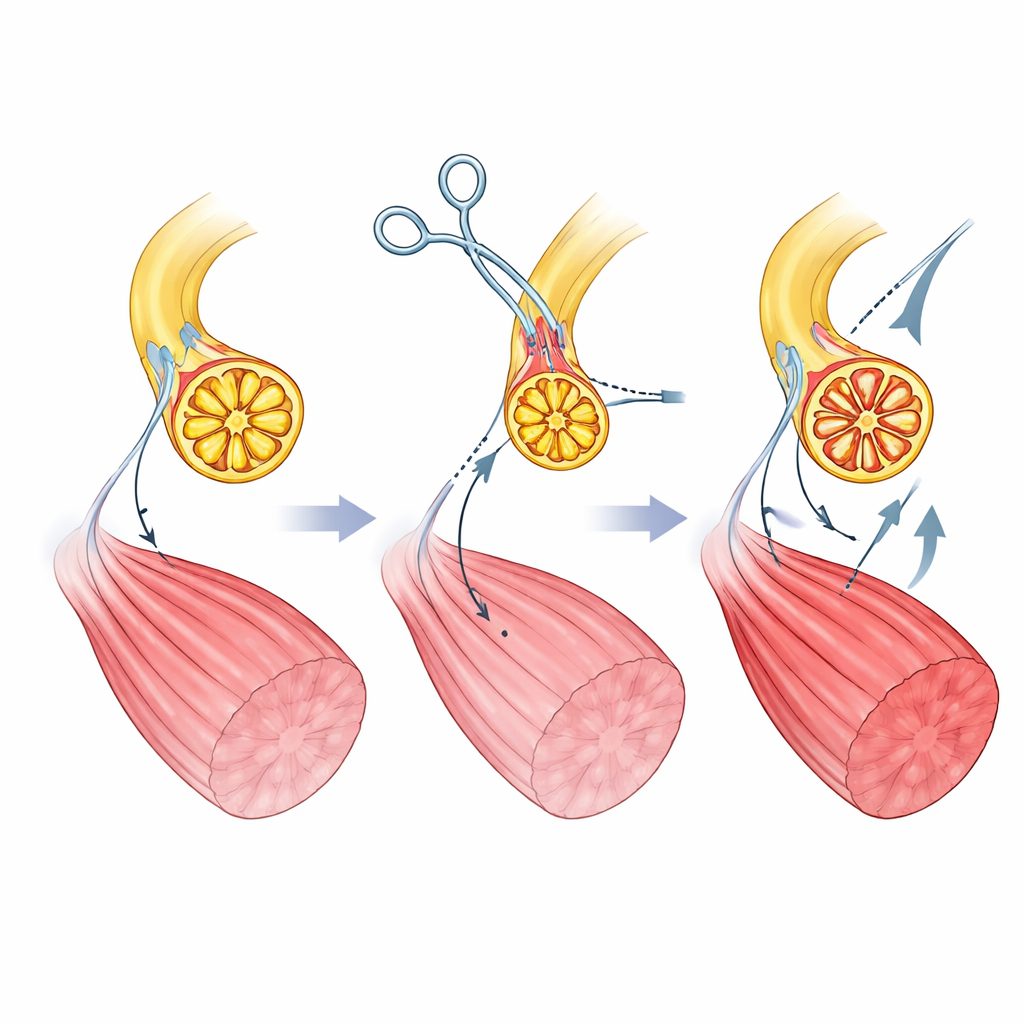
Autorzy tworzą swój mioneuralny aktywator u szczurów, chirurgicznie przekierowując unerwienie mięśnia kończyny. Najpierw przecinają normalny nerw ruchowy przenoszący polecenia z rdzenia kręgowego i uniemożliwiają mu odrost. Następnie prowadzą inny nerw — zwykle przenoszący sygnały dotyku i rozciągania ze skóry i tkanek — bezpośrednio do mięśnia. Z czasem ten „czuciowy” nerw regeneruje się wewnątrz mięśnia i tworzy nowe punkty kontaktowe z włóknami mięśniowymi. Mikroskopia pokazuje, że te nowe złącza wyglądają i działają jak normalne połączenia motoryczne, a mięsień odzyskuje zdolność do kurczenia się po stymulacji elektrycznej nerwu czuciowego. Co istotne, aksony w tym nerwie czuciowym są bardziej jednorodne i mniejsze niż w pierwotnym nerwie ruchowym, co tworzy podstawę do bardziej zrównoważonej rekrutacji włókien mięśniowych pod kontrolą komputera.
Mięśnie, które działają, gdy są mocno obciążone
Gdy przearanżowane mięśnie wygoiły się, zespół poddał je wymagającym testom. Porównywali mięśnie rodzime z nowymi aktywatorami podczas powtarzanych pojedynczych skurczów i długotrwałych okresów ciągłego skurczu. Mioneuralne aktywatory tracą siłę znacznie wolniej i wykazują stabilniejszą wydajność w czasie, z 260-procentową poprawą odporności na zmęczenie przy pracy ciągłej. Ich zachowanie przez kolejne minuty było zasadniczo inne niż mięśni niezmodyfikowanych: zamiast szybkiego spadku siły, siła malała stopniowo, a potem stabilizowała się. Pomimo utraty części masy w trakcie przearanżowania, aktywatory zachowały zdrową strukturę włókien i generowały podobną siłę na jednostkę masy co mięsień rodzimy, utrzymując swój stan przez co najmniej 15 tygodni nawet bez ćwiczeń czy dodatkowej stymulacji.
Sterowanie komputerowe bez zakłócania mózgu
Ponieważ nowe okablowanie nerwowe odłącza mięsień od normalnych sygnałów ruchowych mózgu, wszystkie skurcze pochodzą teraz z zewnętrznego stymulatora. Badacze osadzają mięsień w pętli sprzężenia zwrotnego: czujnik mierzy siłę, regulator dostosowuje stymulację nerwu, a system utrzymuje wybrany docelowy poziom siły przez wiele cykli. Mięśnie rodzime szybko zawodzą w takim układzie, natomiast mioneuralne aktywatory nadal realizują polecenia. Aby zwiększyć bezpieczeństwo i elastyczność systemu, zespół wprowadza też odwracalny „blok nerwowy”. Poprzez przykładanie sygnału elektrycznego o wysokiej częstotliwości na nerw bliżej rdzenia kręgowego, zapobiegają wysyłaniu przez impulsy stymulacyjne niechcianych sygnałów z powrotem do ośrodkowego układu nerwowego, jednocześnie pozwalając stronie mięśniowej na reakcję. W testach aktywator kontynuował generowanie kontrolowanych sił, podczas gdy mózg pozostawał skutecznie odizolowany od sztucznej stymulacji.
Od bionicznych kończyn do wspierania niewydolnych narządów
Aby pokazać możliwe zastosowania tego żywego napędu, autorzy zbudowali dwa systemy demonstracyjne u szczurów. W pierwszym sprzężono aktywator szeregowo z innym mięśniem pełniącym rolę pozostałego mięśnia przy kikucie po amputacji. Poprzez napinanie lub rozluźnianie tej pary zmieniają rozciągnięcie mięśnia resztkowego, a w konsekwencji aktywność jego czuciowych włókien nerwowych — zasadniczo regulując w górę lub w dół czucie położenia i siły kończyny. Ten „proprioceptywny mechanoneuralny interfejs” mógłby w przyszłości dostarczać naturalnie odczuwalnego sprzężenia zwrotnego z protez robotycznych lub wirtualnych awatarów. W drugim systemie owijają aktywator wokół pętli jelita cienkiego wypełnionej płynem. Pod wpływem stymulacji nerwowej mięsień ściska i rozluźnia odcinek jelita, a śledzenie ruchu pokazuje, że organ porusza się zgodnie z aktywatorem. To sugeruje przyszłe urządzenia, które mogłyby wzmacniać mechanicznie osłabione narządy, takie jak jelito, pęcherz, a nawet serce.
Co to może znaczyć dla medycyny przyszłości
Podsumowując, praca ta pokazuje, że przez staranne przekierowanie nerwów własny mięsień człowieka może zostać przekształcony w odporny na zmęczenie, sterowany komputerowo aktywator, który nadal zachowuje cechy tkanki rodzimej i może być elektrycznie odizolowany od mózgu w razie potrzeby. Ponieważ podejście opiera się na technikach chirurgicznych i elektrodach podobnych do istniejących narzędzi klinicznych, może być prostsze do wdrożenia niż całkowicie syntetyczne implanty czy hodowane w laboratorium tkanki. Jeśli podobne mioneuralne aktywatory można bezpiecznie zbudować i kontrolować u ludzi, mogłyby stać się trzonem nowych systemów biohybrydowych przywracających czucie kończyn, wspomagających niewydolne narządy i dostarczających precyzyjnych wskazówek mechanicznych dla ciała bez ciężaru i sztywności tradycyjnych maszyn.
Cytowanie: Song, H., Herrera-Arcos, G., Friedman, G.N. et al. A myoneural actuator with engineered biophysics for implantable biohybrid systems. Nat Commun 17, 2584 (2026). https://doi.org/10.1038/s41467-026-70626-6
Słowa kluczowe: aktywator biohybrydowy, neuroprotetyka, zmęczenie mięśni, regeneracja nerwów, wsparcie narządów