Clear Sky Science · pl
Oddzielenie efektów elektronowych i geometrycznych w katalizatorach Pd poprzez termiczną rekonstrukcję powierzchni dla selektywnej hydrogenacji
Wykorzystanie ciepła jako narzędzia czystszej chemii
Chemicy polegają na katalizatorach stałych przy wytwarzaniu wszystkiego, od leków po tworzywa sztuczne, jednak drobne cząstki metali wykonujące pracę są złożone i kapryśne. W tym badaniu autorzy pokazują, jak prosty zabieg termiczny może przekształcić i „przełączyć” cząstki palladu, dzięki czemu hydrogenują alkiny — ważną klasę bloków budulcowych — znacznie wydajniej i selektywniej. Ucząc się, jak kontrolować zarówno kształt, jak i właściwości elektronowe tych cząstek, dostarczają mapy drogowej do bardziej ekologicznych reakcji przemysłowych z mniejszą ilością niepożądanych produktów ubocznych.
Dlaczego kształt i ładunek katalizatora mają znaczenie
Na powierzchni katalizatora stałego atomy układają się w krajobraz tarasów, krawędzi i narożników. To, gdzie cząsteczka się adsorbuje w tym krajobrazie, często decyduje o przebiegu reakcji. Równocześnie charakter elektronowy powierzchni — to, czy atomy metalu są bogate czy ubogie w elektrony — kontroluje, jak silnie cząsteczki przywierają i jak łatwo wiązania są łamane lub tworzone. W rzeczywistych katalizatorach czynniki geometryczne i elektronowe zazwyczaj są ze sobą powiązane, co utrudnia określenie, który z nich jest rzeczywistą przyczyną lepszych własności. Rozdzielenie ich jest kluczowe, jeśli chcemy projektować katalizatory celowo, a nie metodą prób i błędów.
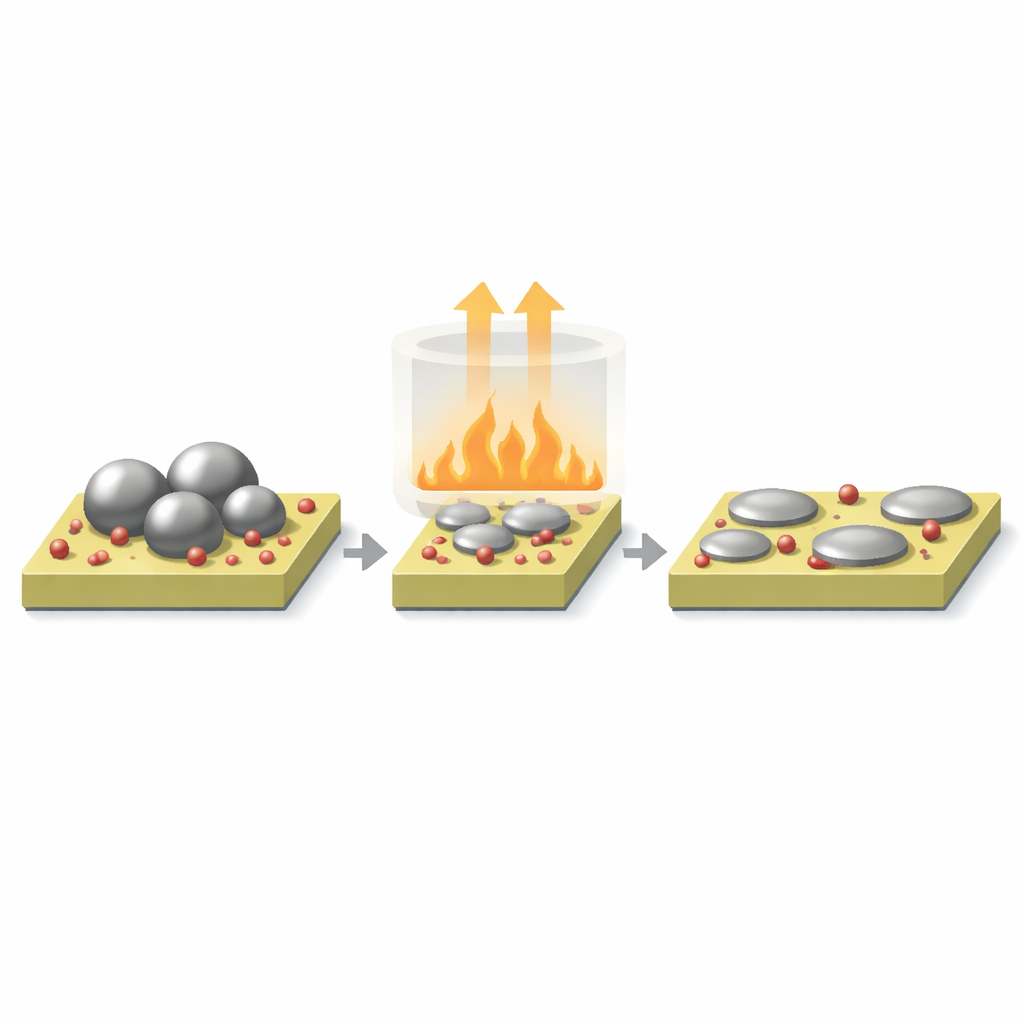
Wykorzystanie ciepła do przekształcenia palladu na cerii
Zespół skupił się na cząstkach palladu osadzonych na tlenku ceru, tak zwanym redukowalnym tlenku, który może wymieniać tlen z metalami na swojej powierzchni. Podgrzewając te materiały w powietrzu w kontrolowanych temperaturach, wywołali proces zwany rekonstrukcją powierzchni. Większe, w przybliżeniu sferyczne nanocząstki palladu rozpadały się i rozlewały w znacznie bardziej płaskie, „kałużowe” wysepki nawiązujące bliższy kontakt z nośnikiem. Równocześnie elektrony przepływały z palladu do tlenku ceru, pozostawiając wiele powierzchniowych atomów palladu nieco ubogich w elektrony. Mikroskopia, adsorpcja gazów i pomiary rentgenowskie potwierdziły, że ogrzewanie tworzyło wysoce zdyspergowane, spłaszczone struktury palladu ze silnymi interakcjami metal‑nośnik.
Powiązanie kształtu z szybkością i siłą wiązania
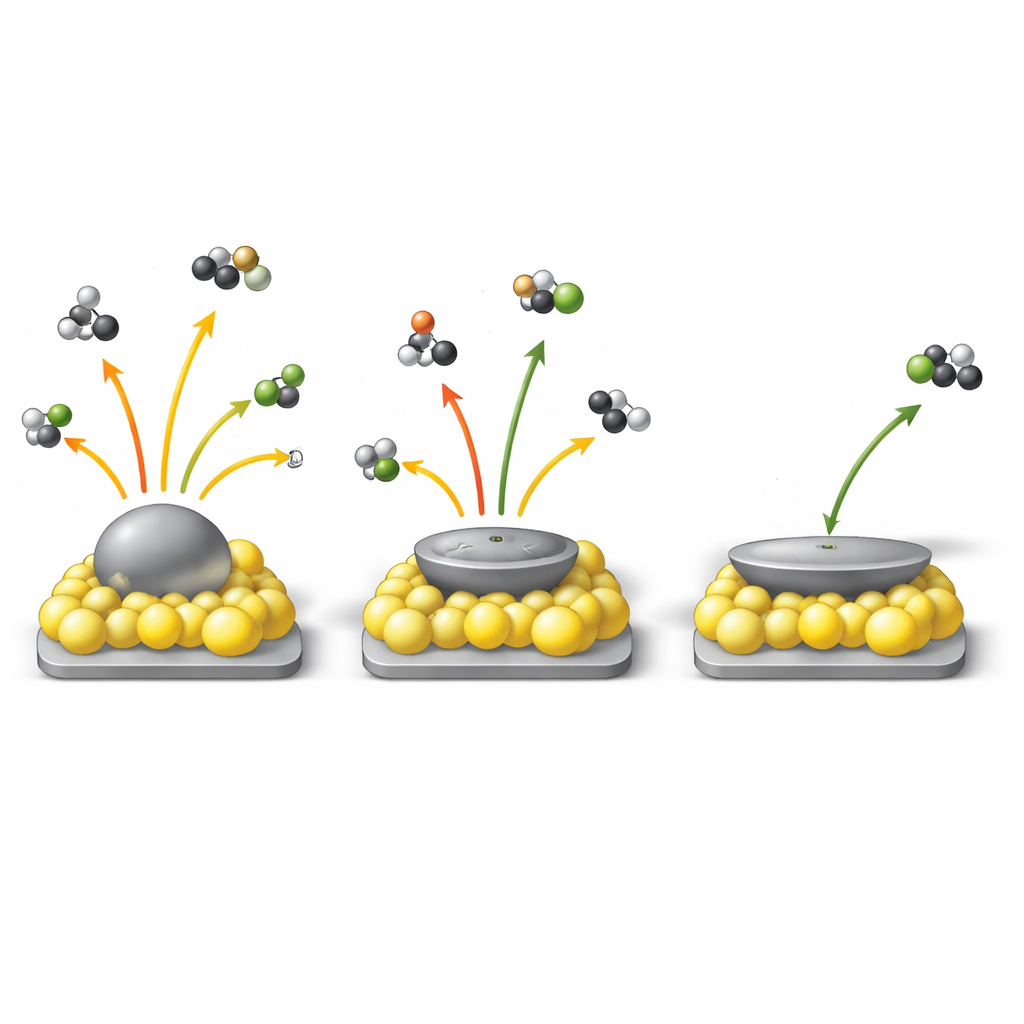
Aby sprawdzić praktyczne znaczenie tej rekonstrukcji, badacze wybrali półhydrogenację alkinu o nazwie 2‑metylo‑3‑butyn‑2‑ol, wymagającą reakcję, w której celem jest zatrzymanie się na pożądanym alkenie zamiast jego nadmiernego zredukowania. Mierzyli „spłaszczalność” cząstek prostą miarą geometryczną W, stosunkiem krótkiej do długiej średnicy cząstki na obrazach: im mniejsze W, tym bardziej płaska cząstka. W wielu próbkach i warunkach przygotowania częstość obrotu reakcji — liczba cząsteczek konwertowanych przez każdy powierzchniowy atom palladu na godzinę — skalowała się liniowo z W: bardziej płaskie cząstki były konsekwentnie bardziej aktywne. Badania kinetyczne i obliczenia komputerowe wyjaśniły dlaczego: w miarę jak rekonstrukcja zwiększała udział ubogich w elektrony miejsc palladu, alkin przestał tak silnie przywierać do powierzchni, zmniejszając „samozatrucie” i uwalniając miejsca reakcyjne.
Jak selektywność przełącza się z kontroli ładunkiem na kontrolę kształtem
Historia selektywności — zdolności zatrzymania się na pożądanym alkenie — była bardziej subtelna. Gdy cząstki były wystarczająco płaskie (W poniżej około 0,85), selektywność utrzymywała się na wysokim poziomie, powyżej około 96%, nawet jeśli szczegółowa geometria nadal się zmieniała. W tym reżimie dominowało zachowanie wynikające z ubogiego w elektrony palladu tworzonego przez silne wiązanie z tlenkiem ceru, osłabiające tendencję reaktywnych miejsc do nadmiernej hydrogenacji alkenu. Gdy jednak W przekraczał próg, powierzchnie palladu stawały się bardziej bogate w elektrony, a udział nisko‑koordynowanych krawędzi i narożników wzrastał. Tam geometria brała górę: te miejsca silnie wiążą produkt alkenowy i sprzyjają niepożądanej dodatkowej hydrogenacji, więc selektywność gwałtownie spadała. Poprzez systematyczne zmienianie rozmiaru cząstek, nośnika i warunków obróbki cieplnej autorzy odwzorowali te trendy w diagramach konturowych pokazujących, gdzie w przestrzeni „kształt‑ładunek” może wystąpić nadmierna hydrogenacja, a gdzie jest ona skutecznie powstrzymywana.
Prosty przepis na lepsze katalizatory hydrogenacyjne
W praktyce zoptymalizowany termicznie zrekonstruowany pallad na tlenku ceru przewyższał klasyczny katalizator przemysłowy Lindlara o ponad rząd wielkości pod względem aktywności, osiągając jednocześnie około 97,5% selektywności, i robił to bez toksycznych dodatków. Być może jeszcze ważniejsze, praca oferuje ramy ilościowe: pojedynczy deskryptor geometryczny (W) oraz miara udziału ubogiego w elektrony palladu razem przewidują nie tylko jak szybko katalizator będzie działał, ale także czy będzie faworyzował pożądany produkt. Ten plan powinien być przenośny na inne metale i nośniki, gdzie geometria i struktura elektronowa są powiązane, pomagając chemikom celowo projektować katalizatory jednocześnie wydajne i czyste.
Cytowanie: Li, M., Fu, Z., Luo, Q. et al. Decoupling electronic and geometric effects in Pd catalysts via thermal surface reconstruction for selective hydrogenation. Nat Commun 17, 2500 (2026). https://doi.org/10.1038/s41467-026-70568-z
Słowa kluczowe: kataliza palladu, selektywna hydrogenacja, interakcja metal‑nośnik, katalizatory na tlenku ceru, rekonstrukcja powierzchni