Clear Sky Science · pl
StrucGAP: modułowa, odchudzona i możliwa do śledzenia platforma do eksploracji danych w strukturalnej i miejscowo-specyficznej glikoproteomice
Rozszyfrowywanie cukrowych powłok na białkach
Każda komórka w naszym organizmie jest pokryta „lasem” cukrowych struktur przyczepionych do białek. Te „cukrowe powłoki”, zwane glikanami, w subtelny sposób kontrolują, jak komórki przylegają do siebie, komunikują się i reagują na otoczenie. Współczesne urządzenia potrafią katalogować te wzorce cukrowe ze zdumiewającą szczegółowością, jednak badacze często toną w ogromie i złożoności danych. W tym badaniu przedstawiono StrucGAP — nową platformę obliczeniową zaprojektowaną do przekształcania tych gęstych pomiarów w jasne, biologicznie znaczące opowieści, wykorzystując starzenie się macicy myszy jako studium przypadku.
Nowe centrum kontroli danych o cukrowych powłokach
StrucGAP to platforma programowa stworzona do analizy jednego, określonego rodzaju dekoracji cukrowej: glikanów N‑wiązanych, które przyłączają się do określonych miejsc na białkach. Zamiast próbować być narzędziem ogólnego zastosowania, StrucGAP został zaprojektowany od podstaw pod to zadanie. Przyjmuje wyniki z kilku popularnych „silników” wyszukiwania spektrometrii mas, które identyfikują, jakie glikany występują na których miejscach białkowych. Gdy te identyfikacje są dostępne, StrucGAP przeprowadza je przez serię modułów sprawdzających jakość danych, podsumowujących ogólne wzorce glikanów, śledzących, jak konkretne miejsca zmieniają się między warunkami, oraz łączących te zmiany z znanymi funkcjami i ścieżkami biologicznymi.
Rozbijanie złożonych cukrów na znaczące części
Większość istniejących narzędzi traktuje każdy glikan jako pojedynczy, niepodzielny obiekt. StrucGAP podchodzi inaczej: rozkłada każdy glikan na mniejsze, biologicznie istotne elementy składowe, takie jak typowe rdzenie, wzory rozgałęzień oraz dobrze znane motywy zawierające fukozę lub kwasy sjalowe. Następnie analizuje nie tylko to, które całe glikany wzrastają lub maleją, ale które motywy pojawiają się częściej, rzadziej lub w nowych kombinacjach. Taki widok „podstruktur” zwiększa odporność analizy na niepewne przypisania i pomaga ujawnić wzorce, które w przeciwnym razie mogłyby pozostać ukryte — szczególnie gdy rzadkie, lecz istotne motywy stają się wzbogacone w specyficznym warunku.
Śledzenie zmian cukrów podczas starzenia macicy
Aby pokazać możliwości StrucGAP, autorzy zastosowali go do szczegółowego zestawu danych z tkanki macicy młodych i średnio wiekowych myszy samic. Surowy eksperyment zidentyfikował ponad dwadzieścia tysięcy unikalnych glikopeptydów, z których każdy reprezentował określone miejsce białkowe z konkretnym glikanem. StrucGAP najpierw oczyścił i ustandaryzował dane, a następnie zobrazował rozkład glikanów w miejscach białkowych oraz liczbę wariantów strukturalnych występujących na każdej pozycji. Macica okazała się bogata zarówno w proste glikany typu high‑mannose, jak i bardziej rozbudowane typy złożone, przy czym wiele składów glikanów występowało jako liczne izomery strukturalne. Poprzez przyjrzenie się podstrukturom, platforma skatalogowała częstotliwość występowania różnych rdzeni, liczby rozgałęzień oraz motywów takich jak epitopy Lewisa czy określone formy kwasu sjalowego i ich współwystępowanie.
Od wzorców do funkcji: adhezja i przebudowa
Moduł ilościowy StrucGAP porównał następnie młode i stare macice, znajdując ponad tysiąc glikopeptydów, które wzrosły, oraz kilkaset, które zmalały z wiekiem. Powtarzającym się motywem była „fukozylacja rdzeniowa” — specyficzny sposób przyłączenia fukozy do rdzenia glikanu — która wykazywała zmiany w obu kierunkach, co sugeruje wyrafinowaną regulację, a nie prosty włącznik/wyłącznik. Inne wzorce ujawniły się wraz z zaostrzaniem progów statystycznych: glikany o większej liczbie rozgałęzień, określone motywy typu Lewis oraz kwasy sjalowe zawierające Neu5Ac stawały się stopniowo wzbogacone. Łącząc te cechy strukturalne z bazami danych funkcji genów i ścieżek, StrucGAP wykazał, że zmieniające się glikany koncentrowały się na białkach zaangażowanych w adhezję komórek, interakcje z macierzą okołakomórkową oraz przebudowę architektury tkanki. Platforma powiązała te wzorce również ze zmianami w enzymach budujących i przycinających glikany oraz z białkami wiążącymi glikany, szkicując skoordynowane sieci, które mogą napędzać starzenie macicy.
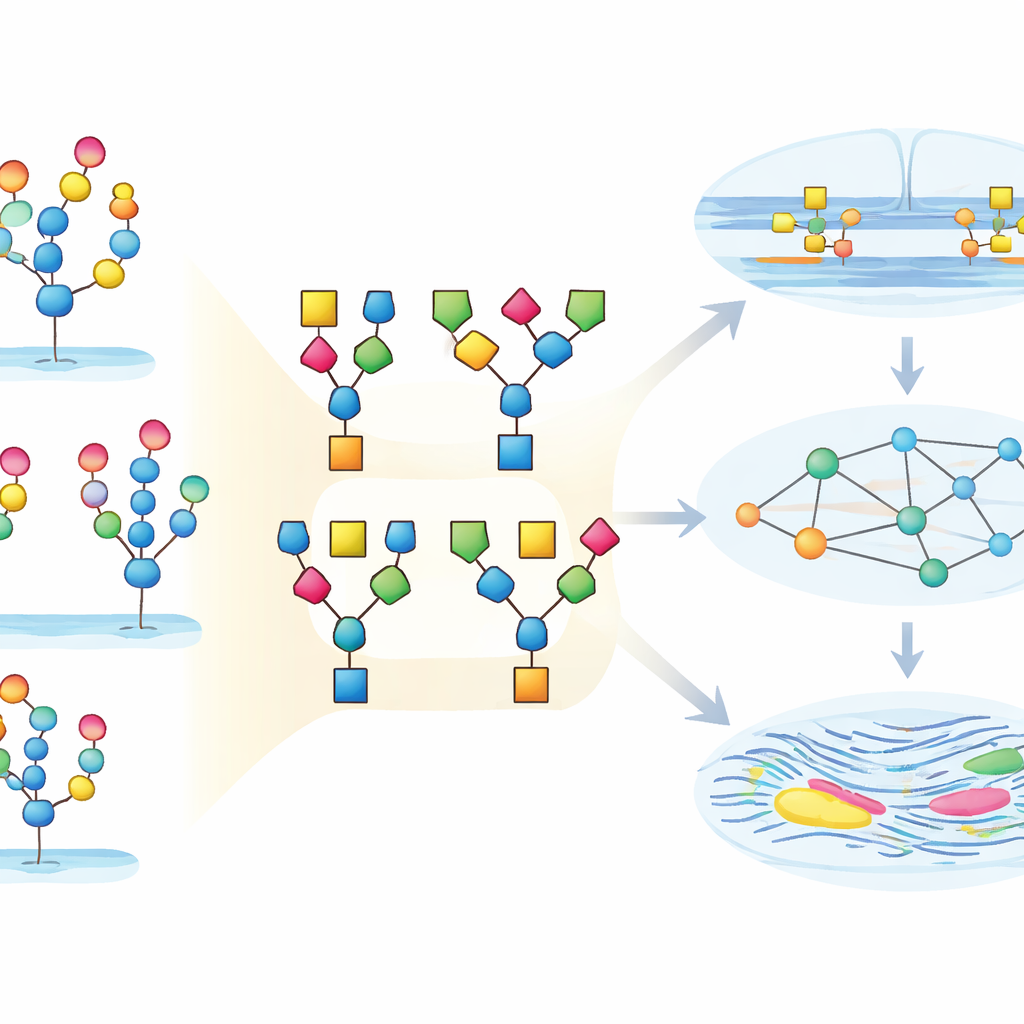
Przekształcanie zalewu danych w biologiczną wiedzę
Mówiąc prościej, praca ta pokazuje, jak silnie techniczna masa pomiarów „cukru na białku” może zostać przekształcona w czytelną mapę zmian w tkankach w czasie. StrucGAP działa zarówno jako strażnik jakości, jak i silnik opowieści: oczyszcza dane, podsumowuje kluczowe motywy cukrowe, łączy je z enzymami, które je kształtują, oraz ze ścieżkami, które one wpływają, a także automatycznie generuje wykresy i raporty podkreślające najważniejsze odkrycia. W macicy myszy ujawnia to skoordynowany przesuw w stronę bardziej obficie ozdobionych glikanów bogatych w Neu5Ac i fukozę, powiązanych z adhezją i przebudową tkanki. W szerszym ujęciu StrucGAP oferuje badaczom praktyczny sposób przejścia od surowych danych glikoproteomicznych do możliwych do przetestowania hipotez o tym, jak cukrowe powłoki pomagają kontrolować zdrowie, choroby i starzenie.
Cytowanie: Yang, M., Wu, Y., Zhang, Z. et al. StrucGAP: a modular, streamlined and traceable data mining platform for structural and site-specific glycoproteomics. Nat Commun 17, 2579 (2026). https://doi.org/10.1038/s41467-026-70560-7
Słowa kluczowe: glikoproteomika, N-glikozylacja, platforma bioinformatyczna, starzenie macicy, glikozylacja białek