Clear Sky Science · pl
Przejścia strukturalne w stopniowym składaniu rdzeniowych cząstek proteasomu
Jak komórki usuwają molekularne śmieci
W każdej naszej komórce zużyte i uszkodzone białka muszą zostać rozłożone, zanim nagromadzą się jak odpady. Olbrzymia maszyna molekularna zwana proteasomem wykonuje większość tej pracy porządkowej i jest już celem leków przeciwnowotworowych. To badanie zagląda za kulisy, pokazując, jak katalityczne jądro proteasomu jest budowane krok po kroku w komórkach drożdży, ujawniając nieoczekiwane skróty i mechanizmy bezpieczeństwa, które pomagają zapewnić, że gotowa maszyna działa precyzyjnie i dopiero gdy jest na to gotowa.
Budowanie baryłki do rozdrabniania białek
Aktywna część proteasomu to baryłkowate jądro zbudowane ze stakowanych pierścieni podjednostek białkowych. Ta baryłka kryje ukryte miejsca tnące, które rozdrabniają inne białka na małe fragmenty. Ponieważ za wczesne uruchomienie tych ostrzy byłoby niebezpieczne, komórki składają baryłkę w serii częściowo zmontowanych pośrednich form. Autorzy skupili się na wczesnych wersjach jądra, znanych jako kompleksy prekursorowe, które zwykle występują rzadko i tylko przez krótki czas. Poprzez lekkie spowolnienie jednego z ostatnich etapów składania udało im się wychwycić i oczyścić te wczesne formy z drożdży oraz zobrazować je przy użyciu wysokorozdzielczej kriomikroskopii elektronowej, która zamraża cząsteczki w działaniu i ujawnia ich trójwymiarowe kształty.
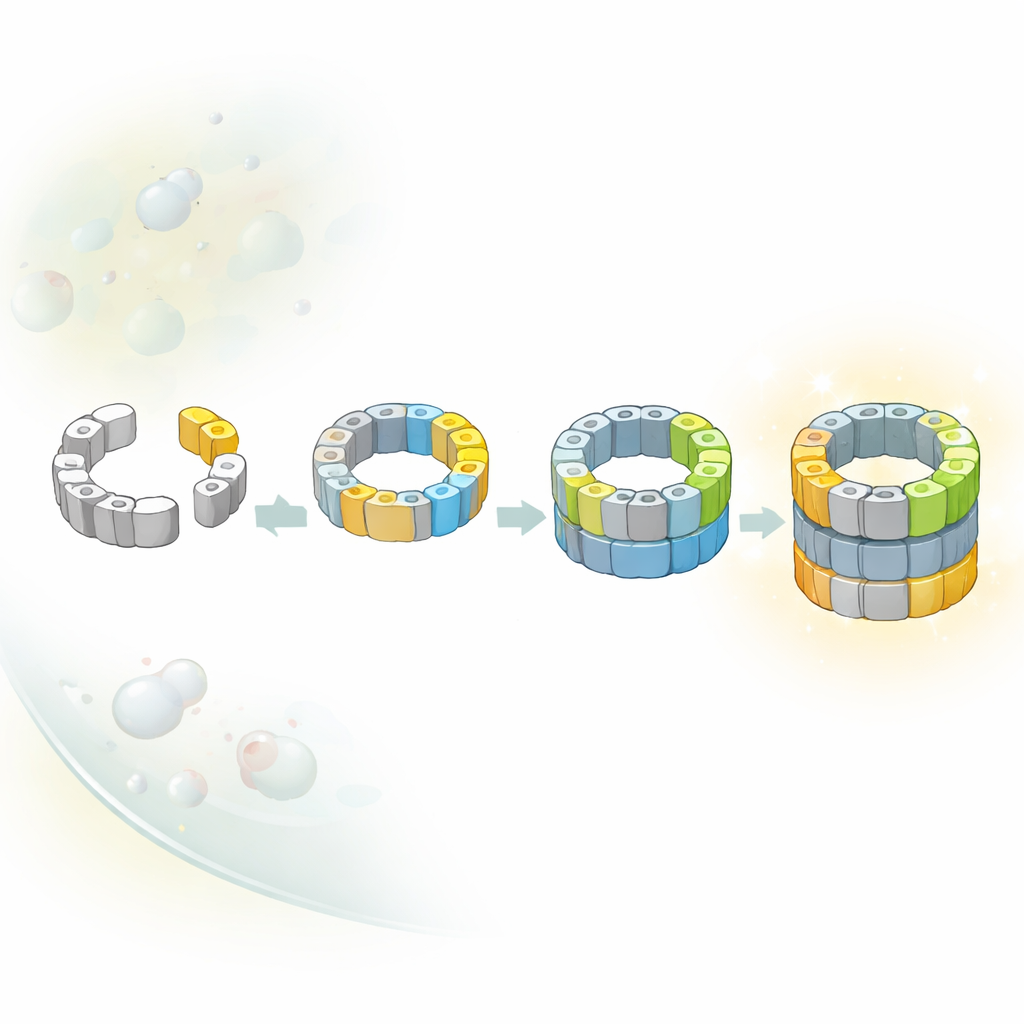
Wiele dróg prowadzących do tego samego jądra
Klasyczne schematy podręcznikowe często sugerują, że złożone maszyny wewnątrz komórek są budowane jedną, stałą trasą. Tutaj badacze wykazali, że w przypadku jądra proteasomu tak nie jest. Zidentyfikowali kilka odrębnych pośrednich form, różniących się tym, które podjednostki katalityczne dołączyły do półzbudowanej baryłki. Łącząc strukturalne migawki z genetycznymi sztuczkami pozwalającymi włączać i wyłączać poszczególne podjednostki, pokazali, że przynajmniej dwie alternatywne ścieżki prowadzą od wczesnej półbaryłki do niemal kompletnej. W jednej ścieżce określona podjednostka nazwana β5 pojawia się najpierw; w innej wcześniej może dołączyć inna podjednostka, β1. Równowaga między tymi drogami zależy prawdopodobnie od tego, które elementy budulcowe są najbardziej dostępne w zatłoczonym środowisku komórkowym.
Z luźnych części do zamkniętej komory tnącej
Struktury ujawniają także, jak miejsca tnące proteasomu są ostrożnie przygotowywane w miarę postępu składania. We wczesnych pośrednich formach kluczowe pętle otaczające ukryte reszty tnące są wiotkie i słabo uporządkowane, a centra katalityczne wciąż są zablokowane przez krótkie segmenty „propeptydowe”. W miarę jak kolejne podjednostki wskakują na miejsce wokół pierścienia, te pętle stopniowo przyjmują bardziej określone kształty, ustawiając istotne aminokwasy potrzebne do samoaktywacji. Dopiero gdy dwie półbaryłki wreszcie się złączą, zamykając podwójny pierścień, pętle blokujące w pełni blokują się w aktywne ułożenie i inicjują usunięcie segmentów blokujących. To sprzężenie geometrii i chemii pomaga zapewnić, że silna aktywność tnąca pojawia się tylko wewnątrz uszczelnionej komory, chroniąc resztę komórki.
Chaperony pomagają prowadzić i potem odchodzą
W trakcie składania wyspecjalizowane białka pomocnicze zwane chaperonami nadzorują baryłkę i zapobiegają nieprawidłowym połączeniom. Jeden chaperon, Ump1, zaczyna w dużej mierze nieuporządkowany, lecz stopniowo się fałduje w miarę otaczania go przez kolejne podjednostki, ostatecznie zostając uwięziony w centralnej jamie, a następnie zniszczony, gdy baryłka staje się aktywna. Para innych chaperonów, Pba1–Pba2, chwyta powierzchnię zewnętrznego pierścienia w dwóch sprytnych sposób. Elastyczna pętla Pba1 klinuje się między dwiema podjednostkami pierścienia zewnętrznego jak dystans, trzymając je lekko rozstawione i zapobiegając przedwczesnemu zamknięciu. Jednocześnie końcówka jednej podjednostki zewnętrznej (α1) pomaga ustawić sąsiednie segmenty tak, że na końcowym etapie chaperony mogą zostać uwolnione i pierścień może się prawidłowo zamknąć. Gdy badacze usunęli ogon α1, baryłka ugrzęzła w późnym, niemal ukończonym stanie, który uporczywie zatrzymywał chaperony, co potwierdza, że ten niewielki fragment działa jako część wyłącznika uwalniającego.
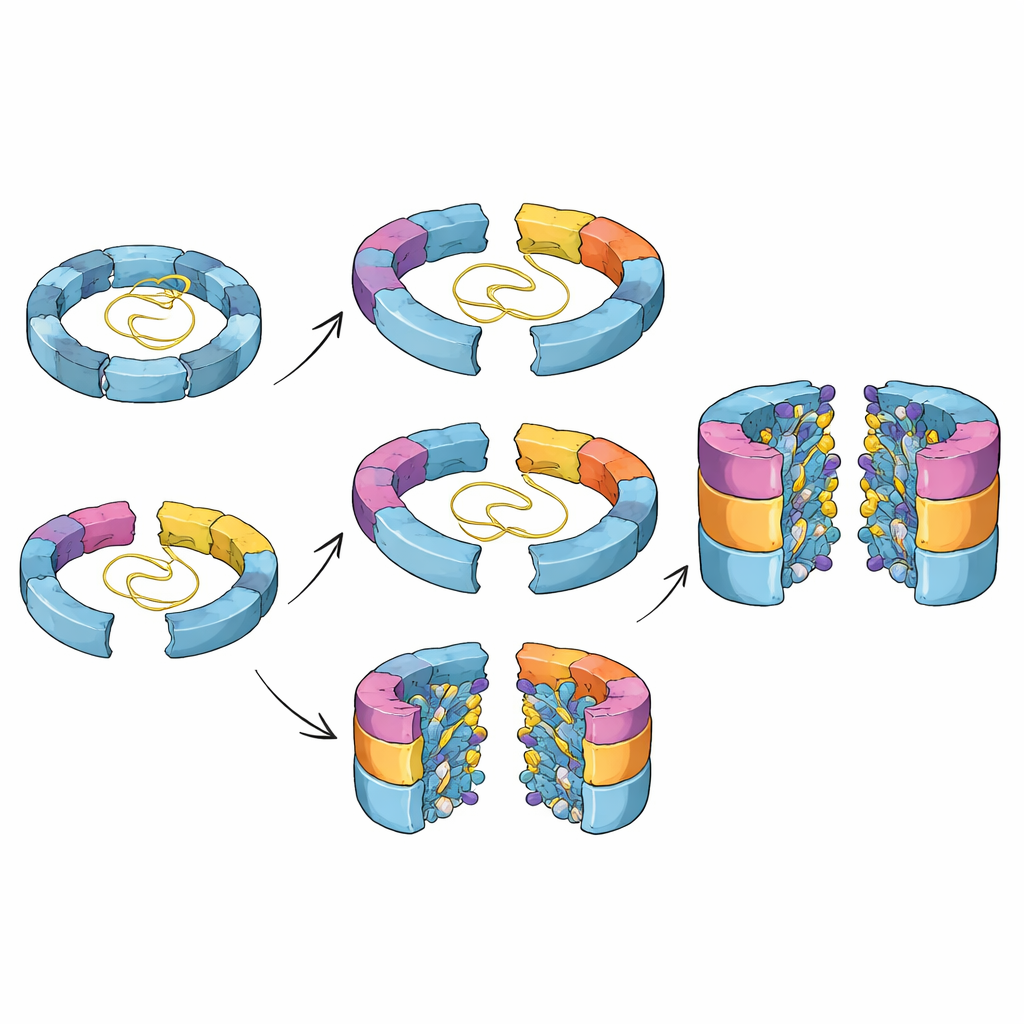
Dlaczego te ukryte kroki mają znaczenie
Razem te ustalenia kreślą szczegółowy obraz tego, jak komórki koordynują składanie niebezpiecznego, lecz niezbędnego niszczarki białek. Praca pokazuje, że jądro proteasomu może być zbudowane więcej niż jedną drogą, że jego miejsca aktywne są stopniowo kształtowane w miejscu oraz że białka pomocnicze nie tylko stabilizują wczesne pośrednie formy, lecz także są wpisane w obwód czasowy, który zapewnia ich odejście we właściwym momencie. Zrozumienie tych ukrytych kroków pomaga wyjaśnić, jak niewielkie zmiany genetyczne w czynnikach składania mogą przyczyniać się do chorób i może ułatwić projektowanie leków, które precyzyjnie dostrajają aktywność proteasomu w nowotworach, zaburzeniach odporności czy neurodegeneracji, celując w jego budowę zamiast formy ostatecznej.
Cytowanie: Mark, E., Ramos, P.C., Nunes, M.M. et al. Structural transitions in the stepwise assembly of proteasome core particles. Nat Commun 17, 2582 (2026). https://doi.org/10.1038/s41467-026-70525-w
Słowa kluczowe: składanie proteasomu, degradacja białek, molekularne chaperony, kriomikroskopia elektronowa, komórkowa kontrola jakości