Clear Sky Science · pl
Bezlabelekowa charakterystyka masy i rozmiaru biomolekuł o masie kilku kDa za pomocą hierarchicznego transformera wizji wspomaganego nanofluidyczną mikroskopią rozproszenia
Widzenie najmniejszych cząsteczek
Wiele z najważniejszych przekaźników w organizmie — takich jak hormony i sygnały układu odpornościowego — jest tak małych, że pozostawały niemal niewidoczne dla silnych mikroskopów, chyba że oznaczono je fluorescencyjnie. Te oznaczenia mogą zmieniać zachowanie cząsteczek, co stanowi poważny problem dla odkrywania leków i badań podstawowych. W tej pracy wprowadzono metodę ważenia i pomiaru rozmiaru pojedynczych cząsteczek wielkości insuliny bez użycia etykiet, łącząc chipy nanofluidyczne z zaawansowaną sztuczną inteligencją. Otwiera to drogę do obserwowania kluczowych biomolekuł w ich naturalnym stanie, jedna po drugiej.
Drobne kanały jako probówki
Rdzeniem metody jest nanofluidyczna mikroskopia rozproszeniowa, która wykorzystuje płytkę wielkości paznokcia wytrawioną z ekstremalnie wąskimi kanałami. Kanały te mają zaledwie kilkadziesiąt nanometrów szerokości — tysiące razy mniej niż grubość włosa. Molekuły rozpuszczone w buforze unoszą się swobodnie przez te kanały, zamiast przylegać do powierzchni. Po oświetleniu chipu światłem widzialnym zarówno ścianki kanału, jak i przechodzące cząsteczki rozpraszają światło. Ponieważ kanał jest znacznie większy niż cząsteczka, ich rozproszone światło interferuje w sposób znacznie wzmacniający optyczne sygnatury cząsteczki. Odejmując obrazy pustego kanału od obrazów z obecnością cząsteczki, badacze uzyskują zapis przypominający film (kimografię) jej przejścia przez kanał, zawierający informacje zarówno o masie, jak i o szybkości dyfuzji.
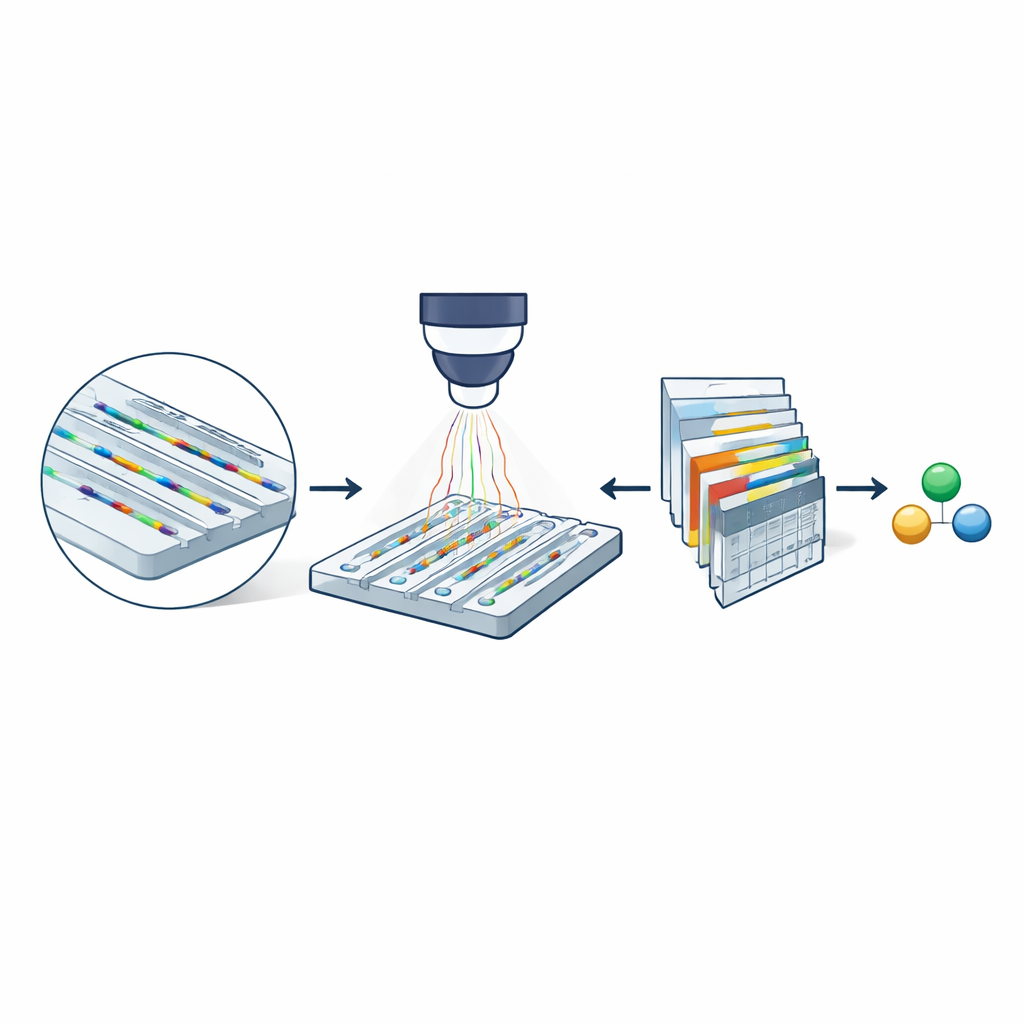
Dlaczego mniejsze kanały mają znaczenie
Nawet przy tym optycznym wzmocnieniu wcześniejsze wersje techniki mogły charakteryzować tylko cząsteczki cięższe niż około 60 kilodaltonów — typowe duże białka — ponieważ sygnały od mniejszych gatunków tonęły w szumie. Zespół pokazuje, że zmniejszenie przekroju kanałów dramatycznie poprawia czułość: kontrast optyczny od cząsteczki rośnie wraz ze zmniejszaniem się pola przekroju kanału. Eksperymenty porównujące dwa rozmiary kanałów z białkiem albuminy surowicy bydlęcej wykazują, że jego ślad jest wyraźnie widoczny w węższym kanale, ale niemal zanika w szerszym. Ta prosta zmiana geometryczna sugeruje, że w zasadzie możliwe jest wykrycie dużo mniejszych biomolekuł, pod warunkiem że ich słabe sygnały da się wiarygodnie wyodrębnić z zaszumionych sekwencji obrazów.
Pozwalając SI czytać zaszumione filmy
Aby wejść w ten zakres, badacze opracowali specjalistyczny model głębokiego uczenia zwany hierarchicznym transformerem wizji. Zamiast rekonstruować dokładny tor każdej cząsteczki piksel po pikselu, model skanuje kimografię na wielu skalach i produkuje dwa wyniki: mapę prawdopodobieństwa wskazującą, gdzie cząsteczka prawdopodobnie się znajduje w danym punkcie przestrzeni i czasu, oraz mapę właściwości kodującą oszacowania masy cząsteczkowej i wielkości hydrodynamicznej. Ważąc oszacowania właściwości mapą prawdopodobieństwa, model może ignorować regiony będące głównie szumem. Trening opiera się wyłącznie na symulowanych trajektoriach nałożonych na eksperymentalnie zmierzone tło szumowe, co pozwala systemowi nauczyć się, jak wyglądają prawdziwe sygnały, nawet gdy są ledwie widoczne dla oka.
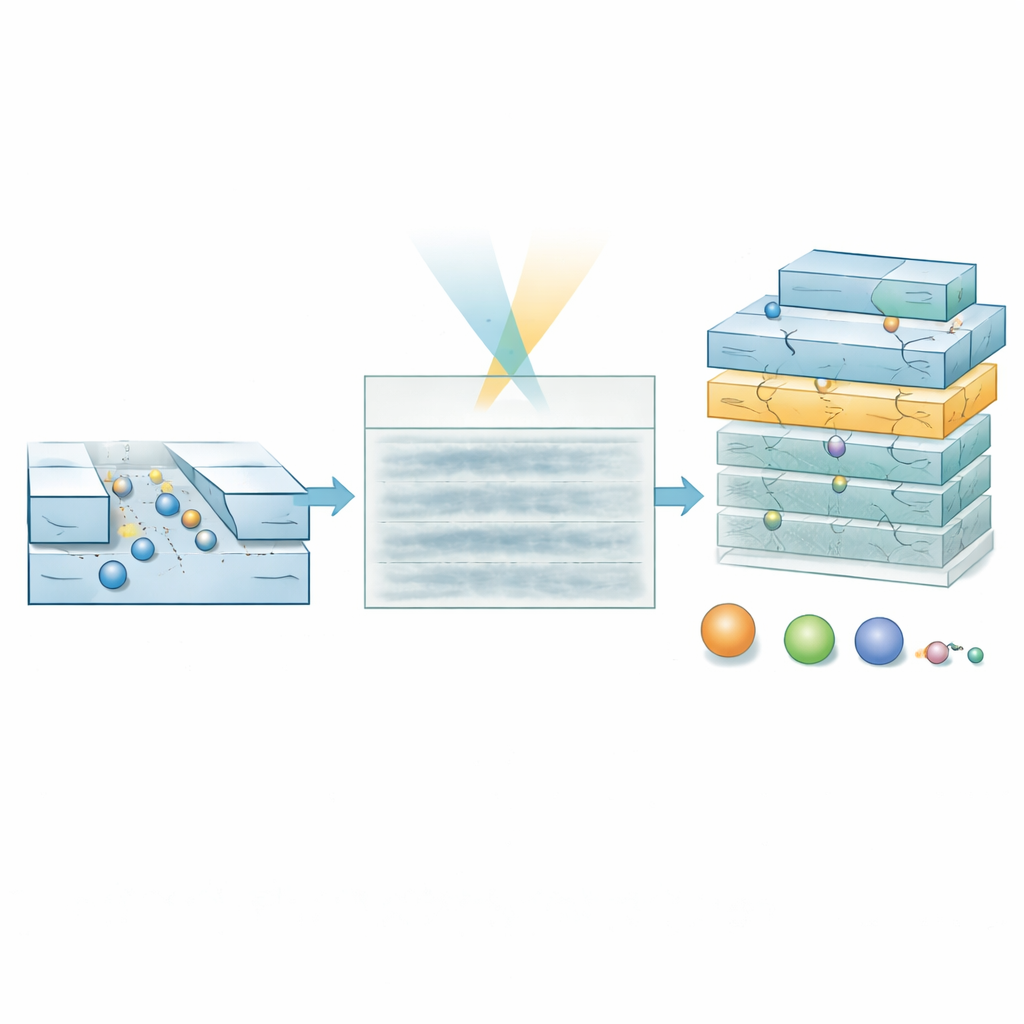
Testy na DNA i cząsteczkach hormonów
Autorzy najpierw zweryfikowali podejście, używając standardowej „drabinki” DNA — mieszaniny fragmentów dwuniciowych o znanych długościach i masach — w stosunkowo szerokich kanałach, gdzie wszystkie fragmenty celowo znajdują się poniżej zwykłego progu detekcji. W surowych filmach nie widać wyraźnych torów DNA. Mimo to model SI generuje mapy prawdopodobieństwa poprawnie wskazujące miejsca przejścia cząsteczek i przewiduje masy zgodne z oczekiwanymi wartościami po odfiltrowaniu danych o niskim zaufaniu. Metoda prawidłowo raportuje także mniejsze efektywne rozmiary sztywnych, pręcikowatych fragmentów DNA niż ich pełna długość fizyczna, co odzwierciedla wpływ kształtu na dyfuzję. Najbardziej wymagający test przeprowadzono w ultrasmalych kanałach na peptydowym hormonie insulinie, który waży tylko około 5,8 kilodaltona i ma około 1,5 nanometra średnicy. Tutaj również kimografie wyglądają bez cech, ale model wydobywa ciasną grupę wartości masy i rozmiaru, doskonale zgodną z danymi literaturowymi i wyraźnie odseparowaną od kontroli z samym buforem.
Badanie granic możliwości
Aby zrozumieć, jak daleko może sięgać ta strategia, zespół porównał precyzję modelu z dolnym ograniczeniem Craméra–Rao, statystyczną granicą definiującą najlepszą możliwą dokładność dla każdego nieobciążonego estymatora przy danym poziomie szumu. Korzystając z dużych zestawów symulacji, pokazali, że gdy liczba klatek przyczyniających się do trajektorii cząsteczki rośnie powyżej około dziesięciu tysięcy, oszacowania masy i rozmiaru przez model zbliżają się do tego teoretycznego optimum nawet dla cząstki sześciokilodaltonowej. Eksperymenty na insulinie przy różnych stężeniach odtwarzają ten sam trend: dłuższe efektywne trajektorie dają bardziej precyzyjne pomiary, ograniczone głównie przez to, jak długo drobne, szybko dyfundujące cząsteczki utrzymują się w polu widzenia. Autorzy proponują przyszłe strategie — takie jak delikatne uwięzienie cząsteczek w kanałach lub ponowne wykorzystanie danych przez bootstrapping — aby jeszcze wydłużyć użyteczny czas obserwacji.
Co to oznacza dla biologii i medycyny
Mówiąc prościej, praca ta pokazuje, że obecnie możliwe jest ważenie i mierzenie rozmiaru niektórych z najmniejszych i najważniejszych cząsteczek w organizmie indywidualnie, bez dotykania ich znacznikami fluorescencyjnymi lub przylegania do powierzchni. Łącząc nanowytworzone kanały z dedykowaną SI, która interpretuje zaszumione filmy rozproszeniowe, metoda obniża granicę detekcji masy tej bezlabelowej mikroskopii w przybliżeniu o rząd wielkości. Otwiera to drzwi do badania rodzin małych białek sygnałowych i peptydowych hormonów — takich jak cytokiny, chemokiny i insulina — na poziomie pojedynczej cząsteczki, oraz do charakteryzowania maleńkich biologicznych nanocząstek i nośników leków z niespotykaną dotąd czułością. W miarę dojrzewania technologii może ona stać się potężnym narzędziem w odkrywaniu leków, diagnostyce i badaniach podstawowych nad tym, jak interakcje molekularne kształtują życie na najmniejszych skalach.
Cytowanie: K. Moberg, H., Yeroshenko, B., Fritzsche, J. et al. Label-free mass and size characterization of few-kDa biomolecules by hierarchical vision transformer augmented nanofluidic scattering microscopy. Nat Commun 17, 2533 (2026). https://doi.org/10.1038/s41467-026-70514-z
Słowa kluczowe: bezlabelowa mikroskopia pojedynczych cząsteczek, nanofluidyczne rozpraszanie, transformer wizji, małe biomolekuły, detekcja insuliny