Clear Sky Science · pl
Patologiczna mutacja Tau powoduje dysfunkcję autofagii‑lizosomów, która ogranicza degradację Tau w modelu otępienia czołowo‑skroniowego
Kiedy sprzątaczki mózgu zostają w tyle
Dlaczego niektórzy ludzie rozwijają druzgocące problemy z pamięcią i zachowaniem na wiele lat przed starością? To badanie zajmuje się tym pytaniem, skupiając się na pojedynczym białku mózgowym — Tau — oraz na małych komórkowych „centrach recyklingu”, które zwykle nad nim czuwają. Obserwując żywe ludzkie neurony pod superostrą mikroskopią, autorzy pokazują, jak chorobotwórcza mutacja Tau zatyka system usuwania odpadów w komórce oraz jak pobudzenie tego systemu małą cząsteczką może pomóc posprzątać bałagan. Wyniki mogą wskazywać nowe strategie terapeutyczne dla niektórych postaci otępienia.
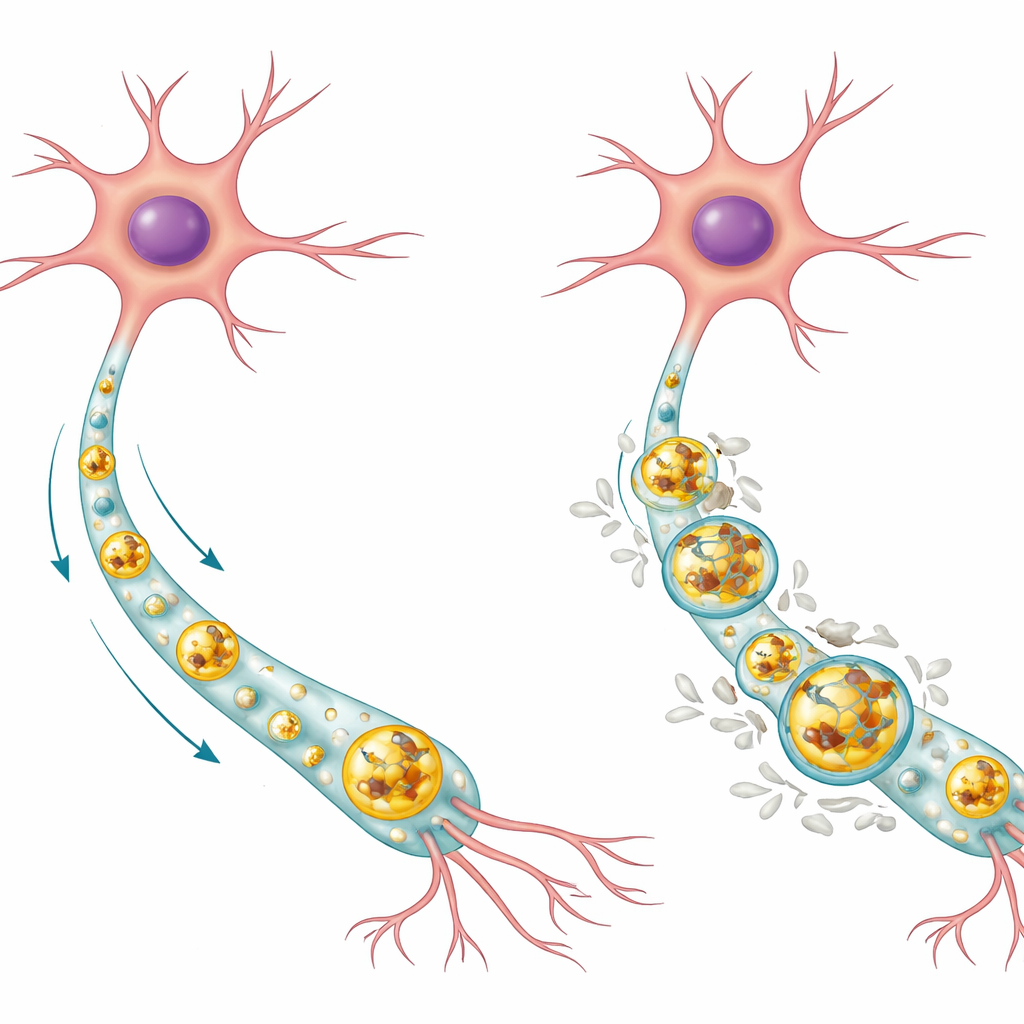
Jak neurony zwykle wynoszą śmieci
Neurony są komórkami długowiecznymi, które nie mogą po prostu dzielić się, by rozcieńczyć uszkodzone elementy, więc silnie polegają na wewnętrznych systemach sprzątających. Jedną z głównych dróg jest ścieżka autofagia‑lizosom. W tym procesie niechciane białka i zużyte części są otaczane pęcherzykami błonowymi zwanymi autofagosomami, które następnie łączą się z wypełnionymi enzymami przedziałami zwanymi lizosomami, gdzie ładunek jest rozkładany i poddawany recyklingowi. W zdrowych ludzkich neuronach autorzy stwierdzili, że normalne białko Tau ma skłonność do gromadzenia się w kwaśnym wnętrzu lizosomów, gdzie może być degradowane, podczas gdy ufosforylowana forma Tau (modyfikacja chemiczna powiązana z chorobą) znajduje się częściej na zewnętrznej błonie lizosomu. Większość lizosomów w zdrowych komórkach była pozbawiona Tau, co sugeruje, że ten system zwykle utrzymuje poziomy Tau niskie i dobrze kontrolowane.
Co idzie nie tak w genetycznej postaci otępienia
Zespół skupił się na mutacji w genie MAPT, zwanej p.R406W, która powoduje dziedziczną postać otępienia czołowo‑skroniowego i może naśladować utraty pamięci podobne do choroby Alzheimera. Wykorzystując technologię komórek macierzystych, przeprogramowali skórne komórki pacjentów do indukowanych pluripotencjalnych komórek macierzystych, a następnie w dużych ilościach wytworzyli ludzkie neurony noszące albo mutację, albo naprawione genetycznie do stanu normalnego. W neuronach mutantów całkowity poziom Tau i ufosforylowanego Tau był wyraźnie podwyższony, nie dlatego że komórki produkowały więcej Tau, lecz dlatego że usuwały go mniej efektywnie. Obrazowanie w super‑rozdzielczości ujawniło, że niemal wszystkie lizosomy w komórkach mutantów były wypełnione Tau, a szczególnie ufosforylowane Tau pokrywało błonę lizosomów. To nagromadzenie sygnalizowało, że główna ścieżka usuwania białek w komórce jest zapchana.
Zatkane centra recyklingu i ospiały ruch
Przy bliższym przyjrzeniu się maszynerii recyklingowej badacze zauważyli, że lizosomy w neuronach mutantów były liczniejsze, większe i miały tendencję do ulokowania się dalej od ciała komórki. Obrazowanie na żywo z użyciem barwników fluorescencyjnych pokazało, że te lizosomy poruszały się wolniej i przebywały krótsze dystanse wzdłuż włókien nerwowych, mimo że podstawowe tory mikrotubul wyglądały normalnie. Neurony mutantów zawierały też więcej autofagosomów, więcej białka adaptorowego ładunku p62 oraz dodatkowych kropli lipidowych — oznaki, że materiały są znakowane do usunięcia, ale nie są w pełni rozkładane. Przy użyciu raportera wrażliwego na pH stwierdzono, że autofagosomy w komórkach mutantów często nie łączyły się prawidłowo z lizosomami, prowadząc do nagromadzenia „pół‑ukończonych” pęcherzyków recyklingowych i szeroko zakrojonych defektów sprzątania komórkowego, nie tylko dla Tau, lecz także dla innych ładunków.
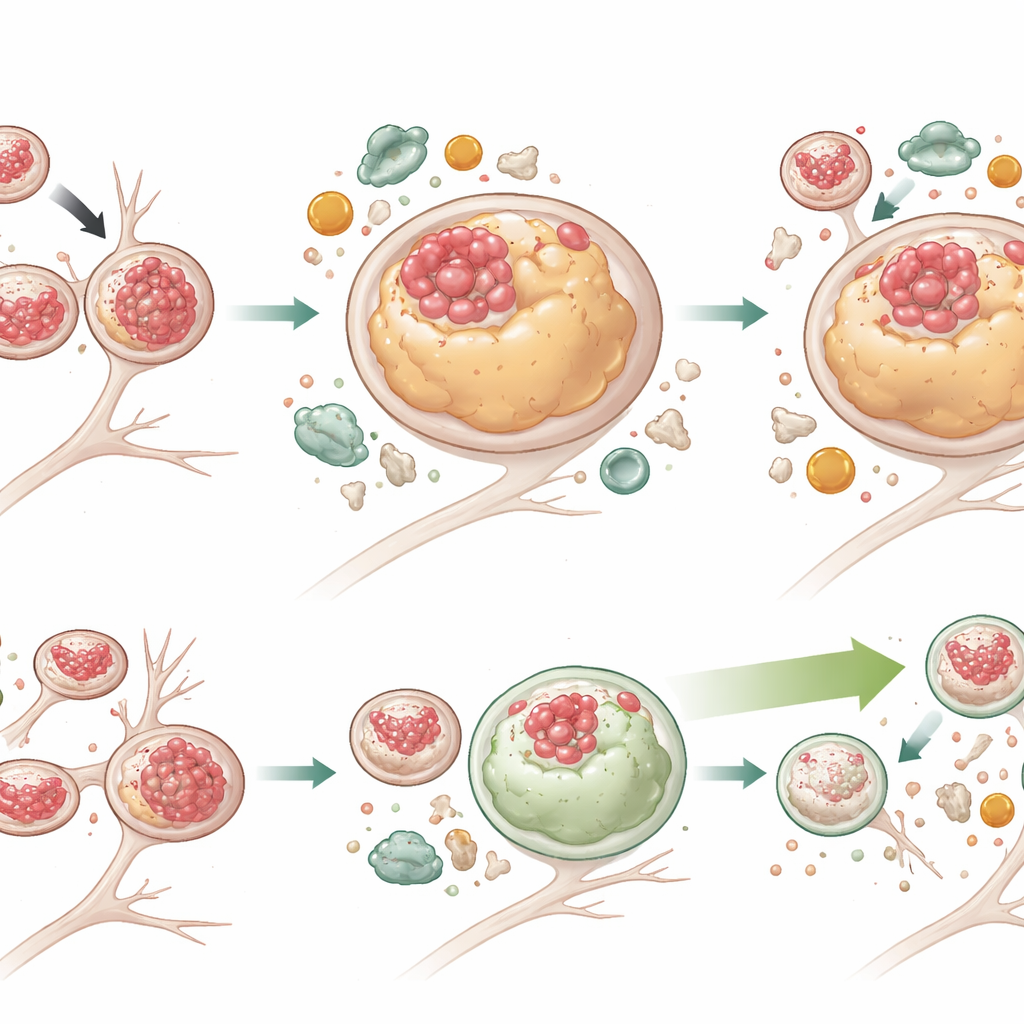
Pobudzenie sprzątania komórkowego bez naprawy korka w ruchu
Aby sprawdzić, czy wzmocnienie autofagii może przezwyciężyć te problemy, zespół potraktował neurony związkiem G2‑567, małą cząsteczką wcześniej wykazującą stymulację systemu autofagia‑lizosom. Po dwóch tygodniach leczenia neurony mutantów miały znacznie niższe poziomy zarówno całkowitego Tau, jak i ufosforylowanego Tau, a wiele lizosomów znów było wolnych od Tau. Lizosomy także zmniejszyły się w kierunku normalnych rozmiarów. Markery aktywnej autofagii wzrosły, podczas gdy p62 — wskaźnik zablokowanej degradacji — spadł w komórkach mutantów, co dowodzi skuteczniejszego rozkładu ładunku. Co ciekawe, G2‑567 nie naprawił wszystkich defektów: lizosomy w neuronach mutantów wciąż miały tendencję do ulokowania się dalej od ciała komórki i poruszały się ospale, a białko adaptorowe (JIP3) powiązane z transportem lizosomów pozostawało podwyższone. Sugeruje to, że funkcje ruchu i degradacji lizosomów mogą być częściowo rozdzielone, i że samo poprawienie rozkładu może wystarczyć, by zmniejszyć toksyczne nagromadzenie Tau.
Co to oznacza dla przyszłych terapii otępienia
Dla osoby niebędącej specjalistą najważniejsze jest to, że w tym genetycznym modelu otępienia czołowo‑skroniowego problem nie polega wyłącznie na tym, że Tau staje się nieprawidłowy; chodzi o to, że system recyklingu neuronu nie nadąża. Mutacja Tau p.R406W bezpośrednio zaburza kilka etapów ścieżki autofagia‑lizosom, powodując akumulację Tau — zwłaszcza jego ufosforylowanej formy — na i wewnątrz lizosomów, razem z innymi nierozłożonymi materiałami. Poprzez farmakologiczne pobudzenie maszynerii sprzątającej komórki badacze byli w stanie obniżyć poziomy Tau i znormalizować rozmiar lizosomów, mimo że defekty transportu utrzymywały się. Te wyniki wzmacniają ideę, że leki zaprojektowane do bezpiecznego zwiększania autofagii i funkcji lizosomów mogłyby pomóc przywrócić równowagę białek w demencjach związanych z tau, a być może także w częstszych schorzeniach, takich jak choroba Alzheimera.
Cytowanie: Mirfakhar, F.S., Marsh, J.A., Sato, C. et al. A pathogenic Tau mutation drives autophagy-lysosome dysfunction that limits Tau degradation in a model of frontotemporal dementia. Nat Commun 17, 2699 (2026). https://doi.org/10.1038/s41467-026-70473-5
Słowa kluczowe: białko tau, autofagia, dysfunkcja lizosomów, otępienie czołowo‑skroniowe, neurodegeneracja