Clear Sky Science · pl
Hydrofobowość powierzchni i sztywność determinują koronę białkową na doustnie podawanych nanocząstkach leczących colitis
Przeobrażanie pigułek w mądrzejsze terapie
Osoby z chorobami zapalnymi jelit, takimi jak colitis, często przyjmują silne leki przeciwzapalne, jednak duża część dawki jest marnowana lub wywołuje działania niepożądane w innych częściach ciała. W tym badaniu autorzy badają nowy sposób, by doustne leki zachowywały się bardziej jak sterowane pociski: projektując maleńkie nośniki leków, które rekrutują własne białka jelitowe organizmu jako naturalny system celowania, pomagając lekom trafiać do komórek odpornościowych napędzających stan zapalny w jelicie.
Jak jelito ubiera nanocząstki
Kiedy jakakolwiek nanocząstka wchodzi do organizmu, szybko pokrywa się cienką warstwą białek, tworząc to, co naukowcy nazywają „koroną białkową”. W chorobowo zmienionym jelicie ta korona wygląda bardzo inaczej niż w tkance zdrowej, ponieważ lokalny skład białek ulega zmianie. Autorzy wcześniej ustalili, że colitis powoduje specyficzną koronę jelitową, która umiarkowanie kieruje cząstki ku komórkom odpornościowym zwanym makrofagami, które zarówno napędzają, jak i wygaszają stan zapalny. W tym badaniu postanowili celowo kształtować tę koronę, modyfikując dwie podstawowe cechy nośników leków — ich hydrofobowość (odpychanie wody) i sztywność (rigidność) — aby przekształcić umiarkowany, chorobowy efekt w silną strategię celowania.
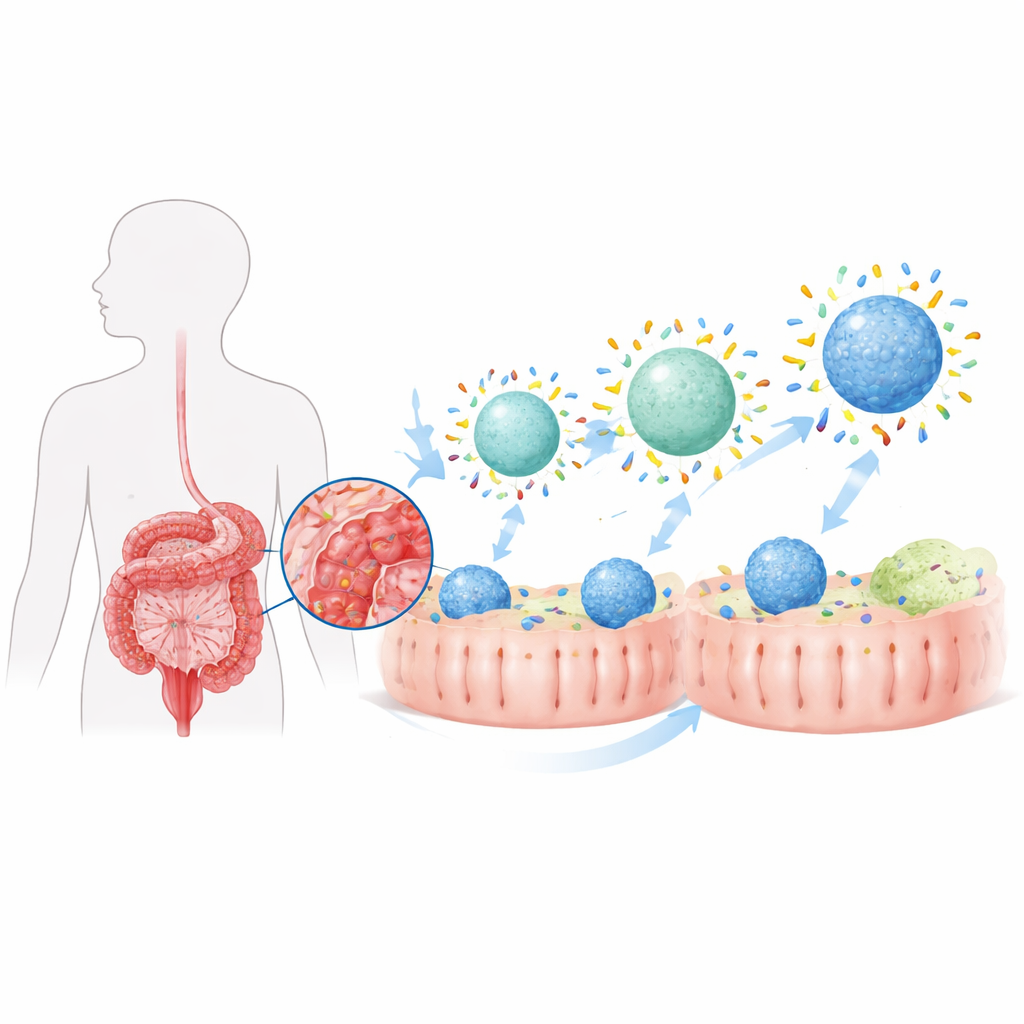
Sprawianie, by cząstki były bardziej atrakcyjne dla białek
Zespół skonstruował nanocząstki lipidowe podobne do maleńkich pęcherzyków tłuszczu i dostroił, jak ich powierzchnie są hydrofilowe lub hydrofobowe, dodając różne ilości powszechnej powłoki polimerowej. Cząstki o bardziej hydrofobowych powierzchniach wiązały znacznie więcej białek jelitowych po wystawieniu na płyny z colitis, zarówno w modelach zwierzęcych, jak i w probówkach. Gdy te „fobiczne” cząstki załadowano steroidem budezonidem i podano doustnie szczurkom z colitis, dostarczyły one dużo więcej leku do makrofagów okrężnicy niż bardziej hydrofilowe wersje. W rezultacie leczone zwierzęta odzyskiwały więcej masy ciała, wykazywały mniejsze skrócenie okrężnicy i uszkodzenia tkanki oraz miały niższe poziomy molekuł zapalnych w jelicie. Jednak mimo poprawy zapalenia nie doszło do pełnego powrotu do stanu zdrowia, co sugeruje, że samo zwiększenie łącznej ilości białek w koronie nie wystarcza.
Usztywnianie cząstek, by wybierać lepszych partnerów
Aby pójść dalej, badacze utrzymali powierzchnie hydrofobowe, ale zmienili strukturę wewnętrzną tak, by cząstki były miękkie, pośrednie lub sztywne, wypełniając ich rdzenie plastikowymi kulkami o różnych rozmiarach. Wszystkie trzy typy wciąż pochłaniały podobne całkowite ilości białek jelitowych, ale zmieniał się skład tej mieszaniny. Najsztywniejsze cząstki tworzyły korony szczególnie bogate w białka, które mogą wiązać receptory na makrofagach lub przenosić małe składniki odżywcze pobierane przez te komórki. Jedno z takich białek, S100A8, jest obfite w zapalnie zmienionych jelitach i może wchodzić w interakcję ze specyficznymi receptorami makrofagów. Zablokowanie S100A8 na koronie silnie zmniejszało pobieranie sztywnych cząstek przez makrofagi, ujawniając je jako kluczowy składnik celujący wybrany przez sztywność cząstki.
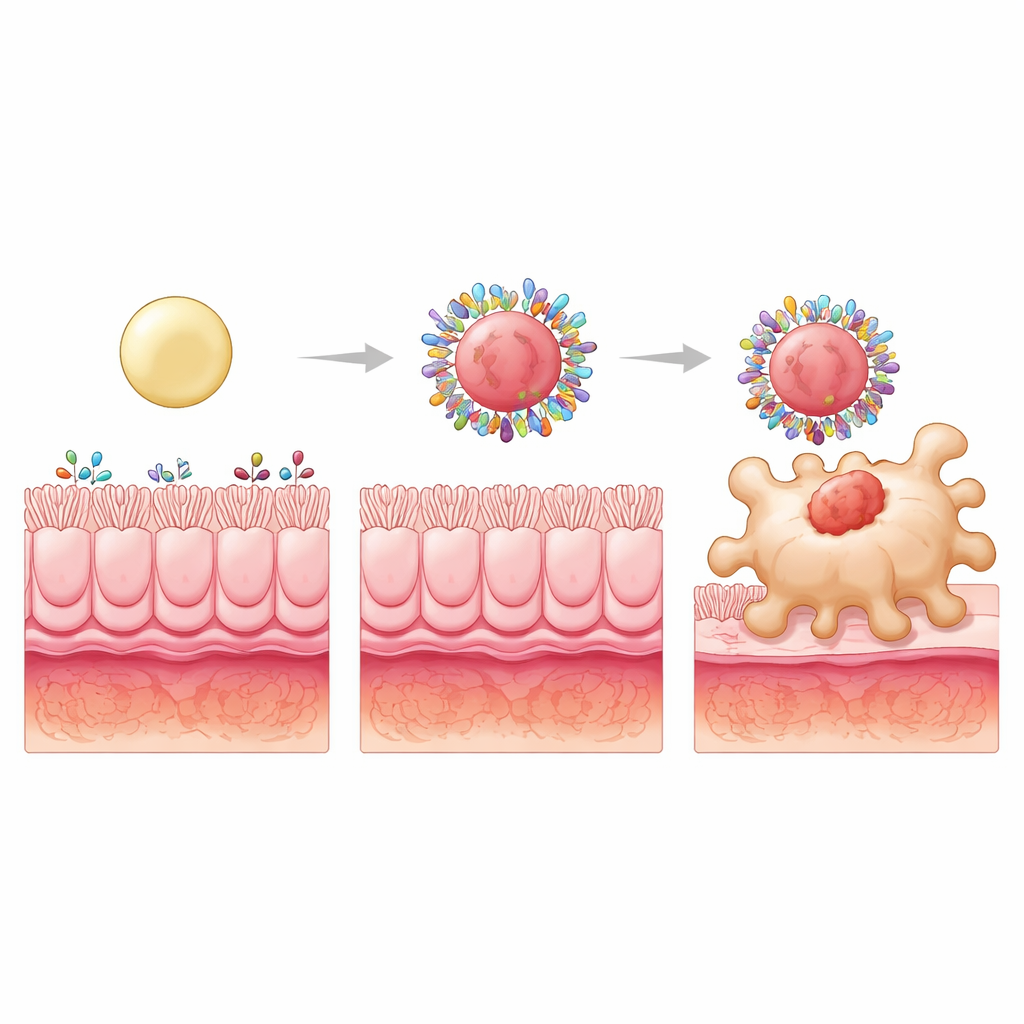
Od lepszego celowania do lepszego gojenia
Kiedy budezonid zapakowano w te cząstki o wysokiej hydrofobowości i dużej sztywności i podano doustnie szczurkom z colitis, korzyści były uderzające. Sztywna formulacja nie tylko zmniejszała uszkodzenia jelita i stres oksydacyjny, lecz także normalizowała wiele sygnałów zapalnych do poziomów obserwowanych u zwierząt zdrowych. Przywróciła zdrowszą równowagę między „atakującymi” a „uspokajającymi” typami makrofagów i zwiększyła liczbę komórek T regulatorowych, które pomagają hamować odpowiedzi immunologiczne. Co ważne, te korzyści zależały od chorobowo zmienionego środowiska białkowego w colitis; ten sam projekt nie wykazywał szczególnego celowania u zdrowych szczurów, podkreślając, że korona jest dynamicznym, specyficznym dla choroby sojusznikiem.
Dlaczego to ma znaczenie dla przyszłych leków
Praca ta pokazuje, że możemy ukierunkować własne białka organizmu, aby działały jako inteligentne, samoodnawialne „etykiety” na doustnych nośnikach leków, po prostu dostrajając właściwości powierzchniowe i mechaniczne nośników. Najpierw zwiększając wychwyt białek dzięki hydrofobowym powierzchniom, a następnie wykorzystując sztywność do faworyzowania białek homingujących do makrofagów, takich jak S100A8, badacze stworzyli nanocząstki, które naturalnie poszukują komórek odpornościowych napędzających colitis i dostarczają terapię tam, gdzie jest ona najbardziej potrzebna. Ta sama logika projektowa — manipulowanie tym, jak cząstki czują się i zachowują na powierzchni jelita — może być zaadaptowana do wielu rodzajów nanomedycyny i chorób, oferując nową, subtelniejszą drogę do celowanego leczenia bez konieczności dodawania sztucznych molekuł ukierunkowujących.
Cytowanie: Wu, J., Ni, M., Xing, L. et al. Surface hydrophobicity and rigidity determines protein corona on orally delivered nanoparticles treating colitis. Nat Commun 17, 2497 (2026). https://doi.org/10.1038/s41467-026-70453-9
Słowa kluczowe: dostarczanie leków za pomocą nanocząstek, choroby zapalne jelit, korona białkowa, doustna nanomedycyna, celowanie w makrofagi