Clear Sky Science · pl
Atlas oddziaływań obejmujący cały rodzaj wśród orthoflawiwirusowych ortologów identyfikuje zachowaną rolę ufmylacji w replikacji ortoflawiwirusów
Dlaczego to badanie wirusa ma znaczenie
Wirusy takie jak dengue, Zika i wirus Zachodniego Nilu rozprzestrzeniają się na nowe tereny i mogą powodować dolegliwości od gorączki po zapalenia mózgu i wady wrodzone. Wciąż jednak brakuje szeroko działających, pewnych terapii. Badanie to bada ukrytą współpracę między tymi wirusami a mało znanym komórkowym systemem znakowania o nazwie ufmylacja i w jaki sposób pomaga on patogenom w rozmnażaniu. Mapując tę relację w wielu spokrewnionych wirusach, autorzy odkrywają wspólną słabą stronę, którą można potencjalnie wykorzystać do opracowania przyszłych leków przeciwwirusowych.
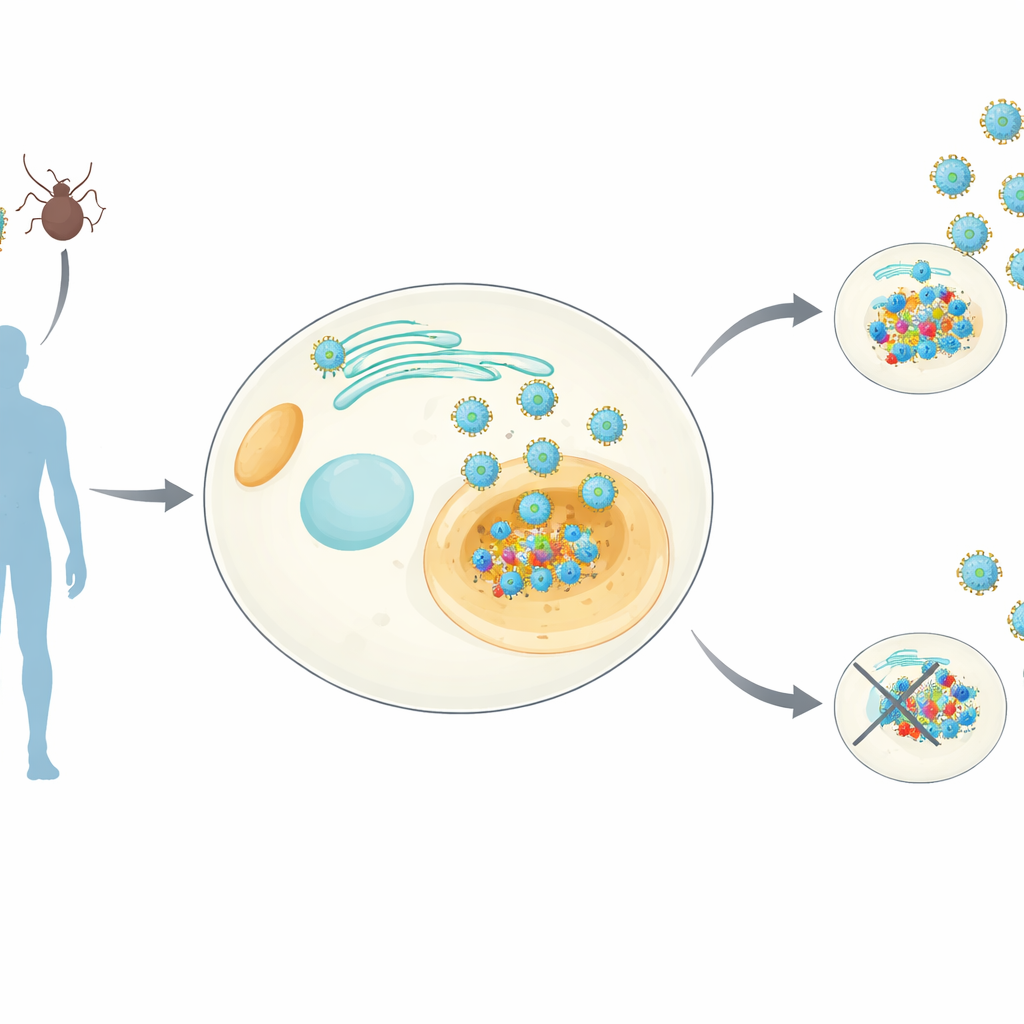
W ślad za kluczowym wirusowym informantem
Ortoflawiwirusy – grupa obejmująca dengue, Zikę, żółtą febrę i inne – wszystkie noszą niewielkie białko NS4B, które osadza się w błonach wewnątrz naszych komórek. Wiadomo, że NS4B jest niezbędne do replikacji wirusa, ale jego dokładne funkcje pozostawały niejasne. Naukowcy stworzyli linie komórkowe ludzkie trwale produkujące NS4B pochodzące od ośmiu różnych ortoflawiwirusów. Następnie zastosowali czułe techniki spektrometrii mas, aby wyłapać NS4B wraz z ludzkimi białkami z nim związanymi, a równolegle zmierzyli, jak ekspresja NS4B zmienia ogólny skład białek w komórce. To pozwoliło stworzyć obejmujący cały rodzaj „atlas interakcji” – który nazwali NS4Bome – ukazujący zarówno wspólne, jak i specyficzne dla wirusa cele gospodarza.
Wspólne sztuczki i specyficzne modyfikacje
Atlas ujawnił 538 ludzkich białek wchodzących w interakcje z NS4B oraz ponad 500 białek, których obfitość zmienia się w obecności NS4B. Wiele z nich skupia się w szlakach zarządzających produkcją energii w mitochondriach, kształtowaniem błon wewnętrznych oraz ruchem nowo syntetyzowanych białek i lipidów. Niektóre interakcje występowały u większości wirusów, co sugeruje ewolucyjnie zachowane mechanizmy wykorzystywane przez wszystkie ortoflawiwirusy. Inne pojawiały się tylko w niektórych gatunkach lub szczepach, co może tłumaczyć, dlaczego niektóre wirusy preferują komary zamiast kleszczy lub powodują choroby mózgu zamiast gorączki krwotocznej. To systematyczne spojrzenie porządkuje dotychczasowy, fragmentaryczny zbiór badań, tworząc spójną mapę tego, jak te wirusy przestawiają funkcjonowanie komórki.
Zaskakujący sojusznik: system ufmylacji
Wśród licznych partnerów, do których przyłączało się NS4B, wyróżnił się jeden: UBA5, enzym startowy szlaku ufmylacji. Ufmylacja to komórkowy system przyłączający małą znaczącą jednostkę białkową, UFM1, do wybranych celów, wpływając na procesy takie jak kontrola jakości białek i odpowiedzi na stres. Przy użyciu interferencji RNA i genowych knockoutów opartych na CRISPR zespół wykazał, że komórki pozbawione UBA5 lub w inny sposób niezdolne do przeprowadzenia ufmylacji miały znacznie zmniejszoną replikację Ziki i kilku pokrewnych wirusów. Ponowne wprowadzenie prawidłowego UBA5 przywróciło wzrost wirusa, natomiast formy mutantów, które nie mogły już przeprowadzać ufmylacji, tego nie robiły, dowodząc, że sama aktywność znakowania jest kluczowa dla infekcji.
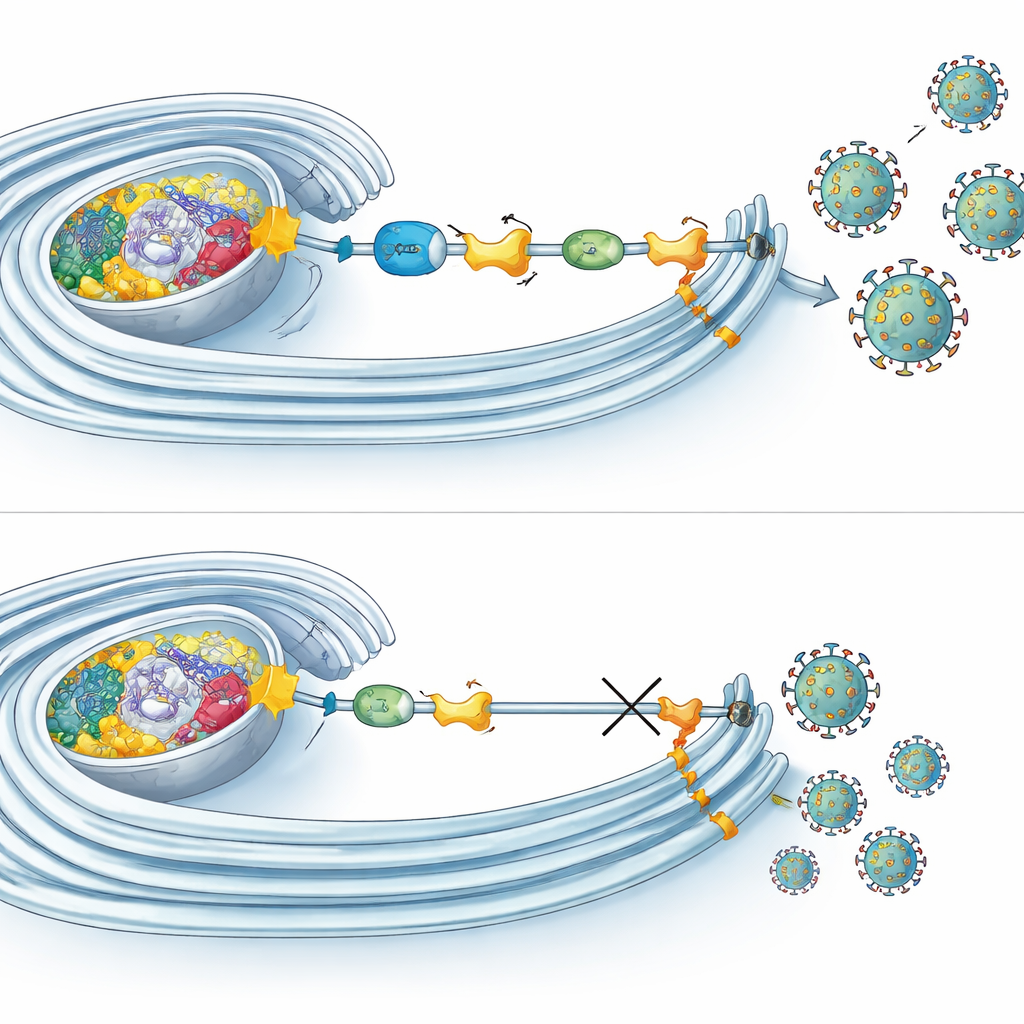
Jak znakowanie wspiera fabryki wirusowe
Mikroskopia i eksperymenty biochemiczne wykazały, że liczne składniki ufmylacji gromadzą się w miejscach, gdzie RNA wirusowe jest kopiowane wewnątrz przebudowanych błon. Tam wiążą się nie tylko z NS4B, ale także z innymi białkami wirusowymi budującymi maszynerię replikacyjną. Co ciekawe, zahamowanie ufmylacji nie zatrzymało wejścia wirusa, produkcji RNA ani syntezy białek. Zamiast tego głównie osłabiło późne etapy cyklu, takie jak składanie lub uwalnianie zakaźnych cząstek. Równocześnie ufmylacja wpływała na „oddychanie” mitochondriów: po wyłączeniu tego szlaku komórki wykazywały obniżone zużycie tlenu i zmienione kształty mitochondriów. Natomiast we wczesnej fazie zakażenia Ziką oddychanie mitochondrialne nasilało się, co sugeruje, że wirusy mogą wykorzystywać ufmylację, by zwiększyć wydajność energetyczną komórki dokładnie wtedy, gdy najbardziej ich to wspiera.
Testowanie leku w komórkach i w małych rybkach
Autorzy zwrócili się następnie ku związku małocząsteczkowemu DKM 2-93, który blokuje miejsce aktywne UBA5. W hodowanych komórkach ludzkich ten inhibitor zmniejszył produkcję wirusa Zika około dziesięciokrotnie przy dawkach, które pozostawiały komórki w dużej mierze zdrowe, i wykazywał aktywność w kilku typach komórek. Aby sprawdzić, czy ta strategia może działać w organizmie, użyto modelu zakażenia Ziką u danio pręgowanego (zebrafish), który odzwierciedla kluczowe cechy choroby w rozwijającym się mózgu. Leczenie zainfekowanych embrionów DKM 2-93 w trakcie wczesnego rozwoju mózgu znacznie obniżyło poziomy RNA wirusowego i zmniejszyło odsetek rybek wykazujących poważne deformacje, co wskazuje na rzeczywistą korzyść przeciwwirusową in vivo.
Co to oznacza dla przyszłych terapii
Tworząc kompleksową mapę tego, jak NS4B z wielu ortoflawiwirusów wchodzi w interakcje z ludzkimi białkami, badanie to wskazuje ufmylację jako zachowany szlak wspomagający, od którego wirusy te zależą przy produkcji zakaźnych cząstek. Ponieważ ten sam układ gospodarza wydaje się wspierać dengue, Zikę, wirusa Zachodniego Nilu i inne, leki selektywnie osłabiające ufmylację mogłyby działać jako środki o szerokim spektrum przeciwwirusowym, zamiast celować w pojedynczy wirus. Choć potrzeba dalszych badań, by ustalić, które białka są znakowane i zapewnić bezpieczeństwo, wyniki wskazują obiecujący cel oparty na gospodarzu, który pewnego dnia mógłby pomóc złagodzić ogniska wielu chorób przenoszonych przez komary i kleszcze za pomocą jednej terapii.
Cytowanie: Rajasekharan, S., Barragan Torres, V.A., Pinheiro Gomes, Y.C. et al. A genus-wide interaction atlas across NS4B orthologues identifies a conserved role for UFMylation in orthoflavivirus replication. Nat Commun 17, 2489 (2026). https://doi.org/10.1038/s41467-026-70437-9
Słowa kluczowe: wirusa Zika, dengue, interakcje gospodarza i wirusa, ufmylacja, leki przeciwwirusowe o szerokim spektrum