Clear Sky Science · pl
Fotochemiczne klatki składane dynamicznie, działające w wodzie przy świetle widzialnym
Formowanie maleńkich pojemników reagujących na światło
Wyobraź sobie, że leki, czujniki lub katalizatory można by włączać i wyłączać w organizmie, po prostu naświetlając je bezpiecznym, kolorowym światłem. W tej pracy opisano maleńkie, puste molekuły—„klatki”—które samorzutnie się składają i przeorganizowują pod wpływem światła, nawet w wodzie i przy użyciu światła czerwonego, które przenika przez tkanki. Te inteligentne pojemniki zachowują się niczym proste maszyny: zmieniają kształt, przechodzą między środowiskami oleistymi a wodnymi i wchodzą w interakcje z jonami metali lub innymi partnerami, wszystko pod zewnętrzną kontrolą.
Dlaczego klatki sterowane światłem mają znaczenie
Komórki żywe opierają się na niezliczonych strukturach molekularnych, które szybko dostosowują się do zmieniających się warunków. Chemicy od dawna dążą do stworzenia sztucznych nanostruktur zdolnych do podobnej adaptacji: reagowania na sygnały takie jak pH, temperatura czy związki chemiczne oraz zmiany tego, co wiążą lub jak się zachowują. Światło jest szczególnie atrakcyjnym sygnałem, ponieważ można je stosować z dużą precyzją w czasie i przestrzeni i nie pozostawia śladów. Jednak większość fotoreaktywnych molekularnych klatek działa tylko w rozpuszczalnikach organicznych i często wymaga szkodliwego promieniowania ultrafioletowego, nieodpowiedniego dla zastosowań biologicznych. Ta praca rozwiązuje oba problemy, projektując klatki reagujące na światło widzialne i czerwone oraz działające w wodzie, co daje obiecujące perspektywy dla zastosowań biomedycznych i technologicznych.
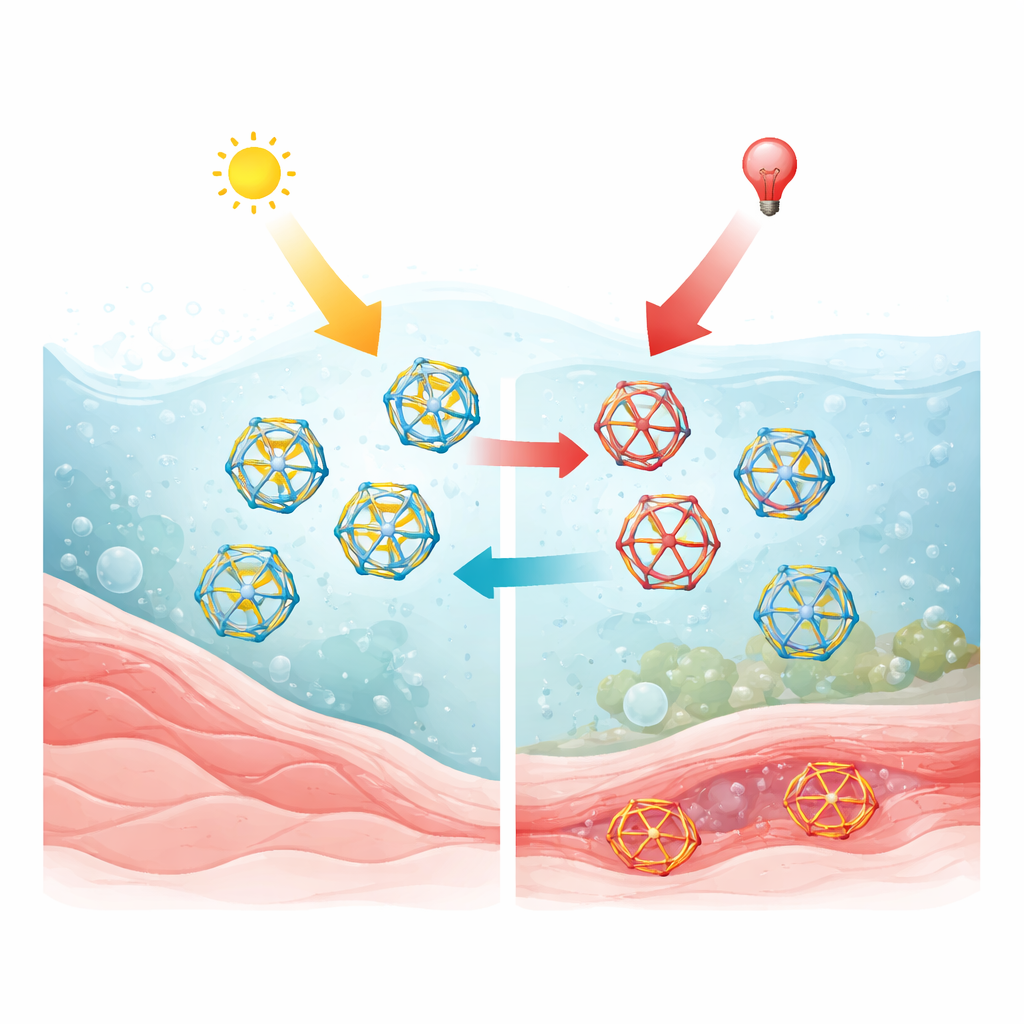
Budowa klatek, które przekonfigurują się pod wpływem światła
Badacze zaczynają od specjalnego „przełącznika fotochemicznego” opartego na azobenzenie, cząsteczce, która pod wpływem różnych kolorów światła może zmieniać kształt. Dołączają grupy aldehydowe, tworząc elementy budulcowe, które mogą łączyć się z trójramienną aminą za pomocą odwracalnych wiązań chemicznych, co pozwala fragmentom samo składać się w dobrze zdefiniowane, puste klatki. W pierwszym układzie trzy fluorowane filary azobenzenowe i dwa centra aminowe spontanicznie tworzą dynamiczną klatkę w roztworze. Światło czerwone (około 660 nm) zgina wszystkie trzy filary, delikatnie napinając struktury klatki, podczas gdy fioletowe lub zielone światło przywraca je do pierwotniejszego, bardziej zrelaksowanego kształtu. Ponieważ rama klatki utrzymuje przełączniki w określonym ułożeniu, wpływa to na efektywność i kompletność fotochemicznych przemian, prowadząc do wyraźnej, przewidywalnej odpowiedzi na światło.
Zamknięcie kształtu i działanie w wodzie
Aby przejść od kruchej, ciągle przeorganizowującej się sieci do odpornego urządzenia, autorzy chemicznie „zamrażają” dynamiczne wiązania, przekształcając je w trwałe połączenia i otrzymując stabilną klatkę kowalencyjną. Ta zablokowana klatka nadal może przełączać się między kształtami sterowanymi światłem, ale teraz bez rozpadu. Kluczowym zabiegiem jest protonacja: gdy klatka staje się naładowana dodatnio przez kwas, rozpuszcza się w wodzie i można ją odwracalnie przemieszczać między warstwą organiczną a wodną przez napuszczanie dwutlenku węgla, a następnie jego uwolnienie. W wodzie klatka pozostaje fotoswitchowalna przy świetle widzialnym i potrafi nawet tworzyć kompleksy inkluzyjne z gospodarzami takimi jak kukurbituryle, co sugeruje, że może przenosić lub wchodzić w interakcje z gośćmi we wnętrzu. Testy toksyczności w hodowlach komórek ludzkich pokazują, że przy niskich stężeniach submikromolowych sprotonowana klatka jest kompatybilna z komórkami, co sugeruje możliwość zastosowań biologicznych przy starannie dobranych dawkach.
Sięgając ku bliskiemu podczerwonemu i komunikując się z metalami
Aby przesunąć sterowanie głębiej w biologicznie użyteczne „okno terapeutyczne” światła, zespół zaprojektował drugi element azobenzenowy z atomami chloru. Ta odmiana może być przełączana w obu kierunkach wyłącznie światłem czerwonym i bliską podczerwienią, bez użycia wyższej energii. Tworzy także własną rodzinę klatek, chociaż bardziej masywne atomy chloru sprawiają, że są one bardziej zatłoczone i skłonne do częściowego otwarcia lub przeorganizowania. Mieszając elementy fluorowane i chlorowane, naukowcy stworzyli hybrydowe klatki, które zmieniają skład w odpowiedzi na światło i ciepło. Pokazali również, że podobne ramy klatkowe zbudowane z nieruchomej jednostki bipirydynowej działają jako wielowartościowe ligandy dla jonów metali takich jak żelazo, tworząc barwne kompleksy, które łatwo przechodzą do wody. Gdy jednostki wiążące metale są wymieniane w fotoreaktywnych klatkach, jony metali stają się dodatkowym narzędziem do kierowania lokalizacją i zachowaniem zestawień.
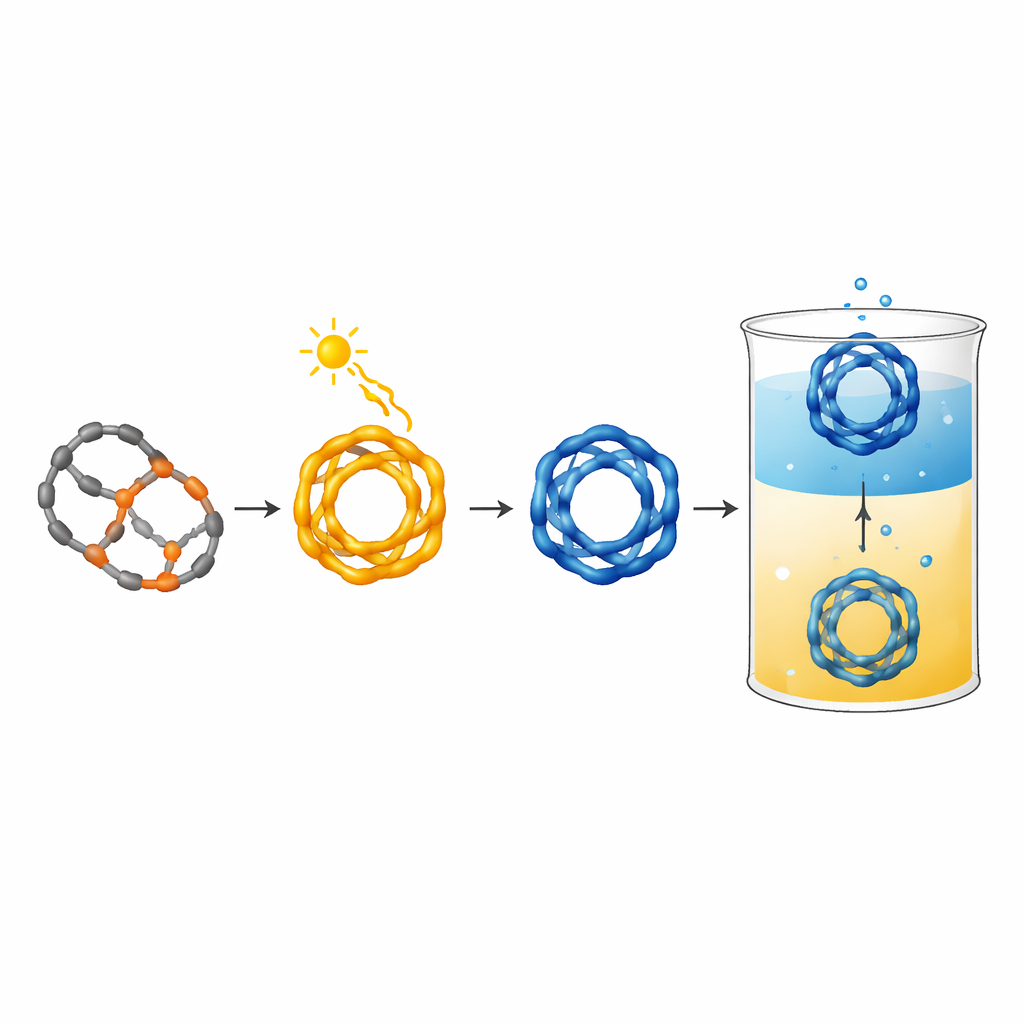
Od maleńkich klatek do maszyn przypominających żywe systemy
Razem te eksperymenty wyznaczają zasady projektowania molekularnych klatek, które składają się samodzielnie, reagują przewidywalnie na światło widzialne i czerwone oraz działają w wodzie, także w warunkach naśladujących środowisko biologiczne. Łącząc odwracalne samozłożenie z krokami „zabezpieczającymi” na stałe oraz integrując wiele wyzwalaczy, takich jak kolor światła, kwasowość, dwutlenek węgla i jony metali, autorzy przybliżają się do molekularnych maszyn zdolnych do adaptacji na sposób przypominający żywe układy. W dłuższej perspektywie takie klatki mogłyby służyć jako sterowane nośniki leków, regulowane nanoreaktory do reakcji chemicznych lub reagujące czujniki wewnątrz żywych systemów, wszystkie kierowane z zewnątrz przez starannie dobrane barwy światła.
Cytowanie: Schäfer, V., Seliwjorstow, A., Fuhr, O. et al. Dynamically assembled photochromic cages operational in water with visible light. Nat Commun 17, 2488 (2026). https://doi.org/10.1038/s41467-026-70406-2
Słowa kluczowe: fotochemiczne molekularne klatki, nanotechnologia reagująca na światło, przełączanie przy świetle widzialnym i czerwonym, samozłożenie w wodzie, przełączniki azobenzenowe