Clear Sky Science · pl
snRNA zakończone przez CPF‑CF przemieszczają się przez cytoplazmę za pośrednictwem mechanizmu nadzoru z udziałem białka‑strażnika mRNA
Jak malutkie RNA‑przewodniki robią niespodziewany objazd
W każdej komórce synteza białek opiera się na precyzyjnym molekularnym układzie. Kluczową rolę w tym tańcu odgrywają małe jądrowe RNA, czyli snoRNA, które pomagają kształtować rybosomy — maszynerię budującą białka. Badanie to ujawnia, że część tych drobnych przewodników niespodziewanie opuszcza jądro, krótko odwiedza cytoplazmę, a następnie wraca, i wszystko to z powodu sposobu, w jaki kończona jest ich produkcja. Zrozumienie tej ukrytej trasy ruchu rzuca światło na mechanizmy ochrony jakości RNA i utrzymania integralności informacji genetycznej.
Bliższe spojrzenie na pomocników RNA w komórce
SnoRNA to krótkie cząsteczki RNA pełniące rolę przewodników, kierujących chemicznymi modyfikacjami innych RNA, zwłaszcza tych tworzących rybosomy. W komórkach drożdży większość snoRNA powstaje w jądrze i są uważane za trwale tam pozostające, tworząc stabilne kompleksy z określonymi białkami — snoRNPy — które modyfikują rRNA. Jednak wcześniejsze badania wykryły interakcje snoRNA z białkami zwykle zaangażowanymi w eksport mRNA z jądra. To zagadkowe spostrzeżenie postawiło pytanie: czy snoRNA czasem przemieszczają się do cytoplazmy, a jeśli tak, to dlaczego?
Odkrywanie snoRNA w ruchu
Ponowna analiza danych sekwencjonowania RNA z precyzyjnie oddzielonych frakcji jądrowych i cytoplazmatycznych wykazała, że wiele snoRNA faktycznie występuje w cytoplazmie normalnych komórek drożdży, na poziomach podobnych do typowych mRNA. Gdy zablokowano kluczowe czynniki eksportu, Mex67 i Xpo1, pula cytoplazmatyczna snoRNA zmalała, a w jądrze nagromadziły się niedojrzałe prekursory snoRNA z przedłużonym końcem 3′. Mikroskopia z użyciem sond fluorescencyjnych potwierdziła tę zmianę: sygnały, które normalnie pojawiały się zarówno w nukleolusie, jak i słabo w cytoplazmie, stały się silnie jądrowe po zablokowaniu eksportu. Wyniki te pokazują, że podzbiór snoRNA, często nadal noszący dodatkową sekwencję na końcach, jest aktywnie transportowany poza jądro, a nie jedynie przecieka lub jest zanieczyszczeniem próbek.
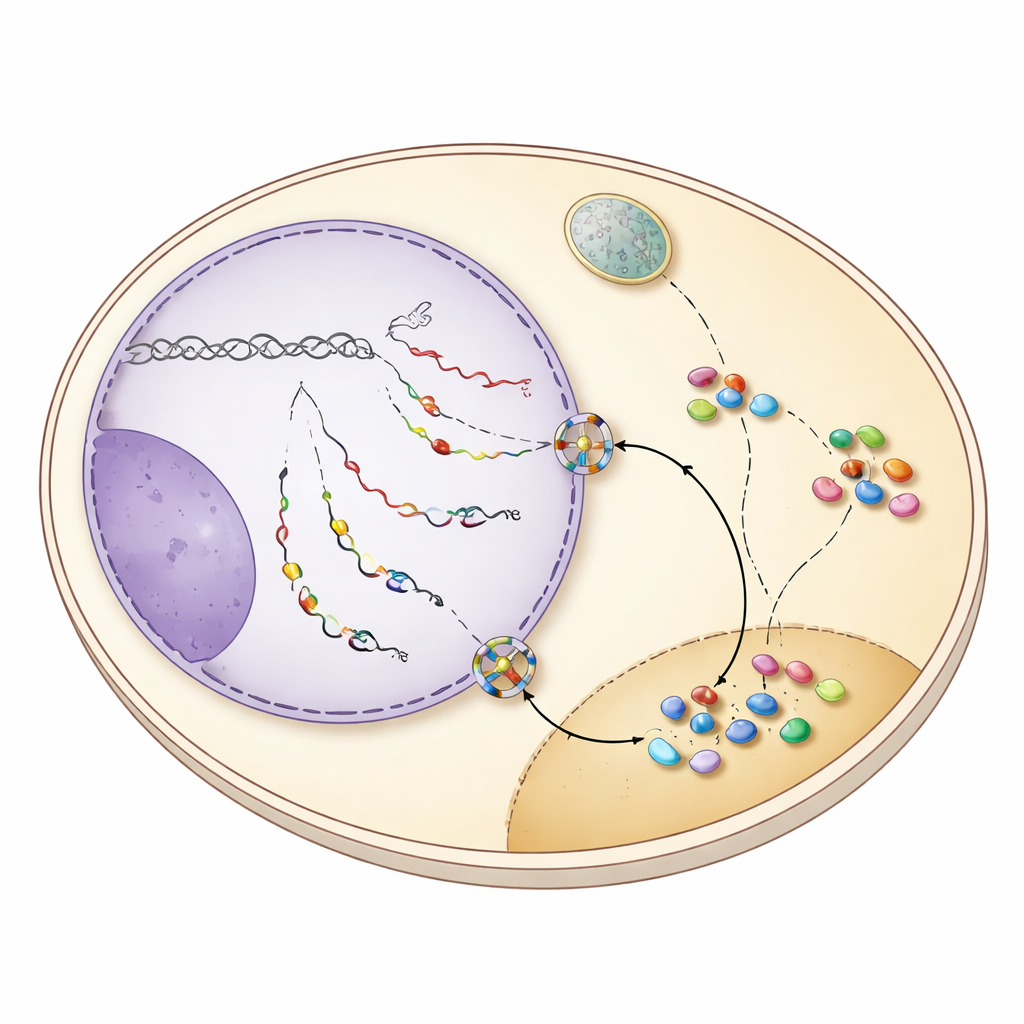
Przełączenie przez białko‑strażnika, które wysyła snoRNA na zewnątrz
Klucz do tego przemieszczania leży w sposobie zakończenia transkrypcji snoRNA. U drożdży większość snoRNA jest normalnie odcinana od maszynerii transkrypcyjnej przez system zwany NNS, który pozostawia krótki ogonek szybko przycinany w jądrze. Wiele genów snoRNA ma jednak też zapasowe sygnały stop rozpoznawane przez drugi system, CPF‑CF, najlepiej znany z kończenia mRNA i doklejania długich ogonków poli(A). Gdy terminacja przez NNS zawodzi, transkrypty snoRNA biegają dalej do tych dalszych miejsc CPF‑CF i otrzymują dłuższy ogonek. Taka zmieniona końcówka rekrutuje zestaw „białek‑strażników” — w tym Hrp1 i Nab2 — które sprawdzają poprawne przetwarzanie i jednocześnie przyciągają czynnik eksportu Mex67. Badanie pokazuje, że gdy snoRNA są kończone przez CPF‑CF, białka‑strażnicy i Mex67 współdziałają, by wysłać te ogoniaste snoRNA przez pory jądrowe do cytoplazmy.
Bilety w obie strony i kontrola jakości
Po dotarciu do cytoplazmy snoRNA nie są pozostawione bez opieki. Pozostają związane z ochronnym pierścieniem białek Lsm oraz czynnikiem Lhp1, które osłaniają podatny koniec RNA. Te cechy umożliwiają dwóm receptorom importowym, Cse1 i Mtr10, rozpoznanie przemieszczających się snoRNA i sprowadzenie ich z powrotem do jądra. Gdy autorzy wyłączyli te czynniki importu lub pierścień Lsm, niedojrzałe snoRNA nagromadziły się w cytoplazmie, co potwierdza, że ten mechanizm mediował ich powrót. Z powrotem w jądrze długie ogonki są przycinane przez jądrowy egzosom, podstawowe białka snoRNP są w pełni składane, a dojrzałe kompleksy przemieszczają się do nukleolusu. Co ważne, snoRNA, które odbyły tę przerwę w podróży, pozostały w pełni funkcjonalne: modelowy snoRNA, snR13, nadal przeprowadzał swoje specyficzne modyfikacje chemiczne na rRNA po zakończeniu przez CPF‑CF i przejściu przez cytoplazmę.
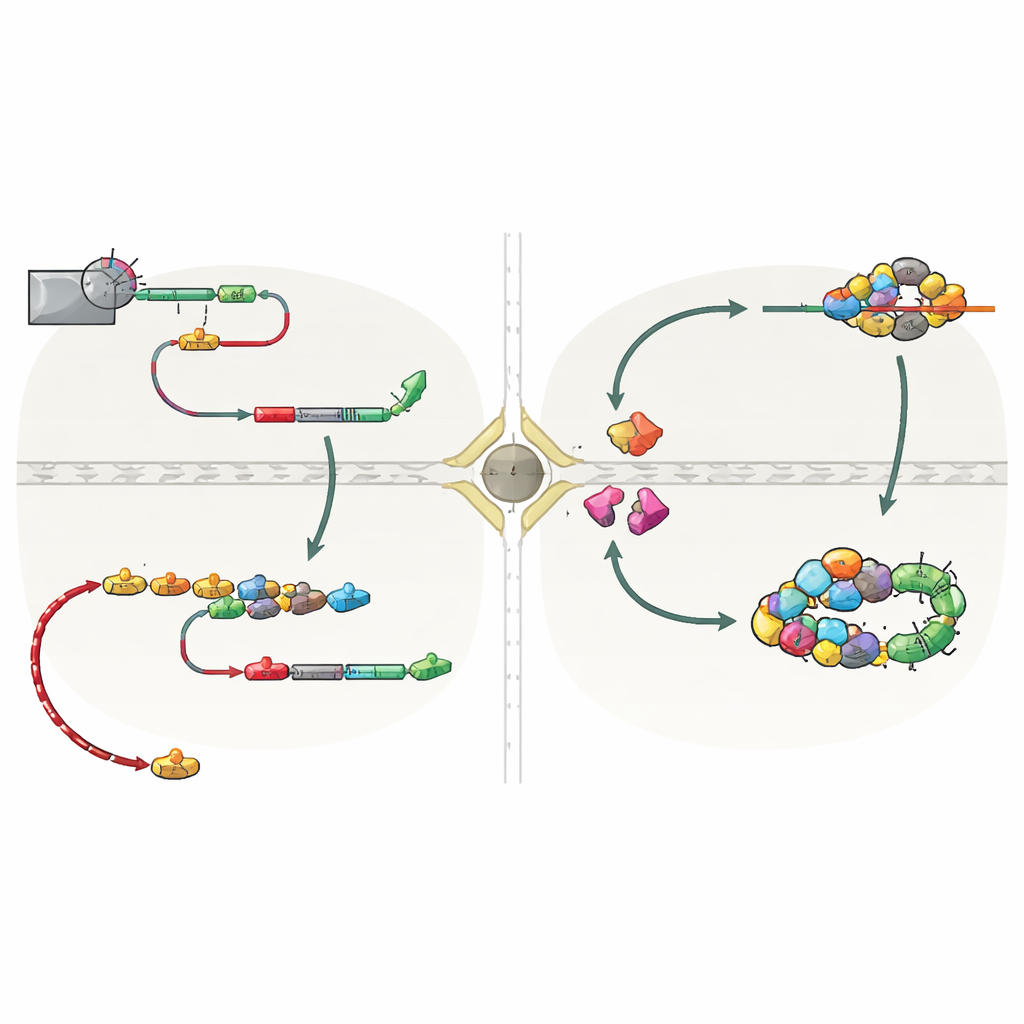
Dlaczego ta ukryta ścieżka ma znaczenie
Praca ta ujawnia, że podróże snoRNA nie są wyjątkiem, lecz wbudowaną ścieżką zapasową kontrolowaną sposobem zakończenia transkrypcji. Gdy podstawowy system NNS jest osłabiony — na przykład w określonych fazach cyklu komórkowego — sygnały CPF‑CF położone dalej ratują produkcję snoRNA. Zapobiega to marnowaniu już zsyntetyzowanego RNA oraz niekontrolowanej transkrypcji, która mogłaby zakłócać sąsiednie geny i uszkadzać DNA. Autorzy znajdują także poszlaki podobnego mechanizmu u komórek ludzkich, gdzie indywidualnie kodowane snoRNA mogą nabywać ogonki poli(A) w pokrewnych miejscach. Mówiąc prościej: to, który „sygnał stop” zostanie wybrany na końcu genu snoRNA, decyduje, czy to RNA spokojnie dojrzewa w jądrze, czy krótko opuszcza je i wraca pod czujnym okiem białek‑strażników. Ten mechanizm nadzoru napędzany terminacją transkrypcji pomaga utrzymać krajobraz RNA komórki elastycznym i bezpiecznym.
Cytowanie: Yu, F., Zaccagnini, G., Duan, Y. et al. CPF-CF-terminated snoRNAs shuttle through the cytoplasm via an mRNA guard protein-mediated surveillance mechanism. Nat Commun 17, 2328 (2026). https://doi.org/10.1038/s41467-026-70373-8
Słowa kluczowe: snoRNA, kontrola jakości RNA, eksport jądrowy, terminacja transkrypcji, genetyka drożdży