Clear Sky Science · pl
Synchroniczna aktywacja cholinergicznych interneuronów prążkowia wywołuje lokalne uwalnianie serotoniny
Dlaczego to odkrycie w chemii mózgu ma znaczenie
Nawyki, motywacja i zachowania kompulsywne zależą od niewielkiego, ale kluczowego obszaru mózgu zwanego prążkowiem. Dwa dobrze znane przekaźniki, dopamina i serotonina, modulują to miejsce, a wiele leków psychiatrycznych ma na celu przywrócenie ich równowagi. Badanie ujawnia wcześniej nieznaną linię komunikacji: specjalna klasa komórek nerwowych uwalniających acetylocholinę może bezpośrednio oddziaływać na włókna serotoninowe i powodować zwiększone uwalnianie serotoniny, lecz tylko w określonej części prążkowia. To nowo odkryte powiązanie może pomóc wyjaśnić, dlaczego zaburzenia takie jak zaburzenie obsesyjno‑kompulsyjne (OCD) i choroba Parkinsona często wiążą się z równoczesnymi zaburzeniami kilku neuroprzekaźników.
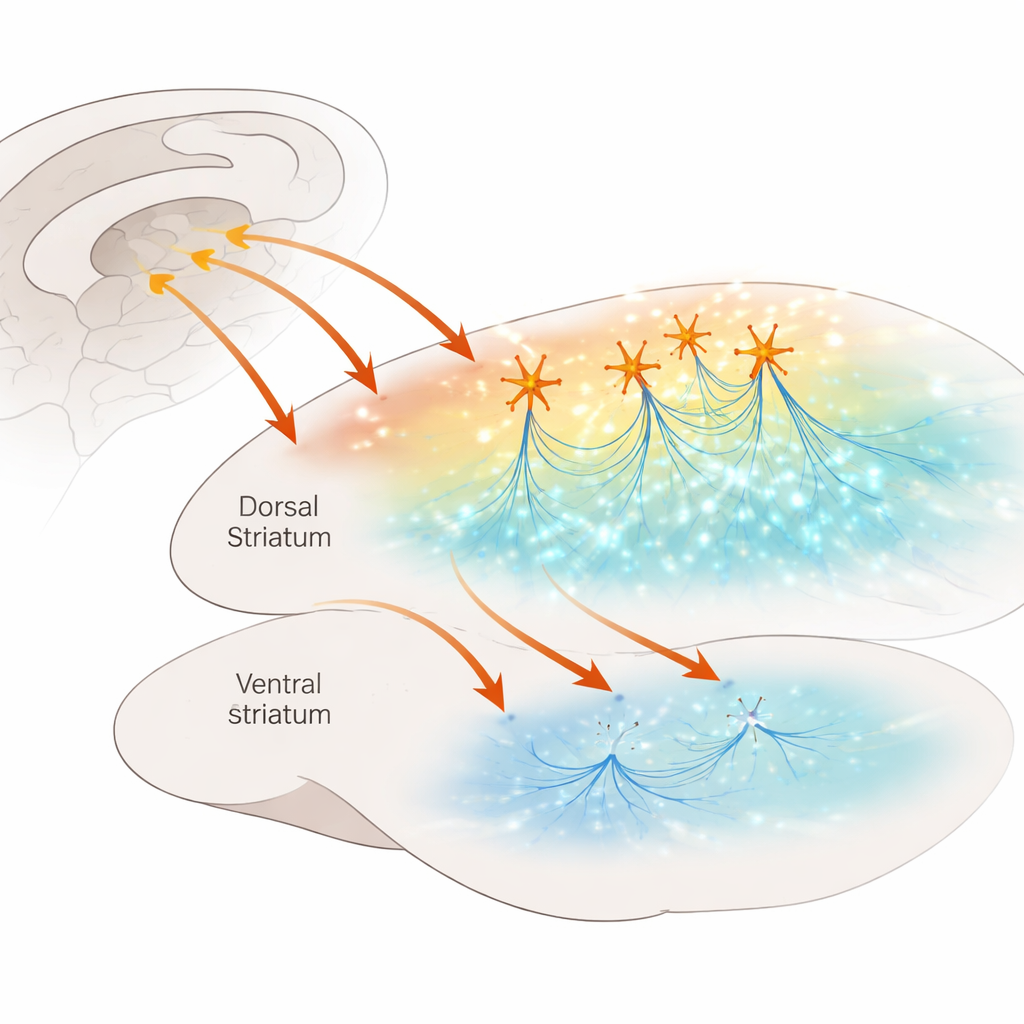
Ruchliwe skrzyżowanie w mózgu
Grzbietowe prążkowie pełni rolę węzła decyzyjnego, pomagając nam przełączać się między działaniami celowymi a automatycznymi nawykami. Otrzymuje gęste wkłady z kory i jest „kąpany” w neuromodulatorach, takich jak dopamina i serotonina, które precyzyjnie dostrajają przetwarzanie sygnałów. W tym węźle znajduje się rzadka, lecz potężna populacja interneuronów cholinergicznych — komórek uwalniających acetylocholinę, które wyładowują regularnie niczym małe metronomy. Wcześniejsze badania pokazały, że kiedy te komórki wyładowują jednocześnie, mogą znacznie zwiększać uwalnianie dopaminy poprzez działanie na nikotynowe receptory acetylocholinowe umieszczone na włóknach dopaminowych. Czy podobne skróty istnieją dla serotoniny, pozostawało nieznane, mimo że serotonina odgrywa kluczową rolę w nastroju, uczeniu się i w efektach leków stosowanych w OCD i depresji.
Obserwowanie rozświetlania serotoniny w czasie rzeczywistym
Aby rozwiązać to pytanie, badacze użyli myszy, w których fluorescencyjny sensor jaśniał mocniej w obecności serotoniny. Wstrzyknęli wirusa niosącego ten sensor do prążkowia, przygotowali cienkie plastry mózgu, a następnie zastosowali mikroskopię dwu‑fotoniczną, by obserwować sygnały serotoniny podczas stymulacji tkanki. Stymulacja elektryczna wewnątrz grzbietowego prążkowia wywoływała wyraźne, wolno wygasające błyski aktywności sensora serotoniny. Gdy zespół podał lek blokujący nikotynowe receptory acetylocholinowe, te błyski zmniejszały się i stawały się bardziej przestrzennie ograniczone, co wskazuje, że acetylocholina działająca przez te receptory pomaga zarówno zwiększyć uwalnianie serotoniny, jak i rozprzestrzeniać je na szerszy obszar. Co ciekawe, wykonanie tego samego eksperymentu w brzusznym prążkowiu — pobliskim regionie o jeszcze gęstszych połączeniach serotoninowych — nie wykazało takiego wkładu nikotynowego, ujawniając, że ta komunikacja jest specyficzna dla regionu.
Wywoływanie serotoniny przy użyciu precyzyjnego światła
Aby sprawdzić, czy sama acetylocholina z interneuronów cholinergicznych może napędzać uwalnianie serotoniny, autorzy zastosowali optogenetykę. Zaprojektowali te interneurony tak, by reagowały na krótkie błyski niebieskiego lub żółtego światła i aktywowali je synchronicznie, jednocześnie nadal monitorując sensor serotoniny. Pojedynczy milisekundowy błysk światła wystarczył, by wywołać silny sygnał serotoniny w grzbietowym prążkowiu, o przebiegu czasowym podobnym do nikotynowo‑wrażliwej składowej odpowiedzi wywołanej elektrycznie. Zablokowanie receptorów nikotynowych niemal całkowicie zlikwidowało ten sygnał, nawet gdy inne chemiczne wejścia i receptory w plastrze były farmakologicznie wyciszone. To połączenie precyzyjnej stymulacji i blokady receptorów wykazało, że acetylocholina działa bezpośrednio na nikotynowe receptory wzdłuż włókien serotoninowych, wyzwalając lokalne uwalnianie serotoniny, zamiast polegać na pośrednich drogach przez inne typy komórek czy aksony dopaminowe.
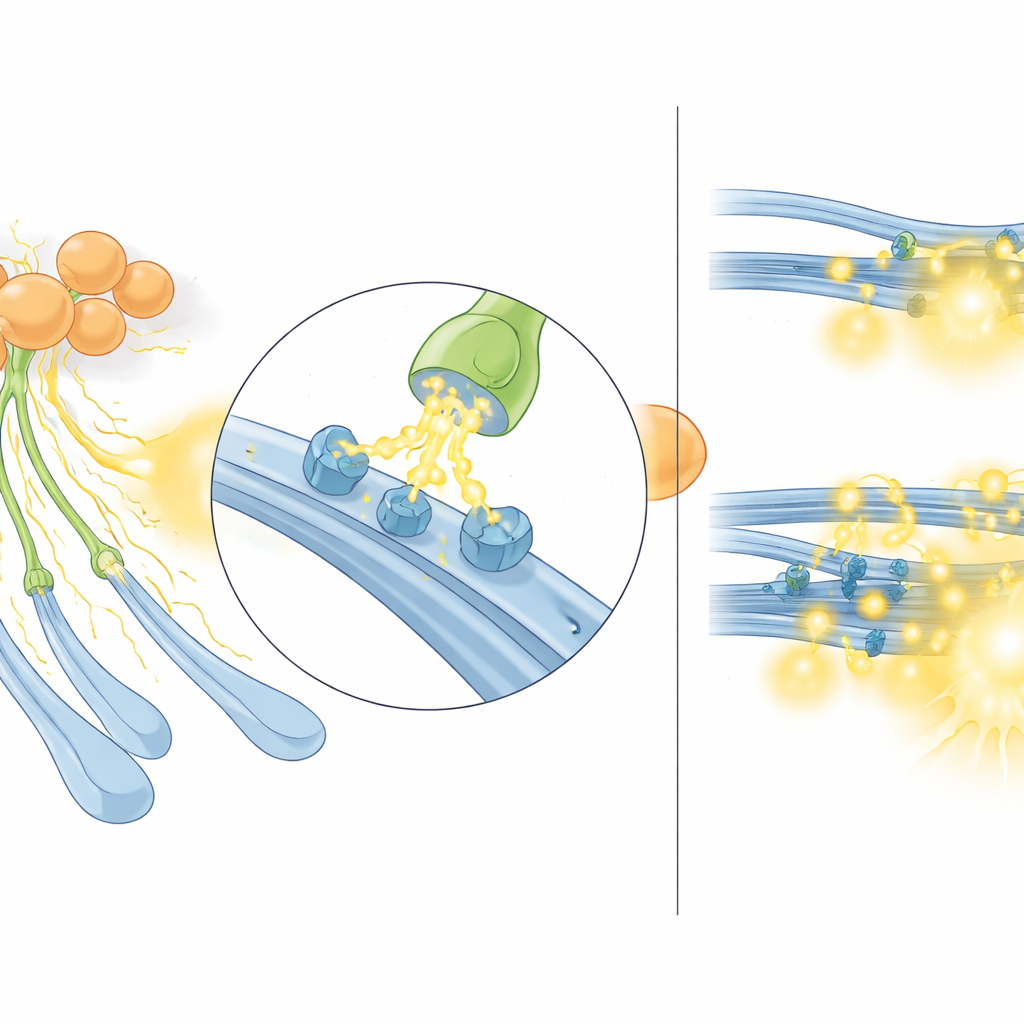
Gdy system działa zbyt intensywnie
Zespół zapytał następnie, co się dzieje w stanie istotnym dla choroby, gdy sygnalizacja acetylocholiny jest patologicznie wzmocniona. Użyli myszy z wyciszeniem Sapap3 (knockout), dobrze znanego modelu wykazującego nadmierne pielęgnowanie i inne zachowania przypominające OCD, u których wcześniej stwierdzono większą aktywność interneuronów cholinergicznych i wyższe uwalnianie acetylocholiny. U tych myszy stymulacja elektryczna grzbietowego prążkowia wywoływała silniejsze sygnały sensora serotoniny niż u zwierząt kontrolnych. Co ważne, ta różnica znikała po zablokowaniu receptorów nikotynowych, co oznacza, że tylko acetylocholinowo‑zależna część uwalniania serotoniny była zwiększona. Podobny wzorzec obserwowano dla dopaminy. Innymi słowy, w tym hipercholinergicznym stanie interneurony cholinergiczne nieproporcjonalnie wzmacniają nikotynową składową uwalniania monoamin, efektywnie pozwalając acetylocholinie „przejąć” włókna serotoninowe jako główną drogę wydzielania serotoniny.
Szerokie implikacje dla zaburzeń mózgu
Te wyniki ujawniają precyzyjnie regulowaną i regionalnie ograniczoną rozmowę między acetylocholiną a serotoniną w grzbietowym prążkowiu. W zdrowych mózgach synchroniczne wybuchy aktywności interneuronów cholinergicznych — na przykład wywołane nagłymi, behawioralnie istotnymi zdarzeniami — mogą tymczasowo poszerzać i wzmacniać sygnały serotoninowe, kształtując sposób, w jaki działania są uczone lub hamowane. W stanach patologicznych, gdy acetylocholina jest przewlekle podwyższona, jak u myszy Sapap3 i być może w stanach takich jak OCD czy choroba Parkinsona, ten sam mechanizm może się wyolbrzymić, przyczyniając się do nieprawidłowych wzorców sygnalizacji serotoniny i dopaminy. Zrozumienie tego ukrytego połączenia oferuje nowe spojrzenie na to, jak różni neuromodulatorzy współdziałają w zachowaniu i chorobie, i może ostatecznie wskazać kierunki terapii celujących precyzyjniej w ich wspólną dynamikę, zamiast traktować każdy związek chemiczny oddzielnie.
Cytowanie: Matityahu, L., Hobel, Z.B., Berkowitz, N. et al. Synchronous activation of striatal cholinergic interneurons induces local serotonin release. Nat Commun 17, 2278 (2026). https://doi.org/10.1038/s41467-026-70359-6
Słowa kluczowe: serotonina prążkowia, interneurony cholinergiczne, nikotynowe receptory acetylocholinowe, zaburzenie obsesyjno-kompulsyjne, zwoje podstawy