Clear Sky Science · pl
Fragmenty SLIT3 orkiestrują rozwój nerwowo-naczyniowy i termogenezę w brunatnej tkance tłuszczowej
Jak nasz „dobry tłuszcz” pomaga nam zachować ciepło
Kiedy wchodzimy w chłód, nasze ciało szybko uruchamia mechanizmy podtrzymujące temperaturę. Kluczową rolę w tej odpowiedzi odgrywa brunatny tłuszcz, szczególny rodzaj tkanki tłuszczowej, który spala kalorie, by wytwarzać ciepło. To badanie ujawnia, w jaki sposób brunatna tkanka organizuje swoje drobne naczynia krwionośne i włókna nerwowe, by wzmocnić produkcję ciepła, odsłaniając ukrytą sieć komunikacji, którą w przyszłości można by wykorzystać do poprawy metabolizmu i leczenia chorób związanych z otyłością.
Ukryty piec wewnątrz ciała
Brunatna tkanka tłuszczowa, czyli brunatny tłuszcz, działa jak wewnętrzny piec. W przeciwieństwie do białej tkanki tłuszczowej, która magazynuje energię, brunatny tłuszcz zużywa paliwo, by generować ciepło przy ekspozycji na niskie temperatury. Aby robić to efektywnie, komórki brunatnego tłuszczu potrzebują bogatego ukrwienia dostarczającego tlen i składniki odżywcze oraz gęstej sieci nerwów sympatycznych, które sygnalizują, kiedy zwiększyć produkcję ciepła. W chłodzie te naczynia i nerwy rozrastają się w imponującym stopniu. Do tej pory nie było jednak jasne, jak poszczególne elementy tkanki tak precyzyjnie koordynują swój wzrost.
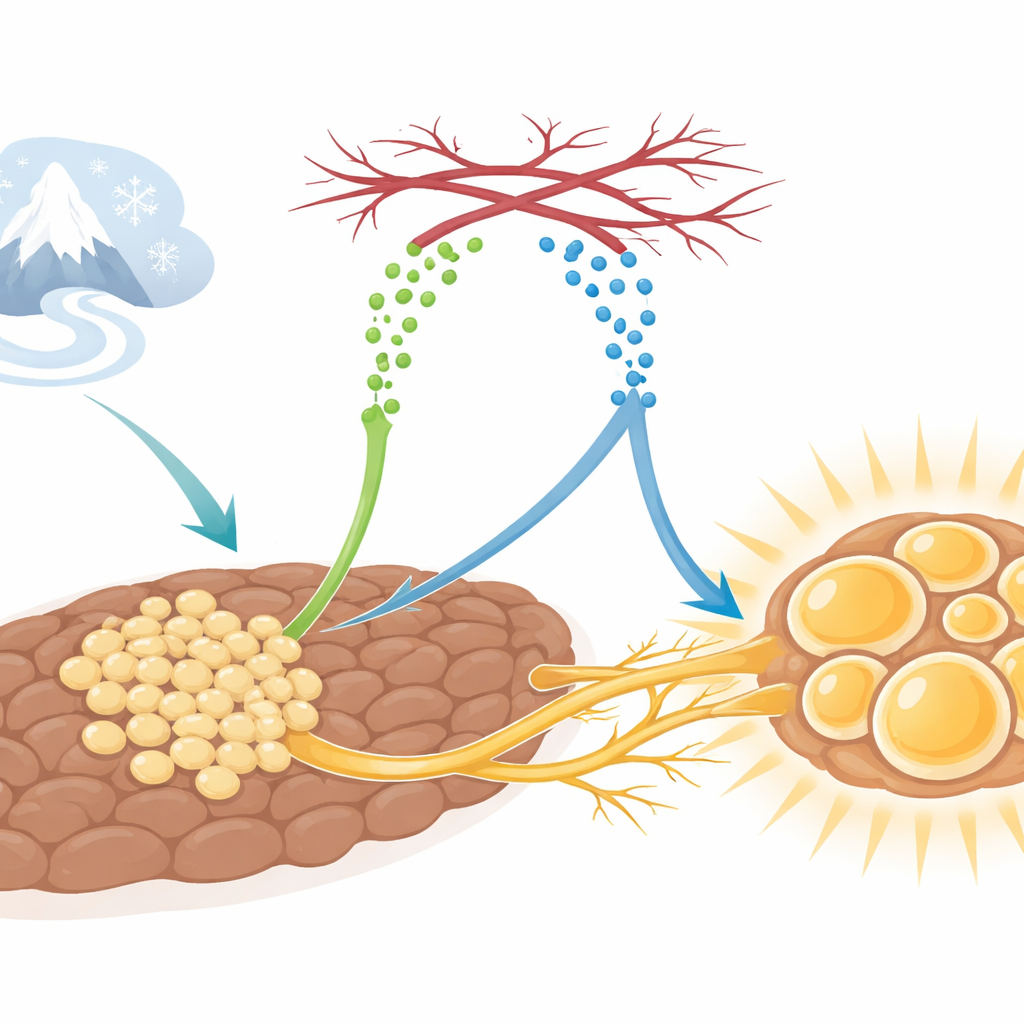
Cząsteczka-posłaniec, która uruchamia wszystko
Naukowcy odkryli, że białko o nazwie SLIT3, produkowane przez niedojrzałe komórki tłuszczowe zwane progenitorami adipocytów, odgrywa centralną rolę w tej koordynacji. U myszy wystawionych na zimno poziomy SLIT3 w brunatnej tkance rosną. Gdy zablokowano SLIT3 specyficznie w brunatnym tłuszczu lub w tych komórkach progenitorowych, zwierzęta miały trudności z utrzymaniem temperatury ciała w zimnie. Ich brunatna tkanka stała się „bielsza”, z większymi kroplami tłuszczu, niższą ekspresją genów produkujących ciepło, takich jak Ucp1, oraz z obniżonym wydatkiem energetycznym, mimo że spożycie pokarmu i aktywność pozostały niezmienione. To wskazywało na SLIT3 jako kluczowego organizatora odpowiedzi brunatnego tłuszczu na zimno — nie przez zmianę wewnętrznej maszynerii każdej komórki, lecz przez kształtowanie otaczającego mikrośrodowiska tkanki.
Wspólne budowanie naczyń i włókien nerwowych
Bliższe badania wykazały, że brunatna tkanka pozbawiona SLIT3 miała mniej drobnych naczyń krwionośnych i mniej włókien nerwów sympatycznych przecinających tkankę. Obrazowanie trójwymiarowe potwierdziło, że sieć nerwowa była wyraźnie rzadsza. Co istotne, gdy zwykły sygnał nerwowy został ominięty przy użyciu leku bezpośrednio aktywującego brunatny tłuszcz, komórki reagowały normalnie. Pokażeło to, że SLIT3 nie jest niezbędne do samego spalania paliwa przez komórki tłuszczowe, lecz do budowy nerwowo-naczyniowego „okablowania”, które pozwala mózgowi je kontrolować. Zespół wskazał progenitory adipocytów jako główne lokalne źródło SLIT3 i wykazał, że usunięcie SLIT3 tylko w tych komórkach wystarcza, by stłumić wzrost naczyń, wzrost nerwów i produkcję ciepła podczas ekspozycji na zimno.
Jedno białko, dwa fragmenty, dwie funkcje
SLIT3 nie działa jako pojedynczy, statyczny sygnał. Naukowcy pokazali, że enzym zwany BMP1 przecina SLIT3 na dwa oddzielne fragmenty o odmiennych rolach. Fragment N-terminalny (SLIT3-N) głównie stymuluje wzrost naczyń włosowatych, działając przez receptory na komórkach śródbłonka wyścielających naczynia. Fragment C-terminalny (SLIT3-C) przede wszystkim promuje rozrost nerwów sympatycznych. Zidentyfikowali receptor o nazwie PLXNA1 na włóknach nerwowych jako bezpośrednie miejsce dokowania dla SLIT3-C, co potwierdziły testy wiązania biochemicznego i modele strukturalne oparte na komputerze. Gdy poziom PLXNA1 został zmniejszony, zdolność SLIT3 lub SLIT3-C do wspierania wzrostu nerwów i podnoszenia temperatury brunatnego tłuszczu zniknęła, a ogólna gęstość nerwów i poziomy noradrenaliny w tkance spadły gwałtownie.
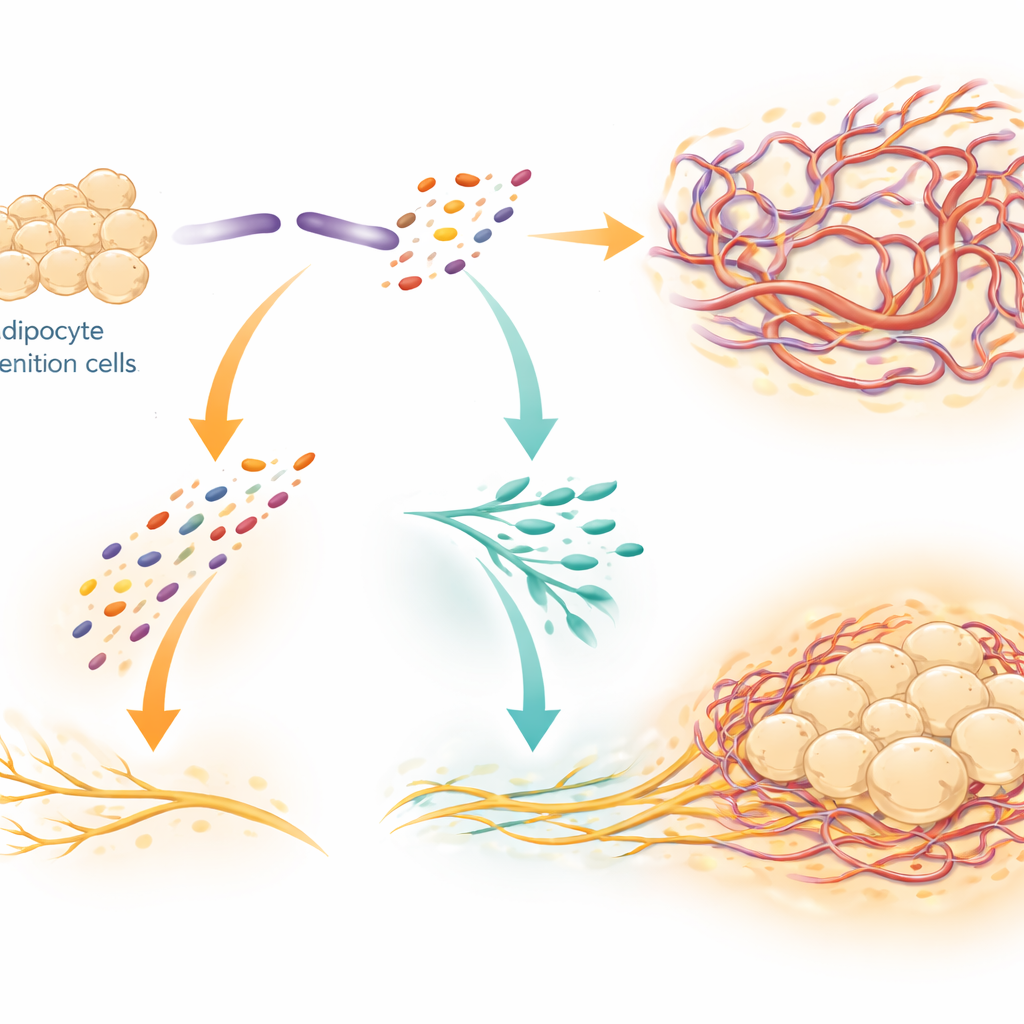
Powiązania z metabolizmem i zdrowiem ludzi
Aby sprawdzić, czy ten mechanizm ma znaczenie u ludzi, autorzy przeanalizowali próbki tkanki tłuszczowej z dużych kohort osób z otyłością. Wyższa ekspresja SLIT3 w tkance tłuszczowej wiązała się z korzystniejszymi profilami: większym poziomem hormonu adiponektyny, mniejszą liczbą zapalnych komórek odpornościowych w tłuszczu trzewnym, lepszą kontrolą poziomu cukru we krwi oraz wyższymi stężeniami korzystnego adipokiny omentyny. Badania genetyczne w innych pracach powiązały także warianty w pobliżu SLIT3 i jego receptora PLXNA1 z otyłością i insulinoopornością. Razem te odkrycia sugerują, że szlak SLIT3 może pomagać w utrzymaniu zdrowej tkanki tłuszczowej i równowagi metabolicznej u ludzi.
Co to oznacza dla utrzymywania ciepła i zdrowia
Podsumowując, badanie ujawnia, że niedojrzałe komórki tłuszczowe w brunatnej tkance robią więcej niż tylko przekształcanie się w dojrzałe adipocyty; aktywnie rzeźbią sieć podtrzymującą tkankę. Uwalniając SLIT3 i pozwalając, by został pocięty na dwa fragmenty, niezależnie lecz synchronicznie napędzają wzrost naczyń krwionośnych i nerwów potrzebnych do efektywnej produkcji ciepła. Ten precyzyjnie wyregulowany, „dwa w jednym” system sygnalizacyjny zapewnia, że brunatna tkanka może szybko się uruchomić, gdy otoczenie wymaga większego ogrzewania. W dłuższej perspektywie zrozumienie i bezpieczne wykorzystanie tej ścieżki może otworzyć nowe możliwości zwiększenia wydatku energetycznego, poprawy zdrowia tkanki tłuszczowej i walki z chorobami metabolicznymi.
Cytowanie: Serdan, T.D.A., Cervantes, H., Frank, B. et al. SLIT3 fragments orchestrate neurovascular expansion and thermogenesis in brown adipose tissue. Nat Commun 17, 2445 (2026). https://doi.org/10.1038/s41467-026-70310-9
Słowa kluczowe: brunatna tkanka tłuszczowa, termogeneza, remodeling nerwowo-naczyniowy, sygnalizacja SLIT3, zdrowie metaboliczne