Clear Sky Science · pl
Aktywacja NF-κB w astrocytach upośledza gojenie się ran po urazie mózgu u samców myszy
Dlaczego stłuczenia mózgu nie zawsze goją się bezproblemowo
Kiedy ktoś otrzymuje uderzenie w głowę, widoczny na zewnątrz uraz to tylko część historii. Głębiej w mózgu zachodzi złożona odpowiedź naprawcza, która może przesądzić, czy osoba wróci do zdrowia, czy też rozwiną się trwałe problemy z myśleniem, nastrojem lub ruchem. Badanie na samcach myszy ujawnia, jak kluczowa ścieżka stresowa w komórkach wspierających, zwanych astrocytami, może przekształcić normalną reakcję gojenia się w proces, który faktycznie pogarsza uszkodzenie po urazie mózgu.
Ukryci pierwsi ratownicy mózgu
Astrocyty to komórki o gwiaździstym kształcie, które otaczają neurony i naczynia krwionośne, pomagając utrzymać wewnętrzne środowisko mózgu w równowadze. Po urazie głowy szybko zmieniają kształt i zachowanie, tworząc barierę wokół uszkodzonego obszaru i pomagając odbudować tkankę. Badacze skupili się na molekularnym wyłączniku w tych komórkach zwanym NF-κB, znanym z kontrolowania zapalenia w wielu tkankach. Zastanawiali się, czy po zamkniętym urazie głowy, podobnym do powszechnych wstrząśnięć mózgu i stłuczeń u ludzi, ten wyłącznik pomaga, czy szkodzi zdolności mózgu do naprawy.
Przełącznik stresu, który zaświeca po uderzeniu
Analizując aktywność genów w tkance mózgowej myszy po urazie, zespół zauważył wzrost ekspresji genów związanych z zapaleniem i sygnalizacją NF-κB, zwłaszcza trzy do siedmiu dni po urazie, gdy wtórne uszkodzenia zaczynają narastać. Używając myszy z reporterami, wykazali, że aktywacja NF-κB nie była rozproszona po całym mózgu, lecz skoncentrowana wokół miejsca uderzenia. Tam była szczególnie aktywna w mikrogleju (strażnikach immunologicznych mózgu) oraz w astrocytach tworzących brzeg rany. To rozmieszczenie i czas sugerowały, że NF-κB w astrocytach może być kluczowym regulatorem organizacji blizny i kontroli odpowiedzi immunologicznej.
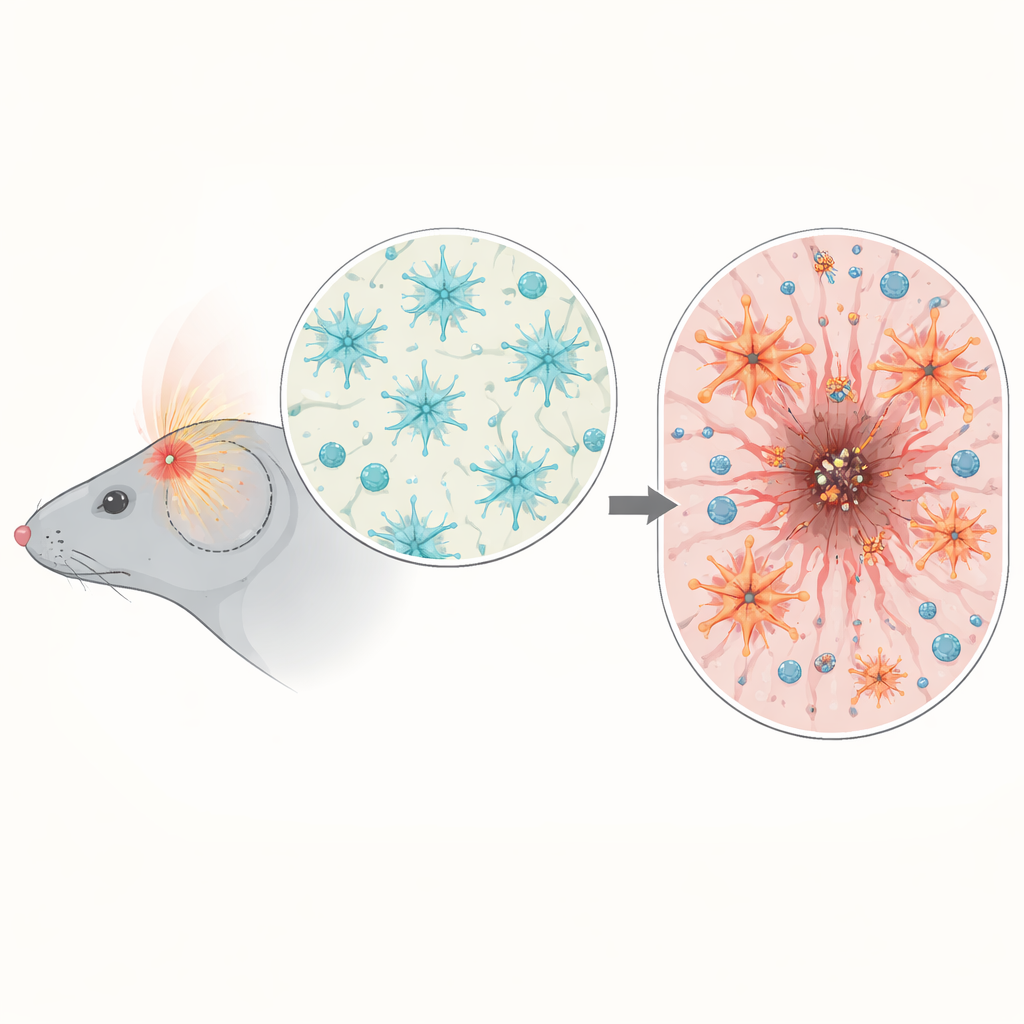
Podkręcenie astrocytów za mocno
Aby sprawdzić związek przyczynowo-skutkowy, naukowcy stworzyli myszy, w których aktywność NF-κB w astrocytach była sztucznie wzmocniona lub osłabiona, ale dopiero po zakończeniu rozwoju mózgu. Po urazie głowy myszy z nadmiernie aktywnym NF-κB w astrocytach traciły więcej masy ciała, wykazywały gorsze wczesne wyniki neurologiczne i miały większe, bardziej trwałe zmiany ogniskowe w tkance na przekrojach i w skanach MRI. Zamiast tworzyć schludną, wyraźną bliznę oddzielającą zniszczone jądro, ich astrocyty wytwarzały grubą, nieuporządkowaną granicę, która nie zmniejszała rany w czasie. Zburzona została normalna równowaga białek macierzy wspierającej wokół uszkodzenia, a kluczowa zewnętrzna struktura barierowa znana jako glial limitans powstawała słabo, co pozostawiało otaczający mózg mniej chroniony.
Kiedy programy gojenia wymykają się spod kontroli
Zagłębiając się w szczegóły molekularne, zespół izolował astrocyty i pobliskie komórki odpornościowe do analizy gen po genie. U zdrowych zwierząt uraz normalnie tłumi niektóre codzienne funkcje konserwacyjne astrocytów, jednocześnie włączając geny wspierające zamykanie ran i regenerację. W przeciwieństwie do tego, astrocyty z przewlekle aktywnym NF-κB już przed urazem wyglądały „uszkodzone”, a po uderzeniu nie były w stanie w pełni wdrożyć korzystnych programów naprawczych, takich jak kontrolowana transformacja pomagająca komórkom zbudować skuteczną granicę. Zamiast tego silnie faworyzowały geny zapalne, przyjmowały cechy toksycznego stanu astrocytów związanego ze starzeniem i chorobami neurodegeneracyjnymi oraz wykazywały oznaki sekretoryjnego profilu przypominającego senescencję, związanego z przewlekłymi, nieustępującymi ranami.
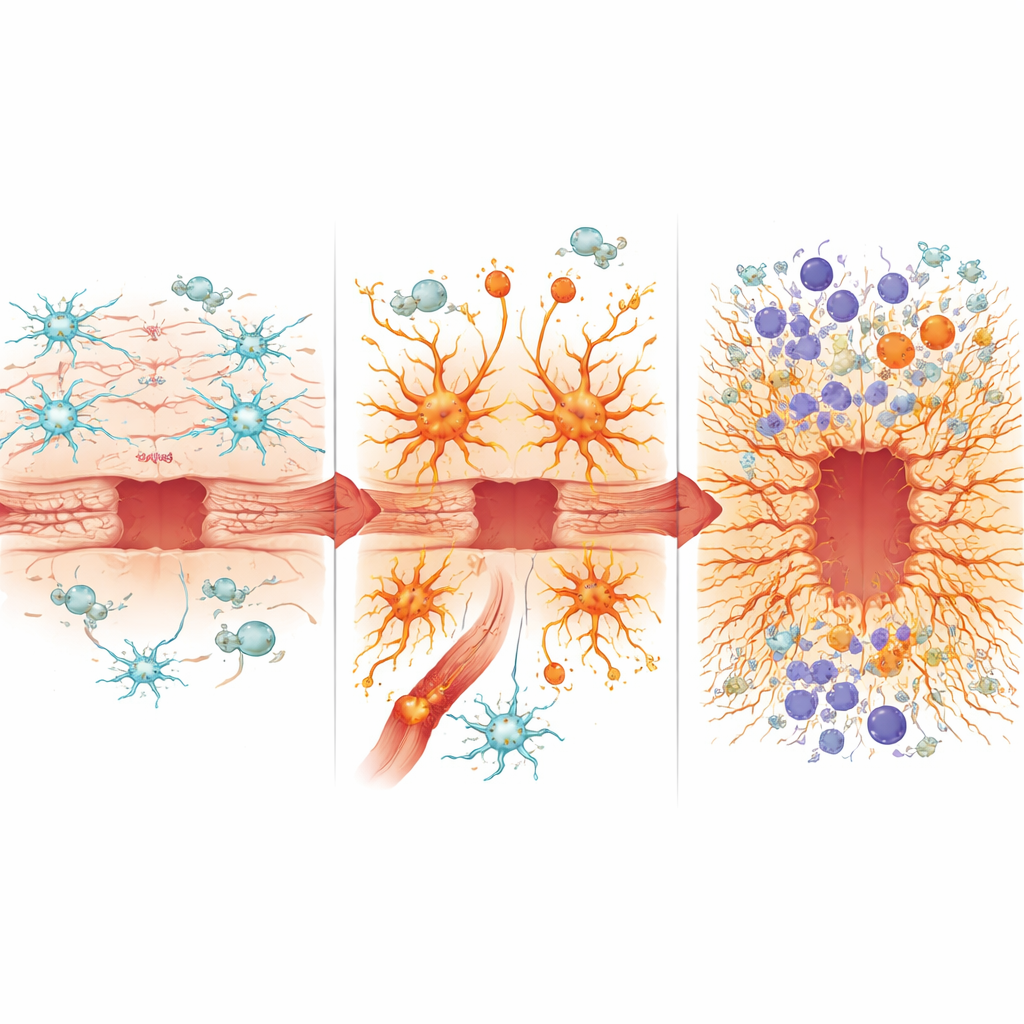
Te błędnie zaprogramowane astrocyty także przekształciły krajobraz immunologiczny mózgu. Bariera krew–mózg stała się bardziej nieszczelna, wpuszczając więcej obwodowych komórek odpornościowych. U myszy z nadaktywnym NF-κB w astrocytach zaobserwowano silniejsze nacieki zapalnych komórek mieloidalnych i zmienione proporcje neutrofili, monocytów i komórek dendrytycznych, a także zwiększenie cytotoksycznych limfocytów T, które mogą dodatkowo uszkadzać tkankę. Komórki odpornościowe w tym środowisku wykazywały silniejsze sygnały napędzane przez interferon i ścieżki inflamasomu, obie powiązane z agresywnym, potencjalnie neurotoksycznym zapaleniem. Jednocześnie stężenia kilku ochronnych lub pro-naprawczych białek, takich jak osteopontyna, były obniżone, podczas gdy inne związane ze stresem oksydacyjnym, przeciążeniem żelazem i bliznowaceniem, w tym oksygenaza hemowa-1 i lipokalina-2, były podwyższone. Stosunek osteopontyny do lipokaliny-2 wyłonił się jako prosty marker korelujący z lepszym lub gorszym gojeniem w różnych szczepach myszy.
Co to oznacza dla rekonwalescencji po urazie głowy
Wspólnie wyniki pokazują, że gdy ścieżka stresowa NF-κB w astrocytach jest przewlekle włączona, te komórki przechodzą od wspierania zorganizowanej naprawy do napędzania chaotycznego bliznowacenia i przedłużonego zapalenia. Zamiast budować czystą granicę, która ogranicza uszkodzenie i umożliwia przebudowę tkanki, przyczyniają się do powstania nieszczelnej, zapalnej niszy, która powiększa zmiany ogniskowe i pogarsza długoterminowy wynik. Chociaż prace przeprowadzono na samcach myszy, wskazują one na NF-κB astrocytów jako obiecujący cel terapii mających na celu poprawę rekonwalescencji po urazie mózgu i sugerują, że poziomy we krwi cząsteczek takich jak osteopontyna i lipokalina-2 mogą w przyszłości pomóc klinicystom monitorować, jak dobrze pacjent się goi.
Cytowanie: Hein, T.M., Nespoli, E., Hakani, M. et al. NF-κB activation in astrocytes impairs wound healing after traumatic brain injury in male mice. Nat Commun 17, 2323 (2026). https://doi.org/10.1038/s41467-026-70304-7
Słowa kluczowe: uraz mózgu, astrocyty, ne zapalenie układu nerwowego, tworzenie blizny mózgowej, NF-kappa B