Clear Sky Science · pl
Model organoidów mózgowych człowieka choroby zapalnej mózgu wywołanej wirusem Zachodniego Nilu wykazuje wrodzoną kompetencję immunologiczną
Dlaczego małe, hodowane w laboratorium mózgi mają znaczenie
Wirus Zachodniego Nilu jest przenoszoną przez komary infekcją, która może dostać się do mózgu i wywołać zapalenie mózgu (encefalitę) — stan zagrażający życiu, który u niektórych pacjentów prowadzi do śmierci, a u wielu ocalałych pozostawia długotrwałe problemy z pamięcią i ruchami. Mimo to lekarze wciąż nie dysponują specyficznym lekiem przeciwwirusowym ani szczepionką dla ludzi. Jednym z głównych powodów jest trudność w badaniu tego, co wirus robi wewnątrz ludzkiego mózgu. W tej pracy naukowcy wykorzystują „organoidy mózgowe” — małe, trójwymiarowe skupiska ludzkich komórek mózgowych hodowane ze komórek macierzystych — aby zbudować realistyczny model laboratoryjny encefalitis wywołanej wirusem Zachodniego Nilu i obserwować, jak komórki mózgowe się bronią.
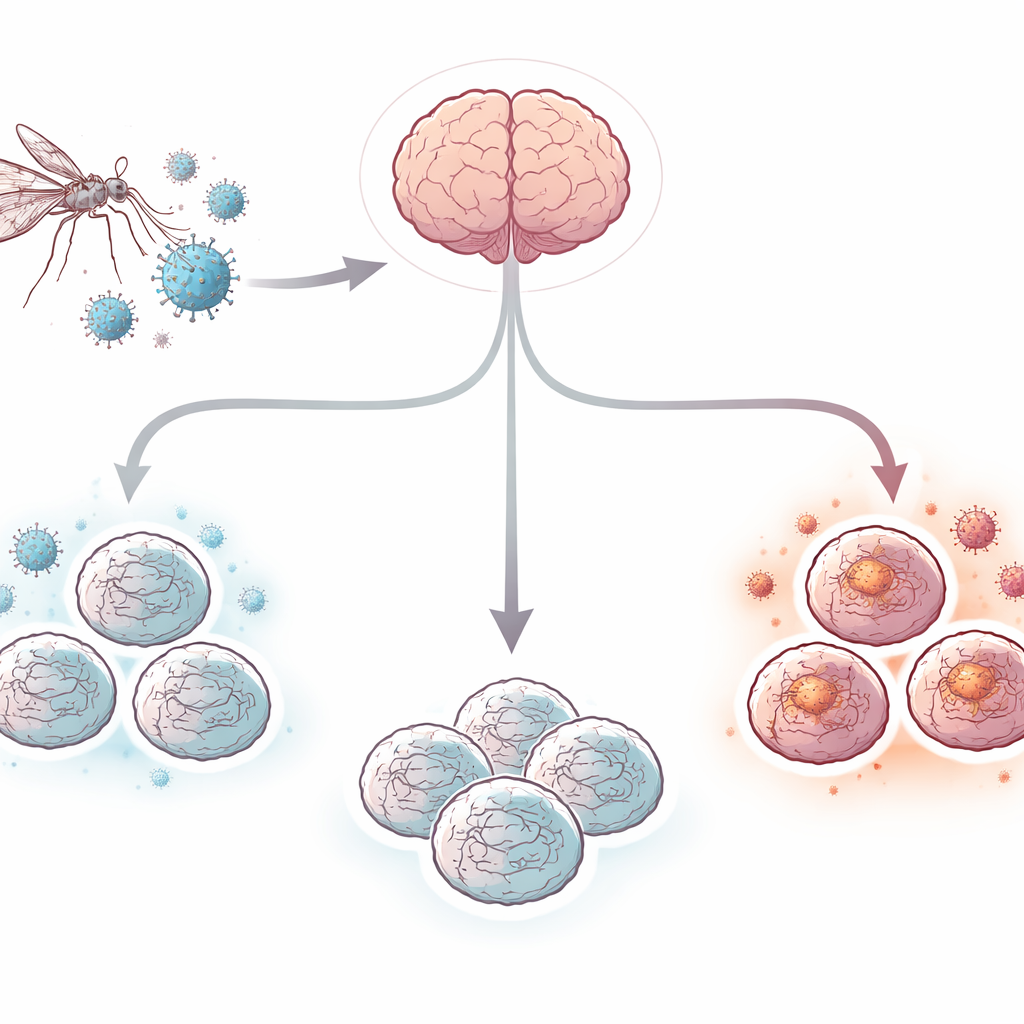
Budowanie miniaturowych ludzkich mózgów na szalce
Zespół rozpoczął od indukowanych pluripotentnych komórek macierzystych pochodzenia ludzkiego, które można nakłonić do różnicowania się w wiele typów komórek. Stosując etapową procedurę, hodowali te komórki przez około 100 dni, tworząc kuleczki wielkości grochu — organoidy mózgowe — które naśladują kluczowe cechy zewnętrznej warstwy ludzkiego mózgu. Te mini‑mózgi zawierały sieci komórek nerwowych (neuronów), komórek wspierających zwanych astrocytami oraz rezydujące komórki odpornościowe zwane mikroglejem. W niektórych organoidach pojawiły się też struktury przypominające splot naczyniówkowy, tkankę produkującą płyn mózgowo‑rdzeniowy i tworzącą istotną barierę między krwią a mózgiem. To zróżnicowanie typów komórek stworzyło bardziej realistyczne środowisko niż tradycyjne, płaskie hodowle komórkowe.
Jak zachowuje się wirus Zachodniego Nilu w mini‑mózgach
Po wystawieniu organoidów na niską dawkę wirusa Zachodniego Nilu infekcja silnie się zawiązała, ale nie jednorodnie. Pomiary wirusa uwalnianego do otaczającego płynu pokazały, że niektóre organoidy szybko osiągnęły szczyt w ciągu pierwszych kilku dni, po czym tendencja była do wygaszania; inne zwiększały poziom wolniej i pozostały zainfekowane przez nawet cztery tygodnie. W kilku organoidach o wczesnym szczycie poziomy wirusa później spadły poniżej progu wykrywalności, co sugeruje, że mini‑mózgi potrafiły same oczyścić infekcję. Co ważne, organoidy nie rozpadały się ani nie wykazywały masywnych widocznych uszkodzeń, co wskazuje, że system może modelować zarówno ostre, jak i długotrwałe zakażenie bez zwykłego „rozpadania się”.
Gdzie wirus atakuje i kto odpowiada
Obrazy mikroskopowe ujawniły, że wirus Zachodniego Nilu nie rozprzestrzeniał się równomiernie przez mini‑mózgi. Zamiast tego białka wirusowe pojawiały się w małych skupiskach blisko zewnętrznych, korze podobnych regionów bogatych w neurony i astrocyty. Materiał wirusowy miał tendencję do gromadzenia się wokół jąder komórkowych, co jest zgodne z aktywną infekcją wewnątrz tych komórek. W przeciwieństwie do tego mikroglej był rozproszony w głębszych warstwach i w dużej mierze nieobecny w obszarach pozytywnych wirusowo, co sugeruje, że nie był głównym wczesnym celem infekcji i nie gromadził się wokół zakażonych miejsc w tym modelu. Ten wzór odzwierciedla obserwacje z sekcji zwłok pacjentów i badań na zwierzętach, gdzie neurony są głównymi celami, a inne komórki mózgowe kształtują otaczające zapalenie.
Chemiczne sygnały zapalenia mózgu
Aby zrozumieć, jak te mini‑mózgi reagują, badacze zmierzyli dziesiątki cząsteczek związanych z odpornością i uszkodzeniem wydzielanych do płynu hodowlanego w czasie. Zaobserwowali skoordynowaną falę sygnałów związanych z zapaleniem mózgu. Na początku ostro wzrastała chemokina CXCL10, po czym pojawiały się inne sygnały przyciągające, takie jak CCL2, CCL17 i CX3CL1, które normalnie rekrutują krążące komórki odpornościowe do mózgu. Klasyczne przekaźniki zapalne — w tym IL‑6, TNF‑α i IL‑18 — również się zwiększyły, podobnie jak markery regulacyjne i związane z uszkodzeniem, takie jak antagonista receptora IL‑1, sTREM‑1, sRAGE oraz czynnik wspierający neurony BDNF. Wiele z tych sygnałów pozostało podwyższonych w późniejszych stadiach infekcji, co sugeruje, w jaki sposób trwałe zapalenie może przyczyniać się do utrzymujących się objawów nawet po opanowaniu wirusa.
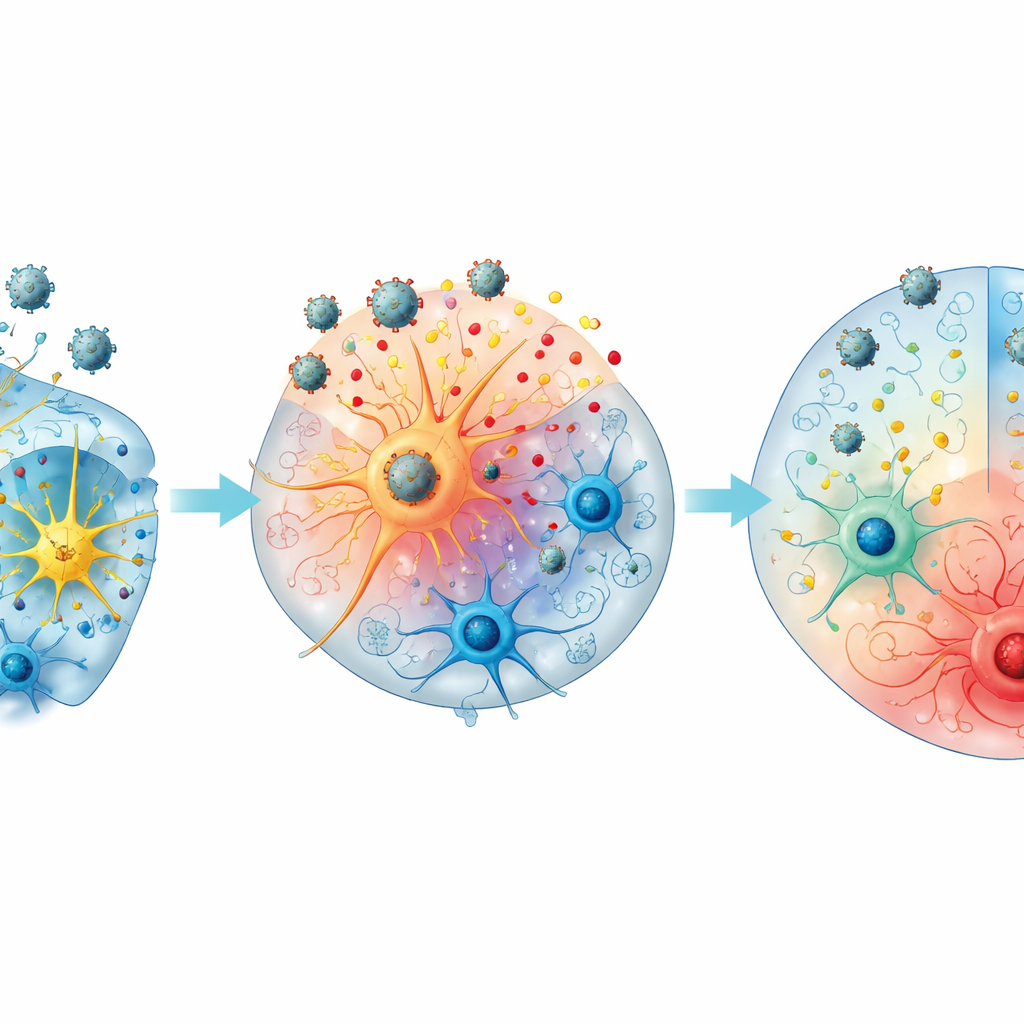
Różne drogi: oczyszczanie lub podtrzymywanie infekcji
Zespół zauważył, że organoidy podążały dwiema głównymi ścieżkami. „Typ A” mini‑mózgi, które osiągały wczesny szczyt wirusowy, częściej później traciły wykrywalny wirus i wykazywały silniejsze skoki niektórych sygnałów zapalnych i regulacyjnych, w tym CXCL10, antagonisty receptora IL‑1 i sTREM‑1. Organoidy „Typu B”, z późniejszymi szczytami, częściej utrzymywały wysokie poziomy wirusa i wykazywały relatywnie wyższe IL‑18 oraz pewne markery uszkodzenia, co sugeruje skłonność do przedłużonego zapalenia. Organoidy, które rozwinęły struktury przypominające splot naczyniówkowy, miały tendencję do wytwarzania jeszcze większych ilości niektórych sygnałów, takich jak IL‑6, CXCL10, CX3CL1 i β‑NGF, co wskazuje na możliwą rolę tej tkanki bariery w kształtowaniu odpowiedzi mózgu na infekcję.
Co to znaczy dla pacjentów
Pokazując, że ludzkie organoidy mózgowe mogą zostać zakażone wirusem Zachodniego Nilu, uruchomić złożone odpowiedzi immunologiczne, a nawet czasami same oczyścić wirusa, to badanie ustanawia potężny nowy odpowiednik ludzkiego mózgu. Dla czytelników niebędących specjalistami kluczowy wniosek jest taki, że naukowcy mogą teraz obserwować, jak tkanka przypominająca ludzki mózg walczy z wirusem przenoszonym przez komary w czasie rzeczywistym, bez eksperymentowania bezpośrednio na pacjentach. Ten model powinien pomóc rozwiązać, dlaczego niektóre infekcje ustępują, podczas gdy inne utrzymują się, jak lokalne komórki mózgowe przyczyniają się zarówno do obrony, jak i uszkodzeń, oraz które szlaki sygnałowe można by ukierunkować, aby zapobiegać długotrwałym problemom neurologicznym. W przyszłości podobne systemy organoidowe mogą zostać wykorzystane do testowania leków przeciwwirusowych, badania szczepionek i analizowania innych wirusów atakujących mózg w kontrolowanych warunkach.
Cytowanie: Steffen, J.F., Widerspick, L., Jansen, S. et al. A human cerebral organoid model of West Nile virus encephalitis shows innate immunocompetency. Nat Commun 17, 2318 (2026). https://doi.org/10.1038/s41467-026-70281-x
Słowa kluczowe: Wirus Zachodniego Nilu, organoidy mózgowe, wirusowe zapalenie mózgu, zapalenie mózgu, wirusy neurotropowe