Clear Sky Science · pl
NAA40 i NAC współpracują przy ko-translacyjnej acetylacji histonów u ludzi
Jak komórki precyzyjnie dostrajają swoje przełączniki genetyczne
W każdej komórce ludzkiej nowo powstające białka są chemicznie modyfikowane w miarę jak wydostają się z maszyn produkujących białka, czyli rybosomów. Te drobne zmiany mogą decydować o miejscu docelowym białka, jego stabilności, a nawet o tym, czy geny zostaną włączone lub wyciszone. W artykule skupiono się na wyspecjalizowanym białku NAA40 oraz pomocniczym kompleksie NAC, ukazując, jak współpracują one na rybosomie, by modyfikować histony — białka, wokół których owinięte jest DNA — i tym samym wpływać na aktywność genów oraz potencjalnie na rozwój nowotworów.
Mała czapeczka, która zmienia zachowanie histonów
Wiele białek ludzkich otrzymuje niewielką chemiczną „czapeczkę” na końcu N, proces znany jako acetylacja końca N. Histony H2A i H4, które pomagają upakować DNA w chromatynę, prawie zawsze są w ten sposób znakowane. NAA40 jest szczególne wśród enzymów, ponieważ wyspecjalizowane jest niemal wyłącznie w dodawaniu tej czapki do tych histonów w trakcie ich syntezy. Ten znak acetylowy konkuruje z innymi modyfikacjami, takimi jak fosforylacja czy metylacja, na tym samym obszarze histonów, więc aktywność NAA40 może przesunąć sposób, w jaki DNA jest upakowane i jak regulowane są geny. Co ważne, zmienione poziomy NAA40 powiązano z kilkoma nowotworami, co czyni je obiecującym celem terapeutycznym.
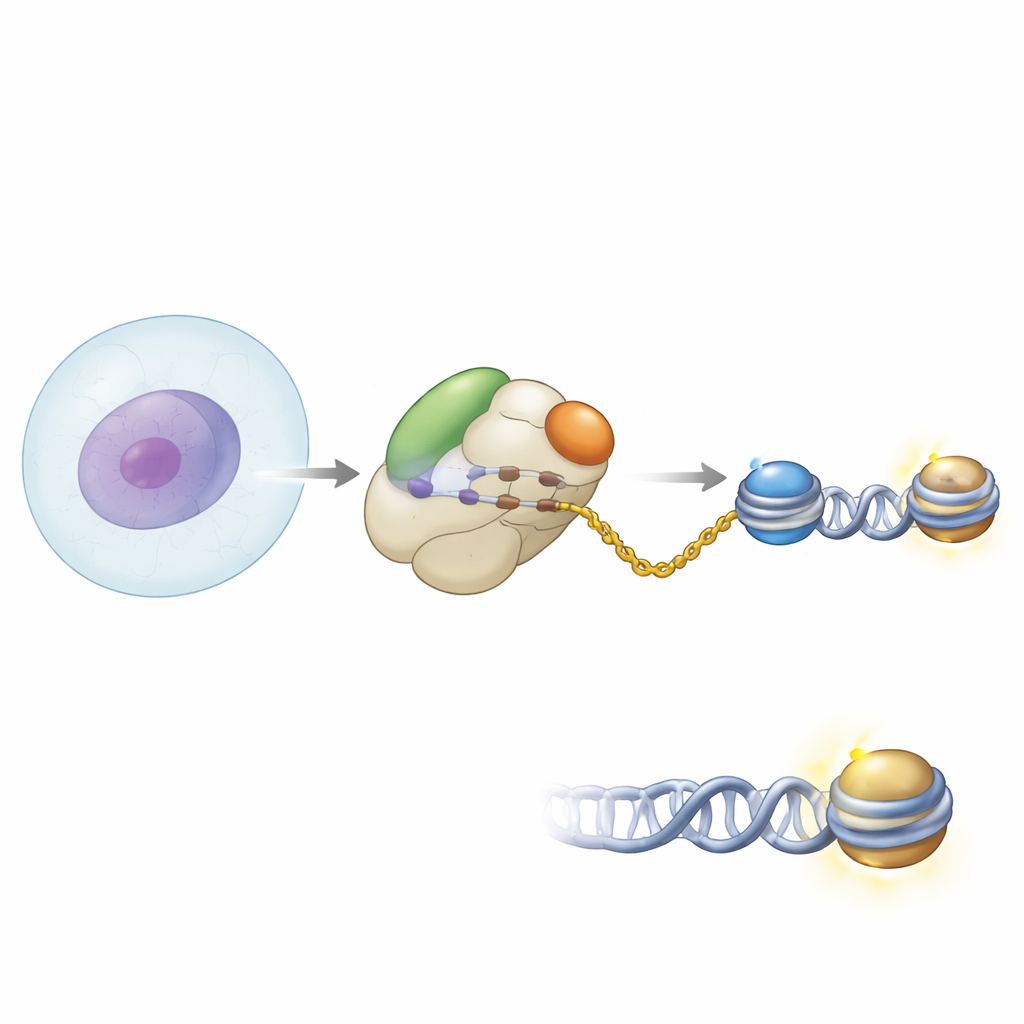
Współpraca przy bramie fabryki białek
Autorzy zastosowali metody biochemiczne oraz wysokorozdzielczą krioelektronową mikroskopię, aby zobaczyć, jak NAA40 jest usytuowane na rybosomie ludzkim. Stwierdzili, że NAA40 znajduje się bezpośrednio przy ujściu tunelu, skąd wydostają się nowo syntetyzowane łańcuchy białkowe. Nie działa tam w pojedynkę: wiąże się obok kompleksu towarzyszącego nowopowstającym polipeptydom (NAC), powszechnego pomocnika przytwierdzonego do rybosomu, który nadzoruje nowe białka w trakcie ich wydostawania się. Migawki strukturalne pokazały, że NAA40 kotwiczy się na rybosomie dzięki unikalnemu dodatnio naładowanemu odcinkowi helikalnemu na swoim początku, podczas gdy NAC jest przytwierdzony za pomocą jednej ze swoich podjednostek do powierzchni rybosomu. Elastyczna domena NAC sięga, aby skontaktować się z NAA40, skutecznie łącząc enzym z rybosomem.
Dlaczego NAC jest potrzebny do regulacji histonów
Aby sprawdzić znaczenie tej współpracy, badacze odtworzyli te interakcje z oczyszczonych składników w probówkach. Zaobserwowali, że NAA40 samodzielnie wiąże rybosomy słabo, ale w obecności NAC wiązanie z rybosomem staje się znacznie silniejsze. Usunięcie specyficznego regionu „UBA” w NAC, który kontaktuje się z NAA40, likwidowało to wzmocnione wiązanie. W komórkach ludzkich obniżenie poziomu NAC prowadziło do zmniejszenia acetylacji histonu H4 zależnej od NAA40 i odpowiadającego wzrostu konkurencyjnego znaku fosforylacji na tym samym ogonie histonowym. Zmiana ta następowała bez zmian w ilości lub lokalizacji samego NAA40, co wskazuje, że główną rolą NAC jest rekrutacja i prawidłowe umiejscowienie NAA40 na rybosomach prowadzących translację, dzięki czemu histony mogą być efektywnie modyfikowane w trakcie ich powstawania.
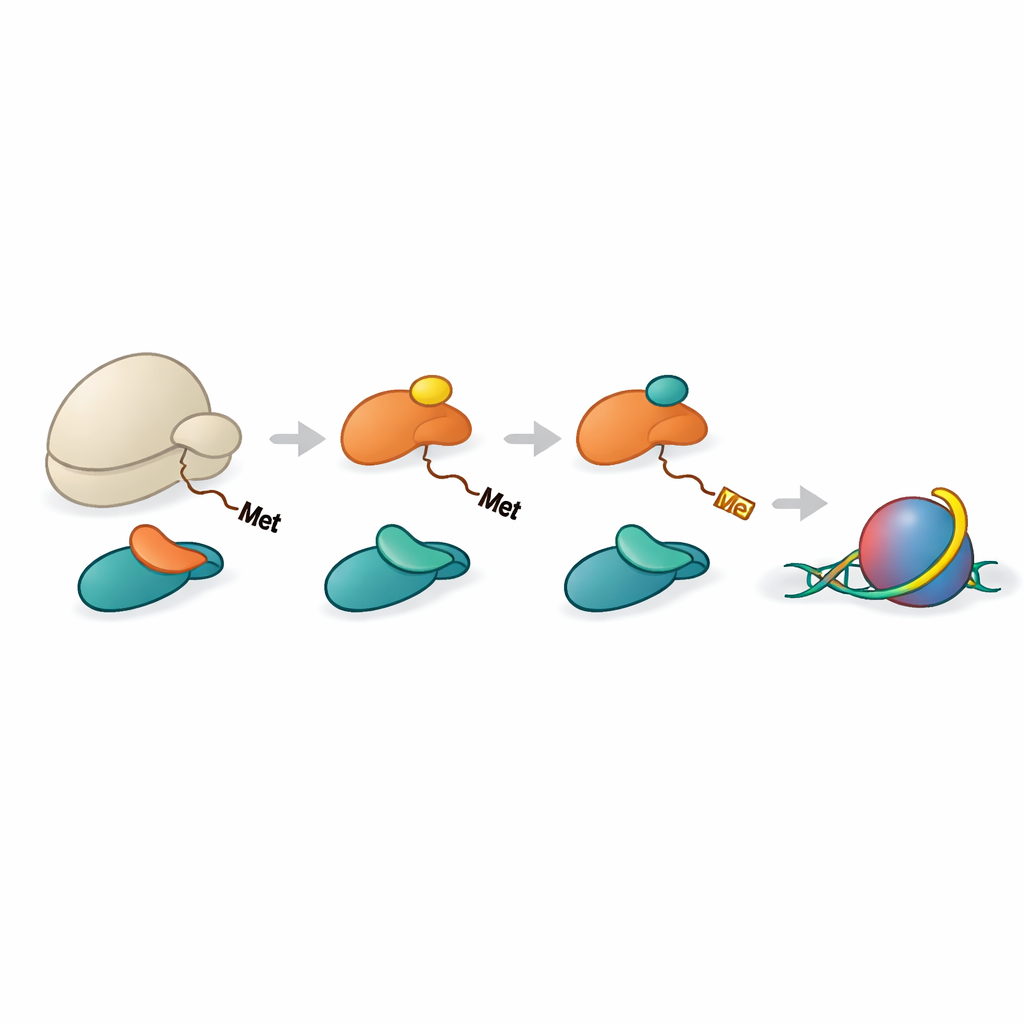
Zsynchronizowana linia montażowa do obróbki histonów
Histony H2A i H4 muszą najpierw stracić początkowy aminokwas metioninę, zanim NAA40 będzie mógł je rozpoznać. Inny enzym, METAP1, dokonuje tego przycinania. Zespół wykazał, że NAC może pomóc sprowadzić METAP1 i NAA40 do rybosomu, tworząc wieloenzymowe zgromadzenie przy ujściu peptydowym. Struktury wysokiej rozdzielczości odtworzonych kompleksów wykazały METAP1 i NAA40 związane obok siebie na rybosomie, z ich miejscami aktywnymi umieszczonymi w niemal równych odległościach od tunelu wyjściowego. Taka geometria oznacza, że gdy ogon histonu wyjdzie na zewnątrz rybosomu na zaledwie kilkanaście aminokwasów, METAP1 może usunąć startową metioninę, a NAA40 natychmiast dodać acetylową czapeczkę, minimalizując opóźnienie między tymi dwoma krokami.
Implikacje dla kontroli genów i raka
Podsumowując, badanie pokazuje, że NAA40 nie krąży swobodnie po komórce w poszukiwaniu histonów do modyfikacji. Zamiast tego jest dokowane do rybosomu przez NAC, tworząc część zorganizowanej stacji przetwarzania, która przygotowuje histony w chwili ich syntezy. Poprzez ścisłe sprzężenie usuwania metioniny i dodawania acetylu, komórka zapewnia, że histony H2A, H4 oraz wariant związany z uszkodzeniem DNA H2A.X szybko otrzymują znak acetylacji, który może kształtować strukturę chromatyny i ekspresję genów. Ponieważ zaburzenia tego wczesnego etapu znakowania histonów mogą sprzyjać rozwojowi nowotworów, poznanie precyzyjnego ułożenia NAA40, NAC i METAP1 na rybosomie dostarcza strukturalnego planu, który może ukierunkować projektowanie leków mających na celu precyzyjne dostrojenie tego krytycznego punktu kontroli epigenetycznej.
Cytowanie: Guan, D., Denk, T., Klavaris, A. et al. NAA40 and NAC cooperate in co-translational histone acetylation in humans. Nat Commun 17, 2486 (2026). https://doi.org/10.1038/s41467-026-70279-5
Słowa kluczowe: acetylacja histonów, NAA40, rybosom, kompleks towarzyszący nowopowstającym polipeptydom, regulacja epigenetyczna