Clear Sky Science · pl
Przejście od acetylacji do fosforylacji zależne od cyklu komórkowego reguluje terminowe dojrzewanie centrosomów
Utrzymywanie naszego ładunku genetycznego na właściwym torze
Za każdym razem, gdy komórka w naszym ciele się dzieli, musi rozdzielić DNA z niezwykłą precyzją. Gdy ten proces się nie powiedzie, komórki mogą zyskać lub stracić chromosomy — stan niebezpieczny, powiązany z rakiem i innymi chorobami. W tym badaniu odkryto molekularny mechanizm czasowy, który pomaga komórkom zbudować maleńkie struktury niezbędne do prawidłowego rozdzielenia chromosomów, ujawniając potencjalne słabe miejsce, które przyszłe terapie przeciwnowotworowe mogłyby wykorzystać.
Mali węzłowi kierowania ruchem komórkowym
W centrum każdej dzielącej się komórki znajdują się centrosomy — niewielkie struktury działające jak węzły ruchu dla włókien, które rozciągają chromosomy. Zanim komórka wejdzie w podział, te węzły muszą „dojrzeć”: wzbogacają się o białka pomocnicze i stają się silnymi organizatorami mikrotubul, dynamicznych włókien tworzących wrzeciono podziałowe. Jeśli to dojrzewanie nastąpi zbyt wcześnie, zbyt późno lub wcale,chromosomy mogą zostać rozdzielone nieprawidłowo, prowadząc do komórek o nieprawidłowej liczbie chromosomów. Zrozumienie, jak komórki włączają centrosomy w odpowiednim momencie, było od dawna istotnym pytaniem w biologii komórki.
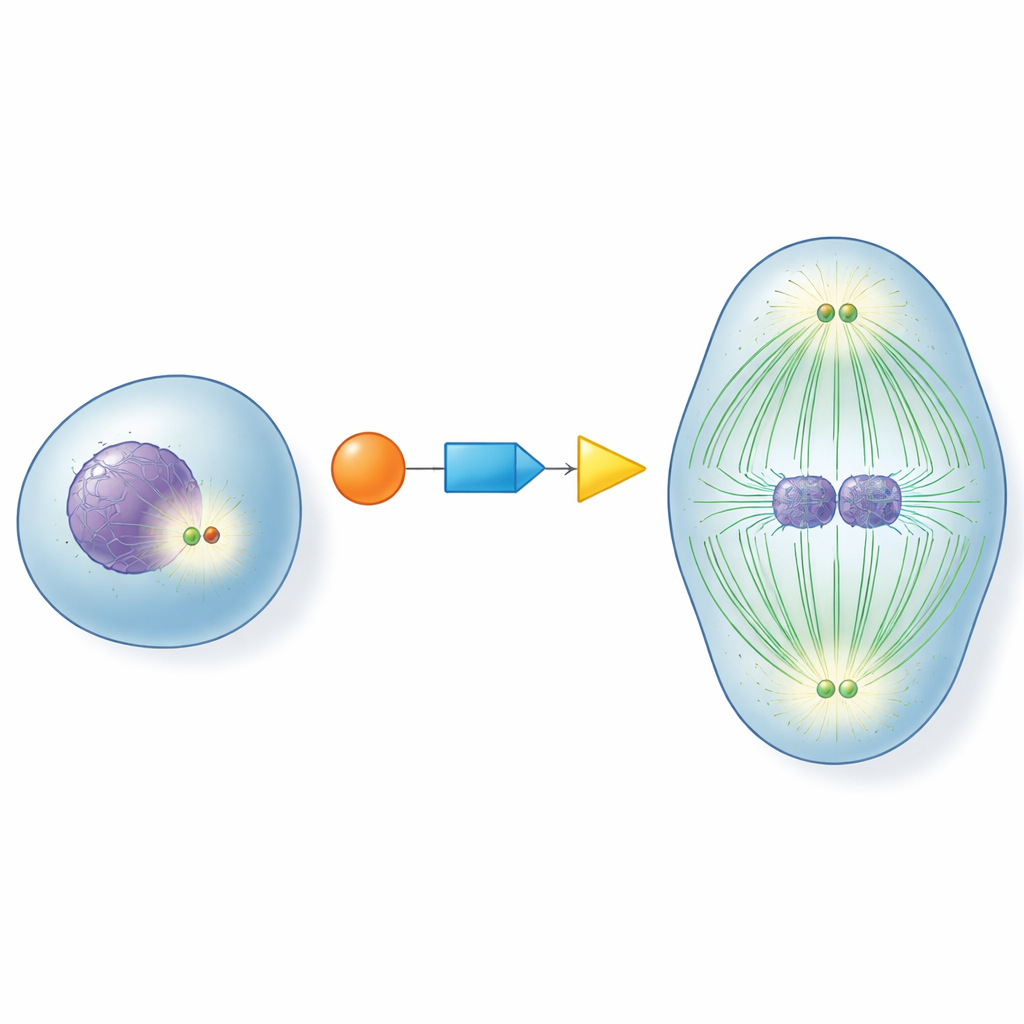
Molekularna sztafeta zapewniająca idealne wyczucie czasu
Autorzy skupili się na trzech kluczowych białkach działających razem jak sztafeta: CDK1, główny regulator cyklu komórkowego; RNF40, wcześniej znane głównie z modyfikowania białek związanych z pakowaniem DNA; oraz PLK1, istotny czynnik napędzający podział komórki. Odkryli, że RNF40 fizycznie obecne jest przy centrosomach przez cały cykl komórkowy i bezpośrednio wiąże PLK1. W miarę przygotowań do podziału CDK1 chemicznie oznacza RNF40 w dwóch konkretnych miejscach, co z kolei zwiększa zdolność RNF40 do przyciągania PLK1. Ten łańcuch CDK1–RNF40–PLK1 zapewnia, że PLK1 trafia do centrosomów dokładnie w późnej fazie przygotowań do podziału, uruchamiając silne dojrzewanie centrosomów, wzrost mikrotubul i zbudowanie prawidłowo uformowanego bipolarnego wrzeciona.
Białkowy przełącznik zmieniający kształt
Co ciekawe, RNF40 nie zawsze przyjmuje te aktywujące znaczniki. W fazach, gdy komórka nie dzieli się lub replikuje DNA, RNF40 nosi inny rodzaj chemicznego ozdobienia — grupy acetylowe — w dwóch sąsiednich pozycjach. Te acetylacje są dodawane przez enzym zwany PCAF i usuwane później przez deacetylazę HDAC1. Acetylowana wersja RNF40 opiera się modyfikacji przez CDK1, skutecznie blokując kolejny etap sztafety. W miarę przechodzenia komórki do końcowej fazy przygotowań HDAC1 stopniowo usuwa znaczniki acetylowe, umożliwiając CDK1 dodanie grup fosforanowych zamiast nich. Starannie wyregulowane przełączenie z acetylacji na fosforylację przekształca RNF40 ze stanu „czuwania” w stan „włączony”, gotowy do rekrutacji PLK1 i uruchomienia centrosomu.
Co się dzieje, gdy zegar zawodzi
Aby sprawdzić, jak istotny jest ten przełącznik, badacze zaprojektowali komórki, w których RNF40 nie mógł być fosforylowany, lub które zmuszono, by pozostawały w stanie naśladującym acetylację. W obu przypadkach PLK1 nie kumulował się prawidłowo przy centrosomach. Komórki te wykazywały osłabiony wzrost mikrotubul z centrosomów, zdeformowane wrzeciona i nieprawidłowo ustawione chromosomy. Wiele z nich kończyło z dodatkowymi lub brakującymi chromosomami — nieprawidłowością znaną jako aneuploidia — a niektóre stały się dwujądrzaste, co świadczy o katastrofalnych błędach podziału. W modelach raka komórki z RNF40 „zablokowanym” w stanie acetylowanym tworzyły mniejsze guzy u myszy i były bardziej wrażliwe na powszechnie stosowane leki chemioterapeutyczne w leczeniu raka jelita grubego, co sugeruje, że zakłócenie tego przełącznika może hamować wzrost nowotworu.
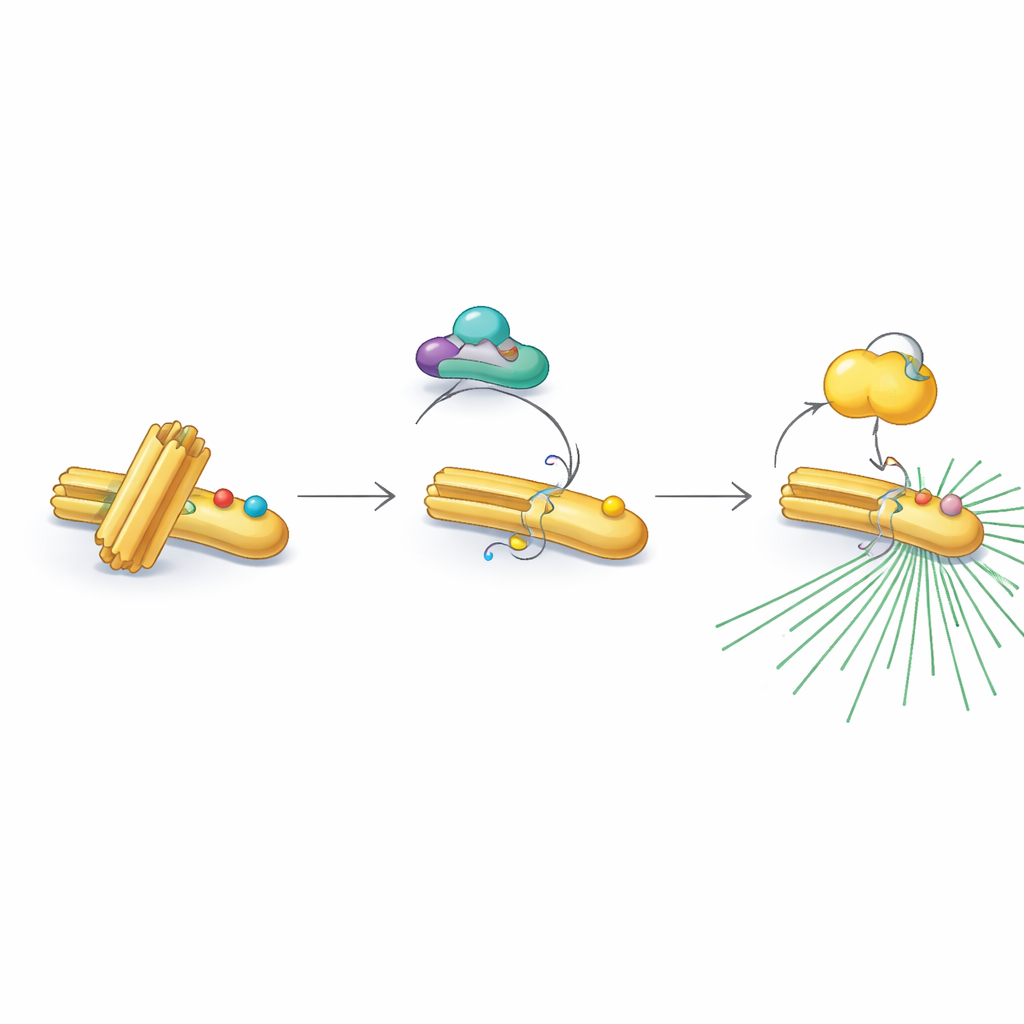
Powiązania z rakiem człowieka i przyszłe możliwości
Zespół przeanalizował także dane pacjentów i próbki nowotworowe. Stwierdzili, że RNF40 często występuje w nadmiarze w raku jelita grubego oraz że niektóre mutacje związane z rakiem w pobliżu miejsc modyfikacji zaburzają jego fosforylację, osłabiając prawidłowe funkcjonowanie centrosomów. Obserwacje te łączą nowo opisany mechanizm czasowy bezpośrednio z chorobą u ludzi. Wskazanie konkretnego białka koordynującego moment dojrzewania centrosomów i rozdział chromosomów podkreśla węzeł sygnałowy, który można by ukierunkować, aby skłonić szybko dzielące się komórki nowotworowe do śmiertelnych błędów podziałowych, pozostawiając w mniejszym stopniu zdrowe komórki.
Nowa dźwignia do wiernego podziału komórek
Dla nie-specjalistów kluczowe przesłanie jest takie, że komórki polegają na precyzyjnie wyregulowanym chemicznym przełączniku na pojedynczym białku, RNF40, aby zdecydować, kiedy dokładnie włączyć mechanizmy rozdzielające chromosomy. Przejście z acetylacji na fosforylację zachowuje się jak światło drogowe na ruchliwym skrzyżowaniu, zapalające się na zielono dopiero wtedy, gdy komórka rzeczywiście jest gotowa do podziału. Gdy światło zawodzi, komórki potykają się podczas podziału, gromadzą błędy genetyczne i mogą przeobrazić się w nowotworowe. Zrozumienie i kontrola tego przełącznika może otworzyć nowe drogi terapii, które selektywnie destabilizują komórki nowotworowe, sabotując ich zdolność do prawidłowego dzielenia się.
Cytowanie: Li, J., Liang, J., Chen, G. et al. A cell cycle-dependent transition of acetylation to phosphorylation regulates timely centrosome maturation. Nat Commun 17, 2583 (2026). https://doi.org/10.1038/s41467-026-70271-z
Słowa kluczowe: dojrzewanie centrosomów, podział komórki, niestabilność chromosomów, sygnalizacja PLK1, rak jelita grubego