Clear Sky Science · pl
Wybór ścieżki między reakcjami click a transferem acylowym napędzanymi przez aminoacylo‑fosfaty
Dlaczego kolejność ma znaczenie w chemii codziennej
W każdej komórce ważne cząsteczki są budowane i modyfikowane w bardzo precyzyjnej kolejności, podobnie jak kroki w przepisie. Ten harmonogram decyduje, czy białko zostanie włączone, wyłączone lub zmieni konformację. Chemicy dążą do naśladowania takiego wewnętrznego harmonogramu za pomocą prostych, nieożywionych cząsteczek w wodzie, bez polegania na enzymach czy zewnętrznych impulsach jak światło czy zmiana pH. W artykule opisano sztuczny układ reakcyjny, który robi dokładnie to: wykorzystuje strukturę małych peptydów i popularną reakcję tworzenia wiązań z „chemii click”, by zdecydować, który krok chemiczny zajdzie jako pierwszy, a który będzie musiał poczekać.
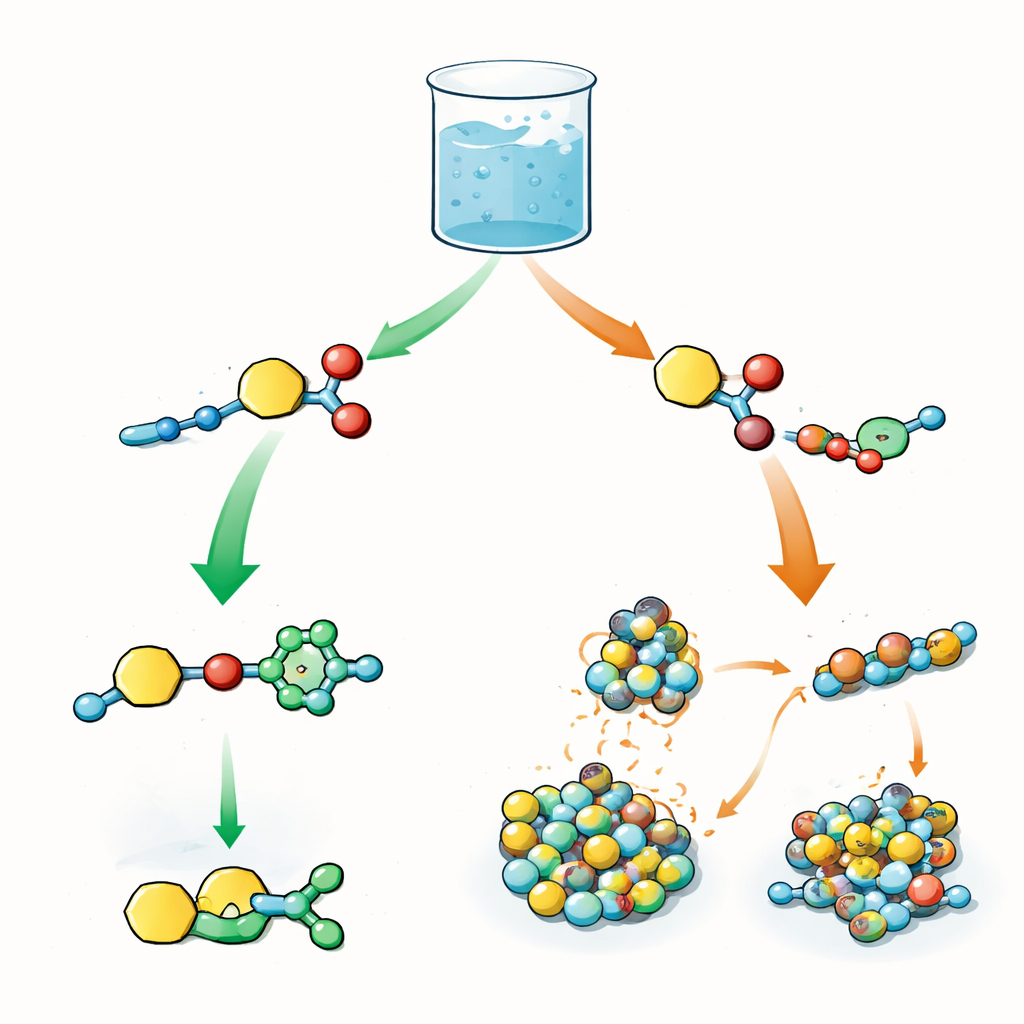
Dwie rywalizujące reakcje w jednym naczyniu
Autorzy zaprojektowali centralny budulec niosący dwie reaktywne cechy: jedną zdolną przekazać grupę acylową (mały fragment chemiczny często używany do modyfikacji białek) oraz drugą, która może przejść reakcję click nazwaną miedziowo‑katalizowaną cykloaddycją azyd–alkinę. W tym samym naczyniu ten budulec miesza się z azydami i krótki peptydami pełniącymi rolę nukleofilów, czyli „chwytającymi” grupę acylową. W biologii kolejność takich kroków — aktywacja, transfer i późniejsze modyfikacje — kontroluje zachowanie białek. Tutaj pytanie jest podobne: gdy obie reakcje są jednocześnie możliwe, czy układ wybiera najpierw reakcję click, transfer acylowy, czy może mieszankę obu?
Wolny tlen, szybki siarka
Zespół najpierw bada peptydy zawierające tyrozynę, aminokwas z bocznym łańcuchem opartym na tlenie. W łagodnie zasadowych warunkach reakcja click przebiega znacznie szybciej: alkin i azyd szybko się łączą, podczas gdy transfer acylu na łańcuch boczny tyrozyny jest powolny i ledwie tworzy wykrywalne pośredniki. Istnieje kilka produktów pochodnych od click i nie ma wyraźnej przerwy czasowej między etapami. Po przełączeniu na cysteinę — aminokwas z bocznym łańcuchem zawierającym siarkę — obraz się odwraca. Cysteina szybko tworzy tioestry — produkty acylowe związane z siarką — które powstają w dużych wydajnościach długo przed pojawieniem się jakichkolwiek produktów click. Dopiero po wielu godzinach zaczynają się pojawiać produkty click. Ta zmiana wynika z tego, że siarka nie tylko reaguje szybciej, ale też wiąże jony miedzi, zajmując katalizator i tymczasowo „wstrzymując” ścieżkę click.
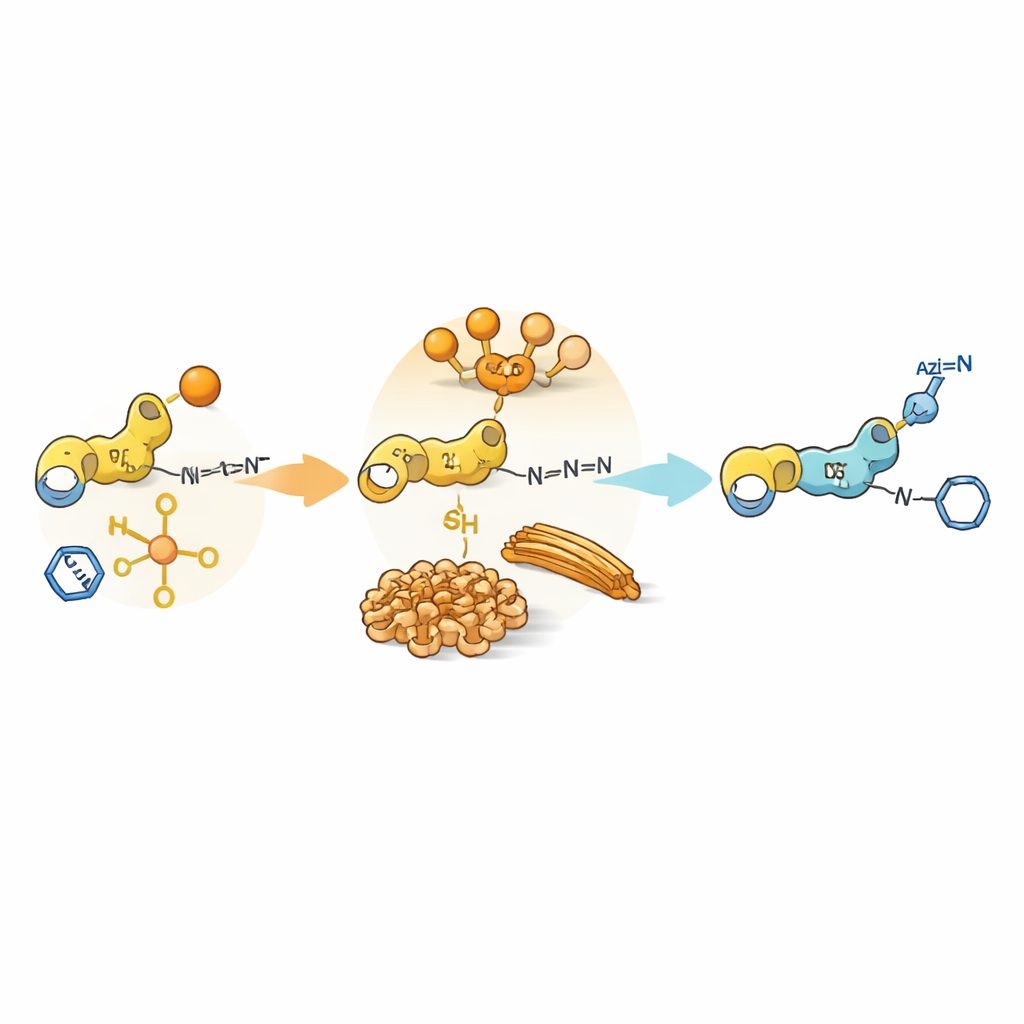
Samoagregacja jako chemiczna bramka
Ponad prostą reaktywność, same peptydy mogą zlepiać się w większe struktury, tworząc w wodzie miękkie żele lub włókna. Te zespoły tworzą małe domeny, w których jedni partnerzy są skoncentrowani, a inni wykluczeni. Dla niektórych dipeptydów zawierających tyrozynę lub cysteinę i dodatkowe grupy aromatyczne, pośredniki samoagregują w fibryle lub gęste cząstki. W tych upakowanych obszarach transfer acylowy jest faworyzowany, ponieważ nukleofil i donor acylu znajdują się blisko siebie, podczas gdy azyd i katalizator miedzi pozostają głównie w otaczającym roztworze. W rezultacie, mimo że reakcja click jest z natury szybka w roztworze wolnym, jest ona spowolniona przez konieczność dotarcia do ukrytych miejsc reaktywnych. To „niezgodność faz” między miejscem obecności katalizatora a lokalizacją substratów wydłuża czas życia acylowanych pośredników i opóźnia rozpoczęcie chemii click.
Programowanie kaskad i wyborów
Aby sprawdzić, jak daleko można posunąć takie wbudowane harmonogramowanie, autorzy zaprojektowali bardziej złożone sytuacje. W jednym przypadku pojedynczy peptyd zawiera zarówno cysteinę, jak i tyrozynę, oferując dwa różne miejsca transferu acylu. Reakcja przebiega jako trzyetapowa kaskada: najpierw tworzy się tioester na cysteinie, potem druga grupa acylowa przemieszcza się na tyrozynę, a dopiero po tych krokach pojawiają się produkty click. W innym zestawie eksperymentów dwa różne azydy — jeden elastyczny i alifatyczny, drugi sztywny i aromatyczny — konkurują o ten sam ośrodek reaktywny. Ku zaskoczeniu, układ konsekwentnie wybiera azyd alifatyczny, co pokazuje, że nawet kształt i charakter elektronowy azydu mogą uprzedzać, które produkty będą dominować, przy jednoczesnej kontroli czasu transferu acylu przez peptyd.
Co to oznacza dla przyszłych inteligentnych materiałów
Mówiąc prosto, praca ta pokazuje, jak można umieścić wiele potencjalnie konkurujących reakcji w tej samej prostej, wodnej mieszaninie i mimo to sprawić, by zachodziły w określonej kolejności — bez enzymów, pomp czy zewnętrznych przełączników. Wybierając, czy peptyd niesie tlen czy siarkę, regulując jego tendencję do samoagregacji i dostosowując naturę partnera azydowego, autorzy kodują rodzaj wewnętrznego zegara w małej sieci chemicznej. Wczesne, odwracalne transfery acylu tworzą krótkotrwałe pośredniki, które determinują, kiedy i jak nastąpi niemal nieodwracalny, trwały krok click. Tak zaprogramowane sekwencje mogą stać się podstawą inteligentnych materiałów i syntetycznych sieci reakcyjnych, które „decydują” o własnych ścieżkach w czasie, podobnie jak precyzyjnie zharmonizowana chemia zachodząca w żywych komórkach.
Cytowanie: Bhattacharjee, D., Sharma, A., Dai, K. et al. Pathway selection between click and acyl transfer reactions driven by aminoacyl phosphates. Nat Commun 17, 2407 (2026). https://doi.org/10.1038/s41467-026-70199-4
Słowa kluczowe: chemia click, transfer acylowy, supramolekularne samoagregowanie, sieci reakcyjne, chemia peptydów