Clear Sky Science · pl
Mapowanie molekularne w DNA-PAINT za pomocą zmodyfikowanego modelowania mieszanin Gaussa
Widzieć niewidzialny świat molekuł
Współczesna biologia coraz częściej polega na mikroskopach, które widzą nie tylko komórki, lecz także poszczególne molekuły w ich wnętrzu. Jednak przekształcenie słabego, migoczącego światła emitowanego przez te molekuły w wiarygodną „mapę” położenia każdej z nich jest zaskakująco trudne. W tym badaniu przedstawiono nową metodę obliczeniową, nazwaną G5M, która sprawia, że te mapy molekularne są znacznie dokładniejsze i bardziej szczegółowe, pomagając naukowcom zrozumieć, jak białka są rozmieszczone i zgrupowane w rzeczywistych komórkach, z rozdzielczością sięgającą kilku nanometrów.
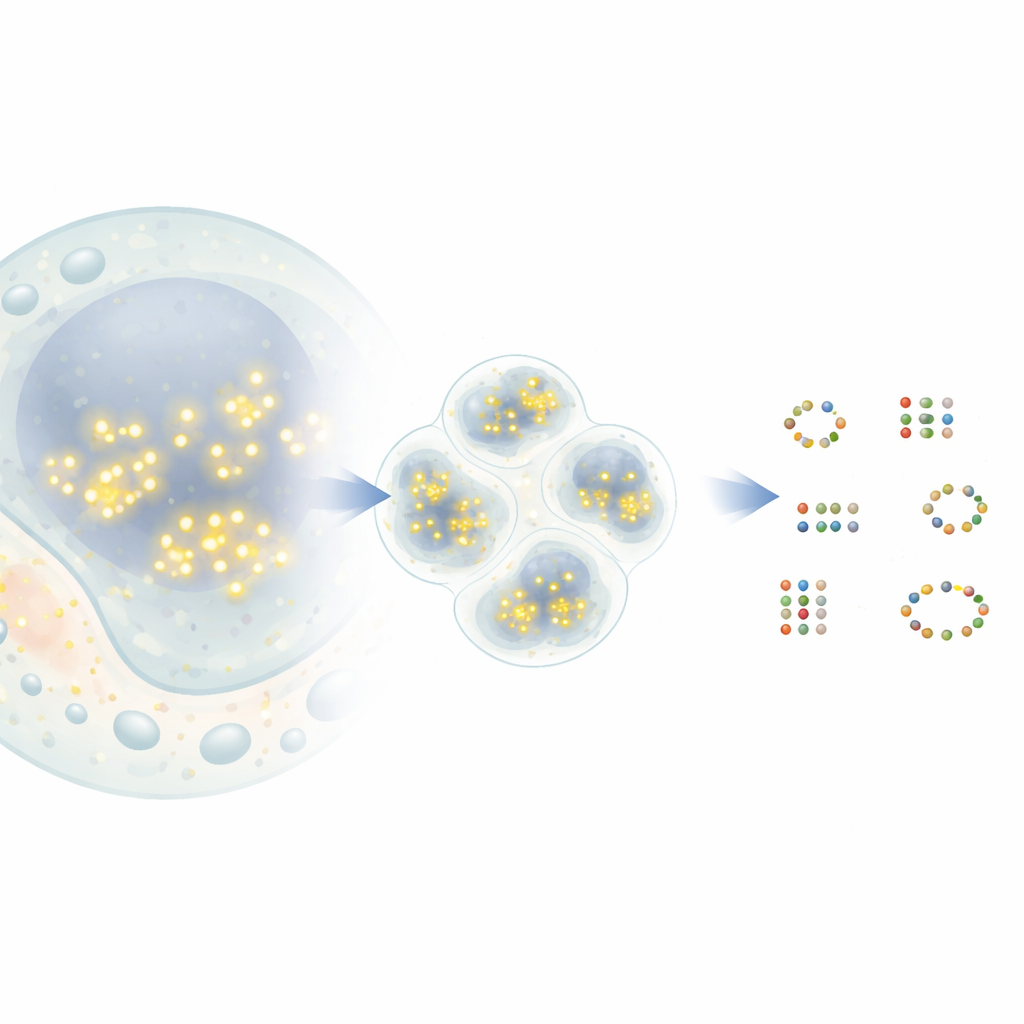
Z migoczących kropek do map molekularnych
W popularnej technice superrozdzielczej zwanej DNA-PAINT krótkie odcinki DNA sprzężone z barwnikami fluorescencyjnymi krótkotrwale wiążą się i odłączają od dopasowanych znaczników DNA przytwierdzonych do białek docelowych. Za każdym razem, gdy barwnik się wiąże, pojawia się jako jasna kropka w mikroskopie, po czym znika. Z czasem wiele takich zdarzeń tworzy chmurę kropek wokół każdego białka. W teorii środek każdej chmury wskazuje prawdziwe położenie białka z precyzją rzędu nanometrów. W praktyce jednak kropki pochodzące od pobliskich białek mogą się nakładać, a część sygnałów to losowe tło. Istniejące narzędzia analityczne często łączą bliskich sąsiadów w jedno białko albo przeciwnie — generują białka, których nie ma, co ogranicza biologiczny wgląd, jaki można uzyskać.
Inteligentniejszy sposób na znalezienie prawdziwych molekuł
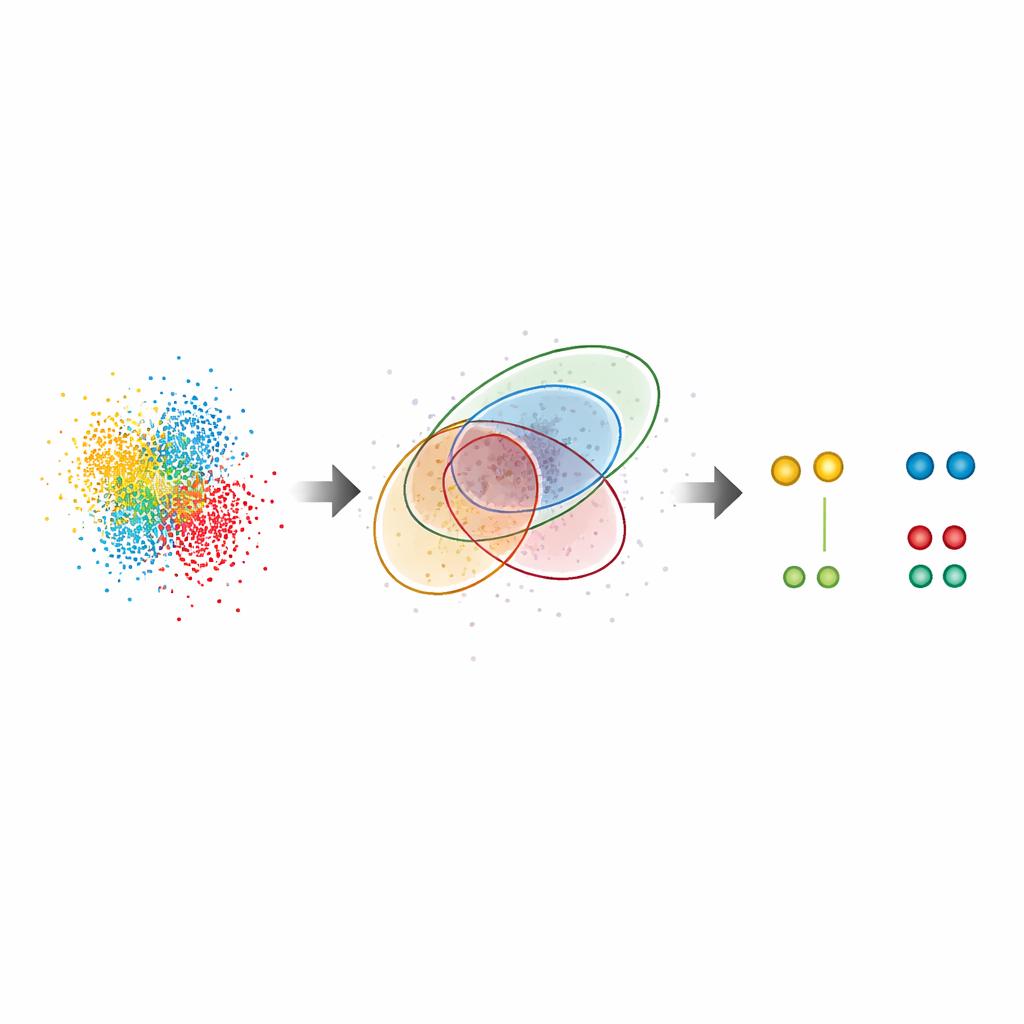
Nowa metoda G5M traktuje rozproszenie kropek jako mieszaninę prostych, dzwonkowatych chmur, z których każda odpowiada jednej rzeczywistej molekule. Zamiast jedynie grupować pobliskie kropki według gęstości, G5M używa modelu probabilistycznego, który uwzględnia to, co już wiadomo o eksperymencie: jak precyzyjnie można mierzyć pozycje, jak szybko odcinki DNA się wiążą i odłączają oraz jak mikroskop rozmywa światło w dwóch lub trzech wymiarach. Następnie testuje różne możliwe wyjaśnienia — różne liczby i kształty chmur — i automatycznie wybiera to, które najlepiej równoważy dopasowanie i prostotę. Dodatkowe zabezpieczenia odrzucają podejrzane rozwiązania, takie jak chmury zbyt wąskie, zbyt szerokie, oparte na zbyt niewielu kropkach lub niezdecydowanie odseparowane od siebie.
Udowodnienie skuteczności w symulacjach i strukturach DNA
Aby przetestować G5M, autorzy najpierw użyli realistycznych symulacji komputerowych prostych scen: par molekuł oraz małych siatek dwunastu molekuł rozmieszczonych zaledwie kilka nanometrów od siebie. W porównaniu z wiodącą obecnie metodą, znaną jako Gradient Ascent, G5M wykrył znacznie więcej molekuł, które powinny być widoczne przy teoretycznym limicie rozdzielczości, przy niemal zerowej liczbie zgłaszanych molekuł nieistniejących. W kluczowych przypadkach odzyskał blisko położone pary 27 razy częściej niż starsza metoda i poprawił efektywną rozdzielczość o ponad połowę. Zespół potwierdził te korzyści eksperymentalnie, używając struktur origami DNA — sztucznych kształtów DNA z miejscami dokującymi umieszczonymi w precyzyjnie znanych pozycjach — wykazując, że G5M potrafi niezawodnie policzyć i zlokalizować niemal wszystkie oczekiwane miejsca w różnych warunkach obrazowania.
Odkrywanie ukrytych wzorców w prawdziwych komórkach
Ponadto G5M zastosowano w złożonych systemach biologicznych. W kompleksach porów jądrowych, wielkich bramkach w jądrze komórkowym, metoda odtworzyła znane pierścieniowe uporządkowanie kluczowego białka Nup96, nawet tam, gdzie partnerzy byli rozdzieleni zaledwie około dziesięciu nanometrów. Znaleziono prawie dwa razy więcej par białek niż w standardowej metodzie i odtworzono niezależne szacunki wydajności znakowania, co sugeruje, że metoda ani nie pomija wielu molekuł, ani nie dodaje fałszywych. Autorzy przebadali także CD20, receptor powierzchniowy zaangażowany w nowotwory krwi i będący celem terapeutycznych przeciwciał. W tym przypadku G5M ujawnił znacząco więcej małych skupień (dimerów, trimerów i tetramerów) CD20 na błonie komórkowej, wyjaśniając, jak przeciwciało przeciwnowotworowe i powiązane formaty leków reorganizują te receptory. Metoda poprawiła nawet wydajność podejścia o ultra-wysokiej rozdzielczości nazwanego RESI, które polega na rozdzielaniu sygnałów w wielu rundach obrazowania.
Co to oznacza dla przyszłej mikroskopii
Wyciągając bardziej wiarygodne informacje z istniejących danych DNA-PAINT, G5M pokazuje, że lepsze oprogramowanie samo w sobie może odblokować nowe szczegóły biologiczne, bez konieczności zmiany mikroskopów czy barwników. Algorytm utrzymuje bardzo niską liczbę fałszywych wykryć, jednocześnie rozróżniając molekuły niemal stykające się ze sobą — co jest kluczowe przy pytaniach o to, ile białek znajduje się w kompleksie, jak są rozmieszczone lub jak lek zmienia ich ułożenie. Zintegrowany z otwartoźródłową platformą Picasso i odporny na typowe ustawienia, G5M ma szansę stać się standardowym narzędziem do przekształcania migoczącej fluorescencji w wiarygodne mapy molekularne, pomagając badaczom odtwarzać nanoskalową organizację życia wewnątrz komórek.
Cytowanie: Kowalewski, R., Reinhardt, S.C.M., Pachmayr, I. et al. Molecular mapping in DNA-PAINT via modified Gaussian Mixture Modeling. Nat Commun 17, 2315 (2026). https://doi.org/10.1038/s41467-026-70198-5
Słowa kluczowe: mikroskopia superrozdzielcza, DNA-PAINT, mapowanie molekularne, oligomeryzacja białek, algorytmy analizy obrazów