Clear Sky Science · pl
Pojedynczo‑komórkowa multiomika ujawnia mechanoczułą oś PIEZO1–IL‑33 w komórkach śródbłonka napędzającą włóknienie płuc
Dlaczego sztywność płuc ma znaczenie
Włóknienie płuc to niszczycielska choroba, w której niegdyś elastyczne pęcherzyki płucne stopniowo zamieniają się w sztywne blizny, przez co każdy oddech staje się ciężką pracą. Obecnie lekarze potrafią jedynie spowolnić postęp choroby, nie zatrzymać jej ani odwrócić. To badanie stawia pozornie proste, ale doniosłe pytanie: jak komórki wyściełające naczynia krwionośne w płucach wyczuwają, że otaczająca je tkanka stała się nienaturalnie sztywna, i jak to odczucie przekształca się w dalsze bliznowacenie? Śledząc ten łańcuch wydarzeń aż do pojedynczych komórek i pojedynczych genów, autorzy odkrywają mechaniczny „włącznik” w naczyniach, który może być podatny na działanie leków.
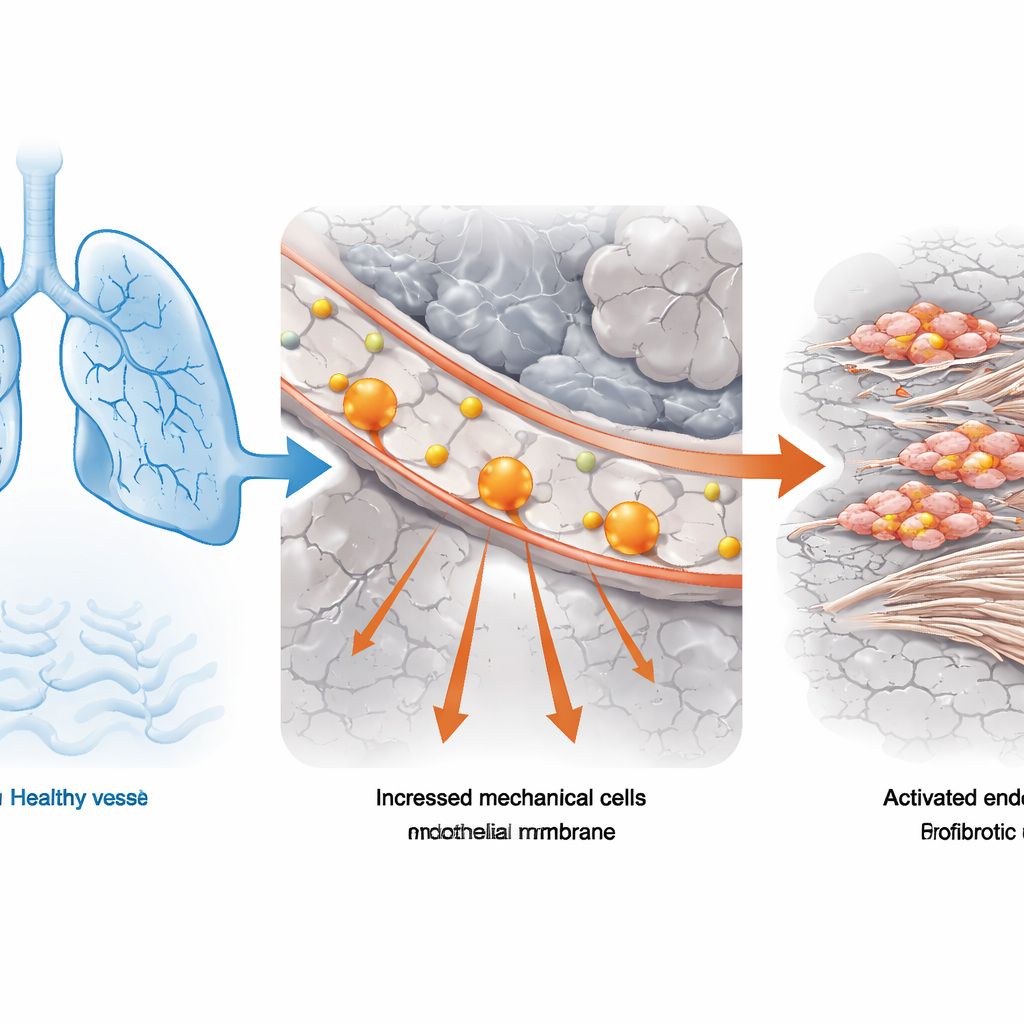
Od badań czynnościowych płuc do pojedynczych komórek
Zespół rozpoczął od tkanki płucnej od osób z idiopatycznym włóknieniem płuc — najczęstszą postacią choroby — oraz od dawców z prawidłowymi płucami. Połączyli standardowe pomiary czynności płuc (ile powietrza osoba potrafi wydmuchać z siłą) z potężną techniką sekwencjonowania RNA pojedynczych komórek, która odczytuje, które geny są aktywne w tysiącach pojedynczych komórek. Korzystając z narzędzia obliczeniowego łączącego dane kliniczne z profili typu bulk z danymi pojedynczo‑komórkowymi, zidentyfikowali typy komórek najsilniej powiązane z poważnie upośledzoną czynnością płuc. Komórki śródbłonka naczyniowego — tworzące wewnętrzną warstwę naczyń krwionośnych — wyróżniały się szczególnym wzbogaceniem u pacjentów, których pojemność płuc była mniejsza niż połowa wartości prawidłowej. W tych komórkach śródbłonka programy genowe związane z „napięciem mechanicznym” były konsekwentnie nasilone, co sugeruje, że nienormalne siły fizyczne są częścią problemu.
Napięcie mechaniczne jako ukryty czynnik napędowy
Aby sprawdzić, czy połączenie między wykrywaniem naprężenia a chorobą jest ogólne, badacze posłużyli się dwoma modelami mysimi bliznowacenia płuc: jednym wywołanym lekiem chemioterapeutycznym bleomycyną, a drugim przez długotrwałe narażenie na pył krzemionkowy, będący zagrożeniem zawodowym. Stosując metody pojedynczo‑komórkowe w tych modelach, ponownie stwierdzili, że komórki śródbłonka nosiły wyraźne sygnatury zwiększonego napięcia mechanicznego. W obu modelach, gdy otaczająca tkanka płuc pogrubiała się i sztywniała, wyściółka naczyń wyglądała, jakby przełączała się w adaptacyjnie nieskuteczny stan. Ta zbieżność między próbkami ludzkimi a modelami zwierzęcymi wzmocniła ideę, że zniekształcone siły fizyczne w płucu, a nie tylko zapalenie czy aktywność układu odpornościowego, są kluczowe dla rozwoju i progresji włóknienia.
Czujnik ciśnienia o kluczowej roli
Zagłębiając się dalej, zespół poszukiwał konkretnych „mechanoczułych” czujników — białek przekształcających rozciąganie fizyczne w sygnały biochemiczne — które byłyby nadekspresjonowane w zestresowanych komórkach śródbłonka. Jeden kanał białkowy, nazywany PIEZO1, wielokrotnie wyłaniał się jako główny podejrzany. Zarówno u myszy, jak i u ludzi z włóknieniem poziomy PIEZO1 były wyraźnie wyższe w komórkach śródbłonka naczyń niż u zdrowych kontroli. Gdy badacze stworzyli myszy, u których PIEZO1 został usunięty jedynie w śródbłonku, zwierzęta te okazały się znacznie bardziej odporne na bliznowacenie płuc wywołane bleomycyną: miały mniej nagromadzenia kolagenu, mniej aktywowanych komórek tworzących blizny oraz niższe poziomy chemicznego markera włóknienia. Farmakologiczne blokowanie PIEZO1 za pomocą peptydowego inhibitora też łagodziło bliznowacenie, podczas gdy jego aktywacja pogarszała włóknienie — o ile receptor nie był usunięty z komórek śródbłonka. Razem te eksperymenty wykazały, że PIEZO1 w komórkach wyściełających naczynia nie jest jedynie obserwatorem, lecz koniecznym czynnikiem napędzającym chorobę.
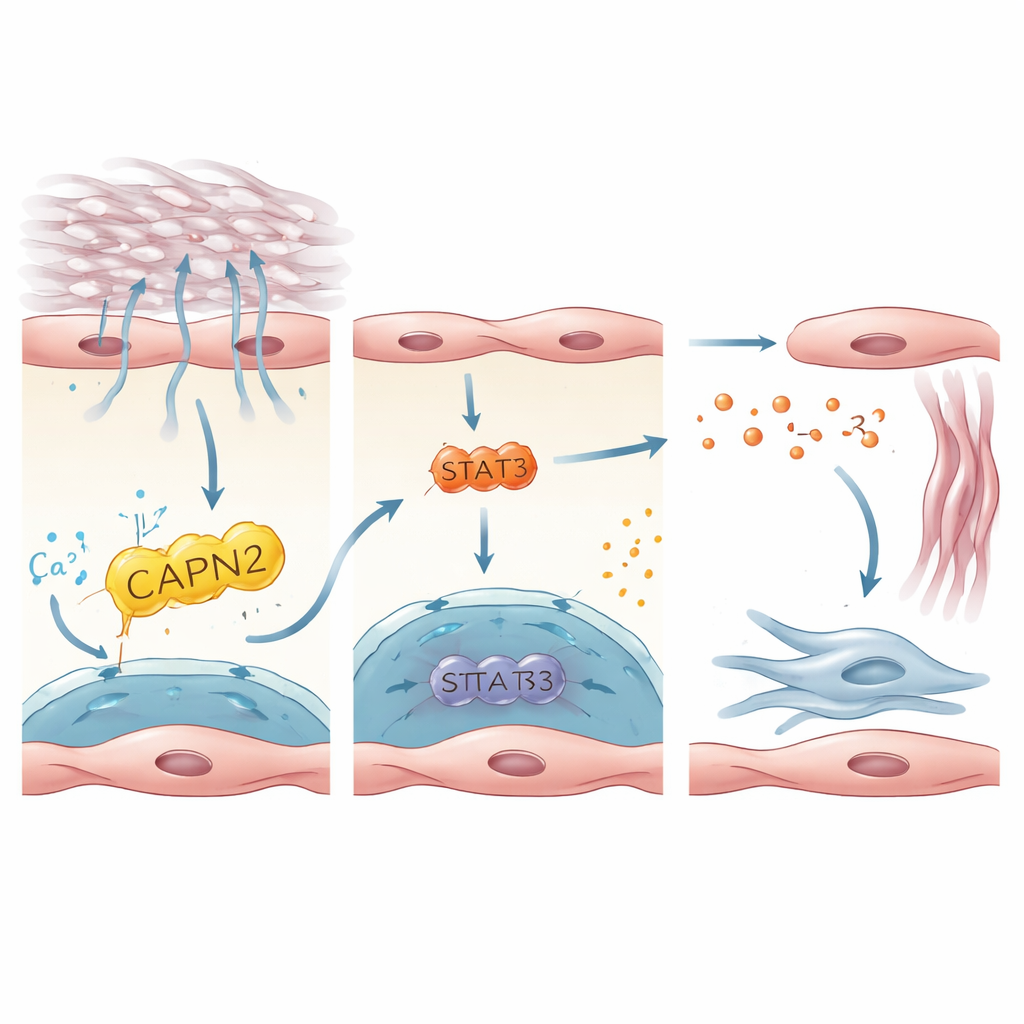
Łańcuch sygnałowy, który budzi komórki tworzące blizny
Badanie następnie odtworzyło, jak aktywacja PIEZO1 w komórkach śródbłonka przekłada się na sygnały pobudzające fibroblasty — komórki odkładające tkankę bliznowatą. Integrując dane z ludzi i myszy, autorzy skoncentrowali się na interleukinie‑33 (IL‑33), małym białku uwalnianym przez zestresowane lub uszkodzone komórki, jako kluczowym posłańcu. IL‑33 była silnie eksprymowana w komórkach śródbłonka pozytywnych pod kątem PIEZO1 i podwyższona w płucach pacjentów i myszy z włóknieniem. W hodowanych ludzkich komórkach śródbłonka umieszczonych na sztywnych podłożach lub rozciąganych, by naśladować oddychanie przeciw opornemu płucom, aktywacja PIEZO1 zwiększała produkcję IL‑33. Zależność ta wymagała udziału enzymu CAPN2 i czynnika transkrypcyjnego STAT3, które wspólnie regulowały aktywność genu IL‑33. U myszy usunięcie IL‑33 specyficznie w śródbłonku chroniło przed włóknieniem, natomiast wymuszone nadmierne wytwarzanie IL‑33 przez komórki śródbłonka znosiło ochronny efekt braku PIEZO1. Wyniki te opisują liniową oś: napięcie mechaniczne → PIEZO1 → CAPN2/STAT3 → IL‑33 → aktywacja fibroblastów i bliznowacenie.
Co to oznacza dla przyszłych terapii
Dla osób niezajmujących się specjalistycznie tematem przekaz jest taki, że włóknienie płuc nie jest wywoływane jedynie przez zbuntowane komórki odpornościowe; to także choroba wadliwego „dotyku” w naczyniach krwionośnych. Komórki śródbłonka odczuwają, że ich otoczenie stało się zbyt sztywne, włączają przełącznik PIEZO1 i w odpowiedzi uwalniają IL‑33 — sygnał zagrożenia, który pobudza pobliskie fibroblasty do dalszego odkładania blizny. Rozbijając ten łańcuch od siły mechanicznej do ekspresji genów, praca wskazuje kilka obiecujących celów — sam PIEZO1, przekaźnik CAPN2‑STAT3 oraz IL‑33 — dla terapii mających przerwać samozaostrzające się cykle sztywności i bliznowacenia. Choć potrzebne są dalsze badania, by bezpiecznie modulować te ścieżki u ludzi, ta mechanoczuła oś śródbłonkowa oferuje nowe, fizycznie ugruntowane podejście do zwalczania choroby, która długo opierała się skutecznemu leczeniu.
Cytowanie: Zhang, L., Gui, X., Hou, R. et al. Single-cell multiomics uncovers an endothelial mechanosensitive PIEZO1-IL-33 axis driving pulmonary fibrosis. Nat Commun 17, 2655 (2026). https://doi.org/10.1038/s41467-026-70193-w
Słowa kluczowe: włóknienie płuc, komórki śródbłonka, mechanotransdukcja, PIEZO1, IL‑33