Clear Sky Science · pl
Dostosowania tubuliny Plasmodium warunkują odmienne architektury mikrotubul, ich mechanikę i podatność na leki
Dlaczego szkielet malarii ma znaczenie
Pasożyty malarii przeżywają wewnątrz ludzkich krwinek, a jednocześnie muszą przecisnąć się przez komórki muchówek i różne tkanki. W tym celu polegają na wewnętrznym rusztowaniu złożonym z mikroskopijnych rurek zwanych mikrotubulami. W badaniu zadano proste, lecz istotne pytanie: jak mikrotubule pasożyta mogą być tak wyspecjalizowane i wytrzymałe, skoro ich podstawowe cegiełki wyglądają bardzo podobnie do tych w naszych komórkach? Odpowiedź ujawnia nie tylko to, jak pasożyt zachowuje kształt, ale też jak możemy projektować leki atakujące jego „szkielet” bez szkody dla naszego własnego.
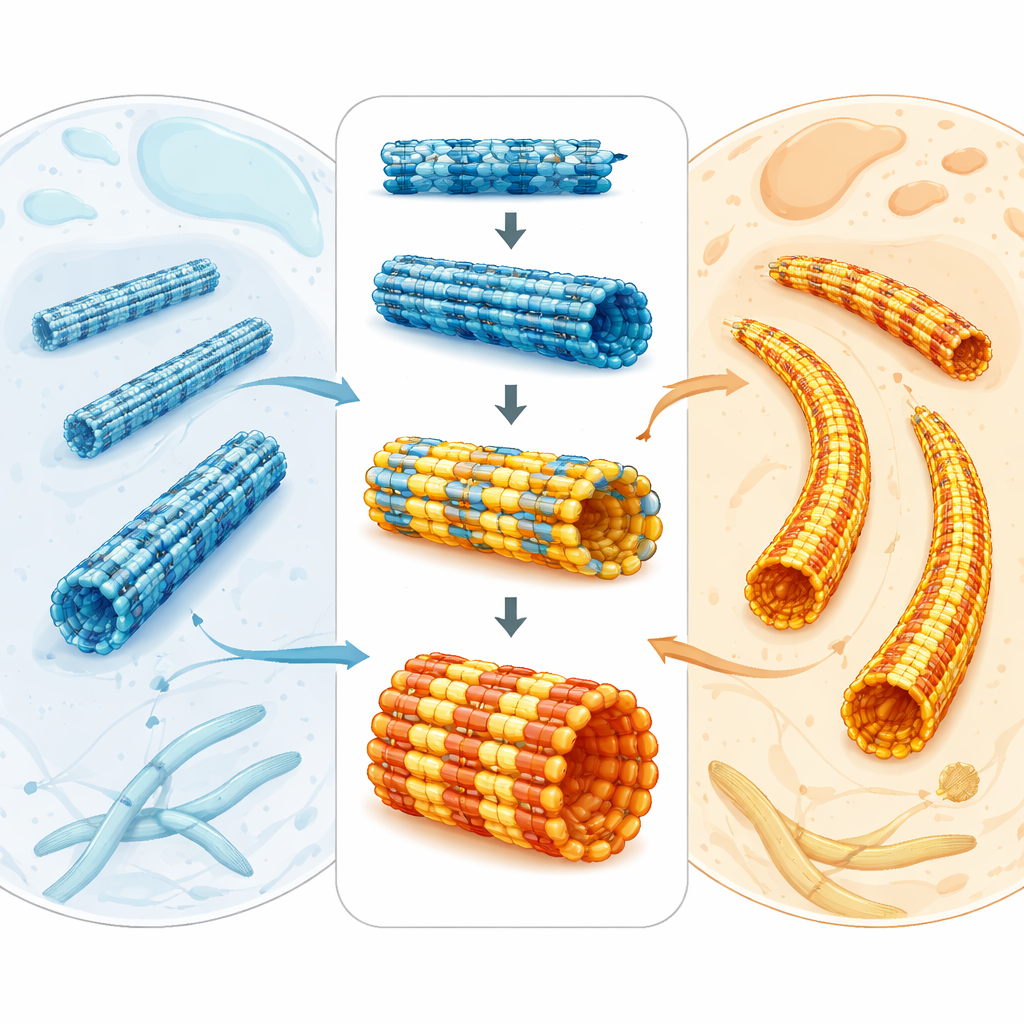
Maleńkie rurki, które nadają kształt zabójczemu pasożytowi
Mikrotubule to puste białkowe rurki, które pomagają komórkom dzielić się, poruszać i utrzymywać formę. Zbudowane są z par jednostek białkowych zwanych tubuliną. Wśród zwierząt, roślin i pasożytów tubulina jest zaskakująco podobna, co utrudnia wyjaśnienie, dlaczego mikrotubule mogą wyglądać i zachowywać się tak różnie u różnych organizmów. W pasożycie malarii Plasmodium falciparum mikrotubule tworzą zróżnicowane układy: niektóre są dynamiczne i działają podczas podziału komórkowego, inne zaś to długie, sztywne podpory pod błoną zewnętrzną pasożyta. Ponieważ struktury te są niezbędne dla wzrostu i transmisji pasożyta, stanowią atrakcyjne cele dla leków przeciwmalarycznych — zwłaszcza w obliczu rosnącej oporności na obecne terapie.
Widzenie tubuliny pasożyta w detalach atomowych
Badacze wyizolowali tubulinę bezpośrednio z P. falciparum i użyli wysokorozdzielczej kriomikroskopii elektronowej, aby zobaczyć, jak składniki te montują się w mikrotubule. Porównali te struktury z dobrze poznanymi mikrotubulami z mózgu ssaków. Na pierwszy rzut oka tubulina pasożyta wygląda praktycznie identycznie jak ludzka i przyjmuje ten sam ogólny fałd. Jednak dokładne porównanie wykryło skupiska drobnych zmian sekwencji wokół kluczowych kieszonek, gdzie wiążą się cząsteczki niosące energię (GTP i GDP) oraz miejsca oddziaływania niektórych leków. Te subtelne przesunięcia zmieniają położenie pobliskich helis i pętli, zwłaszcza na powierzchni dimeru tubuliny, gdzie przyczepiają się inne białka i leki. Praca sugeruje, że choć ogólny plan jest zachowany, lokalne korekty w tubulinie pasożyta delikatnie przeobrażają te ważne miejsca.
Bardziej sztywne rurki dzięki silniejszym bocznym połączeniom
Mikrotubule są polimerami: wiele dimerów tubuliny układa się końcowymi stykami w protofilamenty, a kilka protofilamentów ustawia się obok siebie, tworząc ścianę rurki. Zespół odkrył, że w mikrotubulach pasożyta kontakty wzdłużne wzdłuż każdego protofilamentu wyglądają bardzo podobnie do tych w mikrotubulach mózgowych. Różnica pojawia się w kontaktach bocznych, między sąsiednimi protofilamentami. Chociaż powierzchnia styku jest w istocie nieco mniejsza u pasożyta, symulacje ujawniają, że te boczne połączenia są łącznie silniejsze, co usztywnia sieć. Modelowanie komputerowe fragmentów ściany mikrotubul pokazało, że tubulina pasożyta mniej się wygina i skręca niż tubulina mózgowa. Tomografia elektronowa rzeczywistych końców mikrotubul potwierdziła, że mikrotubule pasożyta mają krótsze, mniej rozszczepione zawijania protofilamentów — cechę charakterystyczną bardziej wytrzymałej rurki.
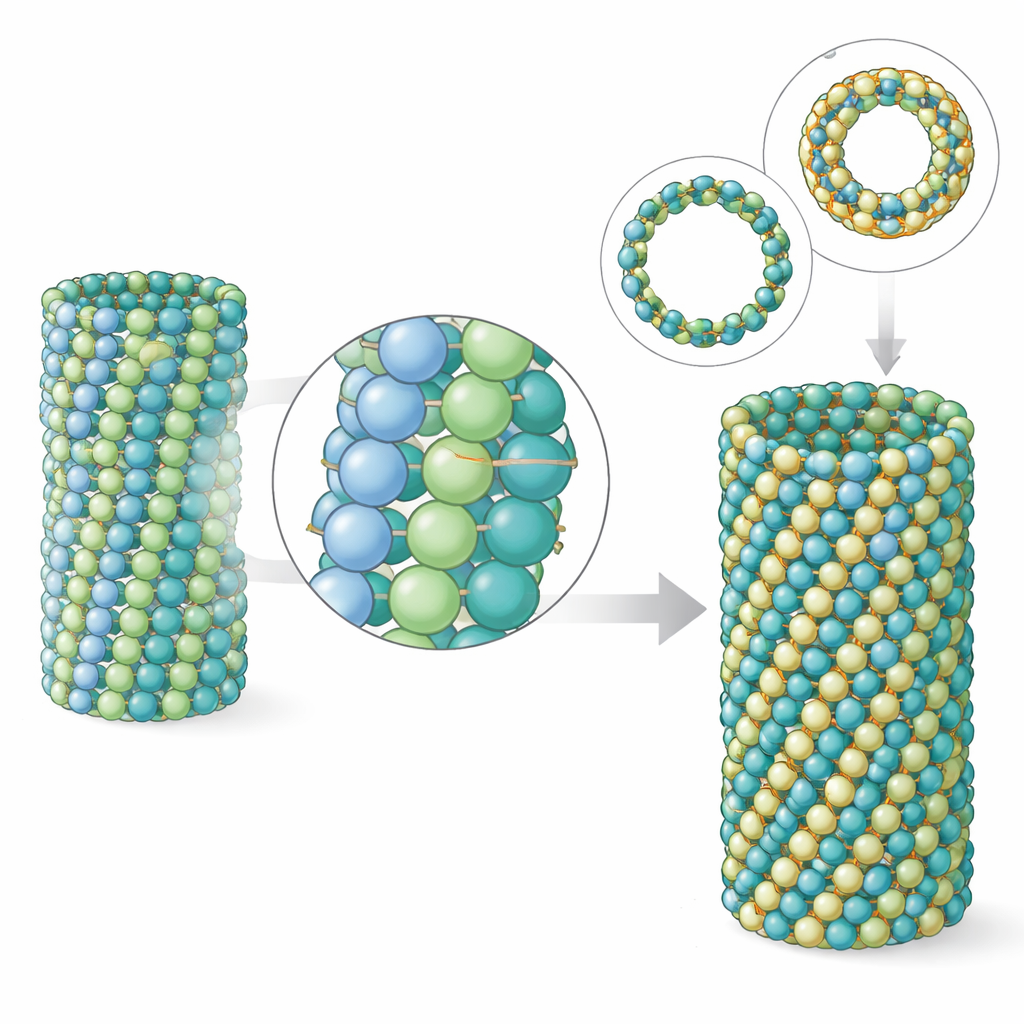
Niezwykłe rozmiary rur pasujące do trybu życia pasożyta
Kolejną uderzającą cechą P. falciparum jest to, że w niektórych stadiach życia jego mikrotubule zawierają więcej jednostek wokół obwodu niż zwykłe 13 spotykane w większości komórek zwierzęcych — często 15, a nawet 17 rzędów protofilamentów. Zespół odtworzył to zachowanie in vitro, zmieniając nukleotyd używany podczas składania. Przy cząsteczce podobnej do GTP, która stabilizuje stan wzrostu, tubulina pasożyta naturalnie preferowała mikrotubule z 15 protofilamentami. Autorzy rozwiązali strukturę tych grubszych rurek i pokazali, jak mieszczą one dodatkowe protofilamenty dzięki lekkiemu przesunięciu sieci, pozostając przy tym prawie idealnie cylindryczne. Porównanie tych laboratoryjnych mikrotubul z 15 protofilamentami i tych obserwowanych we wnętrzu komórek pasożyta wykazało zaskakująco bliskie dopasowanie kształtu i wymiarów, co wskazuje, że właściwości samej tubuliny — a nie koniecznie tłum pomocniczych białek — wystarczają do wygenerowania charakterystycznej architektury pasożyta.
Wskazówki dla przyszłych, specyficznych dla pasożyta leków
W konkluzji badanie wykazało, że ewolucja dostroiła tubulinę pasożyta przez drobne, rozproszone zmiany sekwencji, które łącznie modyfikują mechanikę mikrotubul, ich architekturę i wrażliwość na leki. Te korekty czynią mikrotubule pasożyta bardziej sztywnymi i pozwalają tworzyć niestandardowe rozmiary rurek dopasowane do wymagającego cyklu życiowego, przy jednoczesnym zachowaniu rozpoznawalnego projektu tubuliny. Ważne z medycznego punktu widzenia jest to, że niektóre kieszenie wiążące leki wydają się niemal identyczne u pasożyta i u gospodarza (jak w przypadku leku przeciwnowotworowego paklitakselu), co sugeruje, że są one słabymi celami dla selektywnych leków przeciwmalarycznych. Inne regiony, na przykład obszar przypuszczalnie wiążący związek podobny do herbicydu oryzaliny, wykazują zarówno przesunięcia sekwencji, jak i subtelne przemieszczenia strukturalne, które mogą tłumaczyć, dlaczego mikrotubule pasożyta są tam bardziej wrażliwe niż ludzkie. Zmapowanie tych niuansów daje drogowskaz do projektowania przyszłych leków, które zaburzą „szkielet” pasożyta malarii, pozostawiając w dużej mierze nienaruszone nasze własne komórki.
Cytowanie: Bangera, M., Wu, J., Beckett, D. et al. Adaptations in Plasmodium tubulin determine distinct microtubule architectures, mechanics and drug susceptibility. Nat Commun 17, 2275 (2026). https://doi.org/10.1038/s41467-026-70181-0
Słowa kluczowe: pasożyt malarii, mikrotubule, budowa tubuliny, celowanie leków, kriomikroskopia elektronowa