Clear Sky Science · pl
Składanie kowalencyjnego elementu reaktywnego w biosyntezie fostriecyny obejmuje malonylację-laktonizację przez bifunkcyjną tioestazę oraz enzymatyczną demalonylację
Jak natura buduje maleńki chemiczny element reaktywny
Leki przeciwnowotworowe i antybiotyki często polegają na ułożeniu kilku atomów w odpowiedni sposób — na maleńkim „elemencie reaktywnym”, który wiąże się z białkiem i je wyłącza. Naturalny związek fostriecyna jest takim molekułą, wykazując silne działanie przeciw enzymom biorącym udział w wzroście komórek. Jednak jej złożona budowa utrudnia wytwarzanie i modyfikację w laboratorium. Niniejsze badanie ujawnia, krok po kroku, jak bakterie montują kluczowy element reaktywny fostriecyny, odsłaniając enzymatyczne sztuczki, które chemicy mogą teraz wykorzystać do projektowania nowych leków.
Szczególny hak w silnych naturalnych lekach
Wiele obiecujących leków pochodzących z bakterii glebowych należy do rodziny zwanej poliketydami. W tej rodzinie podgrupa nosi reaktywny pierścień, znany chemikom jako α,β-nienasycony δ-lakton, który działa jak molekularny haczyk. Może tworzyć trwałe wiązanie z określonymi aminokwasami w białkach, wyłączając kluczowe biologiczne przełączniki. W fostriecynie i spokrewnionych związkach ten haczyk występuje wraz z grupą fosforanową, która pomaga im trafiać do konkretnych enzymów kontrolujących podział komórek. Te cechy czynią je atrakcyjnymi kandydatami antynowotworowymi, ale ta sama reaktywność i złożoność strukturalna utrudniają ich syntezę i czynią je niestabilnymi podczas przechowywania.
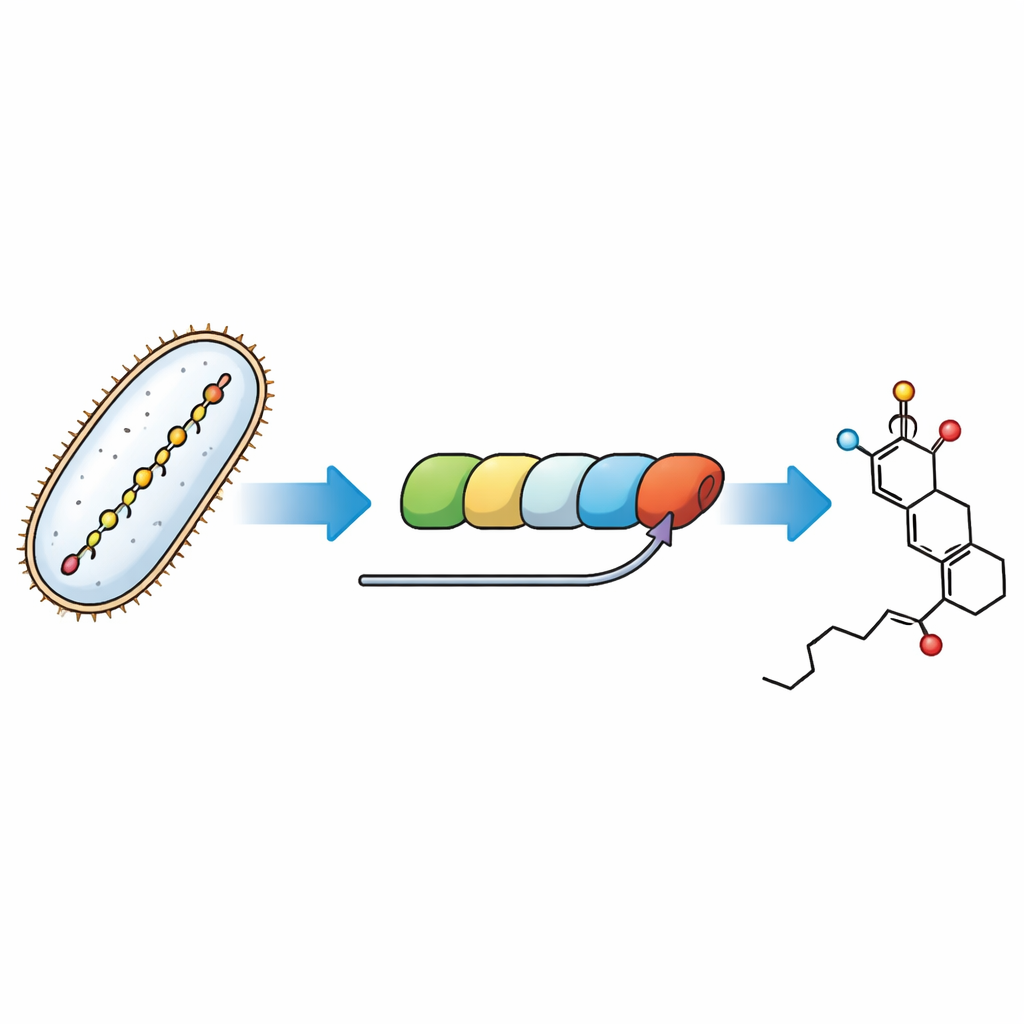
Śledzenie ostatnich etapów molekularnej linii montażowej
Bakterie budują fostriecynę przy pomocy ogromnej modularnej maszyny białkowej zwanej syntazą poliketydową — linii montażowej, w której każde stanowisko wydłuża i modeluje rosnący łańcuch węglowy. Zagadką rozwiązaną tutaj jest to, jak ostatni moduł tej maszyny tworzy pierścień elementu reaktywnego i instaluje tymczasowy „uchwyt” zwany grupą malonylową, który później musi zostać usunięty. Odtwarzając szlak w probówkach z oczyszczonymi enzymami i starannie zaprojektowanymi małocząsteczkowymi substytutami naturalnych pośrednich, badacze mogli obserwować poszczególne kroki i przypisywać je konkretnym częściom linii montażowej.
Wielozadaniowy enzym o niespodziewanym talencie
Zespół odkrył, że ostatnie stanowisko linii montażowej, domena nazwana FosTE, zachowuje się w sposób wcześniej nieobserwowany. Typowe wersje tej domeny po prostu odcinają gotowe produkty od linii. FosTE, w przeciwieństwie do nich, najpierw przechwytuje fragment malonylowy z powszechnego komórkowego budulca i przenosi go na konkretne miejsce tlenowe na rosnącym łańcuchu, a następnie ułatwia jego zagięcie, prowadzące do zamknięcia pierścienia elementu reaktywnego. Zmutowanie jednej reaktywnej reszty seryny w FosTE blokuje obie aktywności. Modele strukturalne wskazują na dwie dodatnio naładowane reszty argininy w centrum aktywnym, które przytrzymują fragment malonylowy i ustawiają go do transferu — funkcje zwykle wykonywane przez inny typ enzymu. Zmiana tych arginin na obojętne reszty usuwa etap transferu malonylu, pozostawiając w dużej mierze nienaruszone podstawowe formowanie pierścienia, co potwierdza ich krytyczną rolę.
Utrwalenie elementu reaktywnego i zapobieganie stratom
Gdy pierścień powstaje i niesie swoją tymczasową grupę malonylową, inny enzym, FosM, musi usunąć tę grupę, aby odsłonić w pełni uzbrojony element reaktywny. Badanie pokazuje, że FosM działa wydajnie tylko po tym, jak jeszcze inny enzym, kinaza o szerokiej swoistości nazwana FosH, doda fosforan w pobliskim miejscu cząsteczki. Gdy badacze podali sam malonylowany pierścień do FosM, zaobserwowano tylko umiarkowaną konwersję. Dodanie najpierw FosH doprowadziło do niemal całkowitego usunięcia grupy malonylowej i powstania końcowej jednostki reaktywnej. Co ważne, FosH może także fosforylować powiązane „odpadowe” pośredniki powstające w wyniku reakcji ubocznych, ratując je, aby mogły być poprawnie przetworzone zamiast zostać utracone jako produkty ślepego toru.
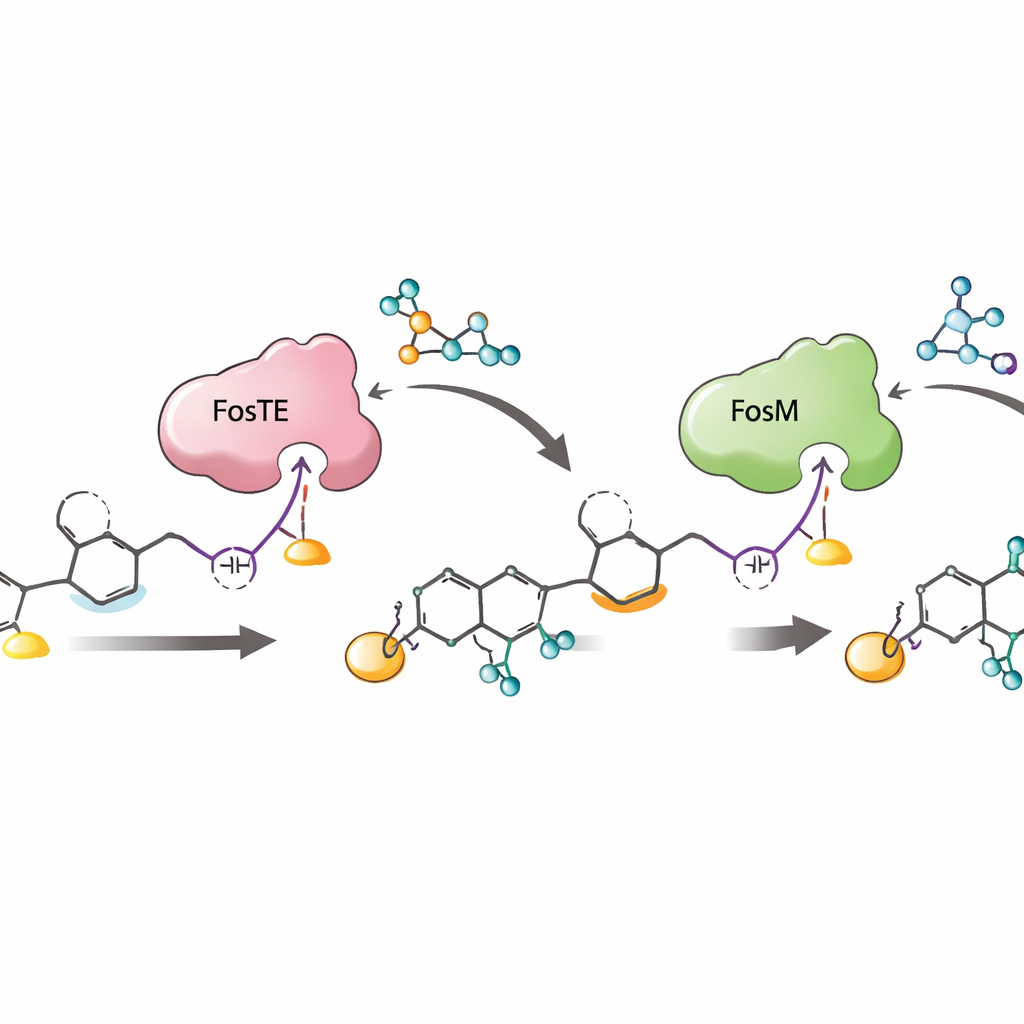
Dlaczego ta enzymatyczna choreografia ma znaczenie
W sumie praca ujawnia ściśle zaaranżowaną sekwencję: wydłużanie łańcucha na linii montażowej, dodanie malonylu i zamknięcie pierścienia napędzane przez FosTE, fosforylacja przez FosH i wreszcie demalonylacja wywołana przez FosM. Ten porządek nie tylko efektywnie konstruuje delikatny element reaktywny, ale także chroni niestabilne pośredniki przed rozpadem i maksymalizuje produkcję pożądanej, sfosforylowanej formy, która jest najaktywniejsza jako kandydat lekowy. Pokazując, jak jedna domena enzymatyczna może jednocześnie ozdabiać i uwalniać rosnącą cząsteczkę — oraz jak partnerujące enzymy dopracowują i ratują reaktywne pośredniki — badanie oferuje plan działania dla inżynierii nowych poliketydów niosących elementy reaktywne i dla budowy krótszych, bardziej wydajnych dróg syntezy złożonych środków przeciwnowotworowych, takich jak fostriecyna.
Cytowanie: Nguyen, L.N.K.T., Schlotte, L., Hoffmann, J. et al. Covalent warhead assembly in fostriecin biosynthesis involves malonylation-lactonisation by a bifunctional thioesterase and enzymatic demalonylation. Nat Commun 17, 2365 (2026). https://doi.org/10.1038/s41467-026-70144-5
Słowa kluczowe: fostriecyna, biosynteza poliketydów, inżynieria enzymów, reaktywne grupy w produktach naturalnych, synteza chemoenzymatyczna