Clear Sky Science · pl
Sygnalizacja peptydu natriuretycznego C typu/guanylylocyklazy‑B w śródbłonku zapobiega nadciśnieniu płucnemu tętniczemu
Dlaczego to ma znaczenie dla płuc i serca
Nadciśnienie płucne tętnicze to rzadkie, lecz śmiertelne schorzenie, w którym naczynia krwionośne prowadzące krew z serca do płuc stają się niebezpiecznie zwężone i pogrubione. To obciążenie może prowadzić do niewydolności prawej komory serca, a w konsekwencji do zgonu. Obecne leki głównie rozkurczają te naczynia, ale niewiele robią, by zatrzymać postępujące uszkodzenie ściany naczynia. Badanie opisane w tym artykule odkrywa naturalny sygnał ochronny wytwarzany przez komórki wyściełające naczynia płucne i pokazuje, jak wzmocnienie tego sygnału mogłoby zarówno zapobiegać, jak i leczyć chorobę.
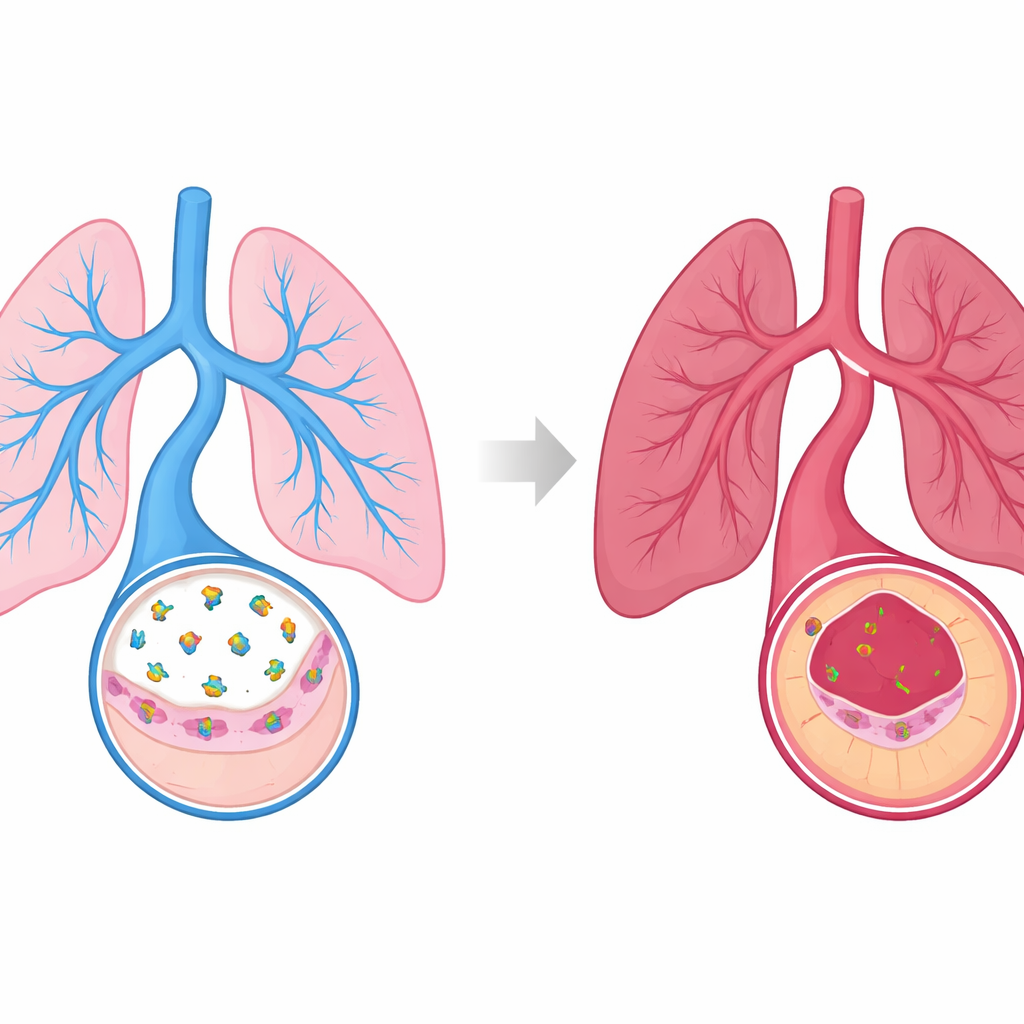
Ochronne przesłanie od wyściółki naczynia
Wewnętrzna wyściółka naczyń tworzy się z komórek śródbłonka, które nieustannie komunikują się z otaczającą warstwą mięśniową, aby utrzymać naczynia otwarte i zdrowe. Autorzy skupili się na niewielkim hormonie zwanym peptydem natriuretycznym typu C (CNP), który te komórki śródbłonka uwalniają w płucach. CNP działa lokalnie na białkowy receptor guanylylocyklazę‑B (GC‑B) na tych samych komórkach, uruchamiając przekaźnik chemiczny, który pomaga naczyniom się rozkurczać i opierać urazom. Badając myszy narażone na dwa różne czynniki wywołujące nadciśnienie płucne — toksyczny chemiczny czynnik i powietrze ubogie w tlen — badacze odkryli, że płuca rozwijające chorobę miały znacznie niższe poziomy zarówno CNP, jak i jego receptora w porównaniu ze zdrowymi płucami.
Wyłączenie sygnału pogarsza chorobę u zwierząt
Aby sprawdzić, czy utrata sygnalizacji CNP rzeczywiście napędza chorobę, zespół stworzył myszy, u których albo sam CNP, albo jego receptor GC‑B został usunięty tylko z komórek śródbłonka. Gdy te myszy zostały wystawione na te same czynniki chorobotwórcze, ich tętnice płucne zwęziły się bardziej, ciśnienie w prawej stronie serca podniosło się bardziej, a mięsień sercowy pogrubiał się bardziej niż u myszy kontrolnych. Dla kontrastu, usunięcie receptora jedynie z otaczających komórek mięśni gładkich nie pogorszyło choroby. To wskazało kluczową rolę działania CNP na same komórki śródbłonka, a nie bezpośrednio na warstwę mięśniową.
Jak sygnał uspokaja ściany naczyń
Patrząc bliżej, badacze odkryli, że szlak CNP–GC‑B w komórkach śródbłonka działa jak hamulec dla kilku szkodliwych reakcji. Bez niego te komórki wytwarzały więcej endoteliny‑1, silnie obkurczającej naczynia molekuły, oraz wyższe poziomy mediatorów zapalnych, takich jak interleukina‑6, CCL2 i TGF‑β1. W eksperymentach z hodowlami komórek przywrócenie CNP osłabiało te sygnały, ale tylko jeśli obecny był receptor GC‑B. CNP pomagał również przywrócić równowagę między dwoma konkurującymi systemami kontroli wzrostu w komórkach, znanymi jako SMAD2/3 i SMAD1/5/9, które wspólnie decydują, czy ściana naczynia pozostanie stabilna, czy ulegnie pogrubieniu. Gdy sygnalizacja CNP była nienaruszona, geny związane ze zdrowymi, nieprzerostowymi tętnicami pozostawały aktywne; gdy jej brakowało, równowaga przesuwała się w stronę nadmiernego wzrostu i bliznowacenia.
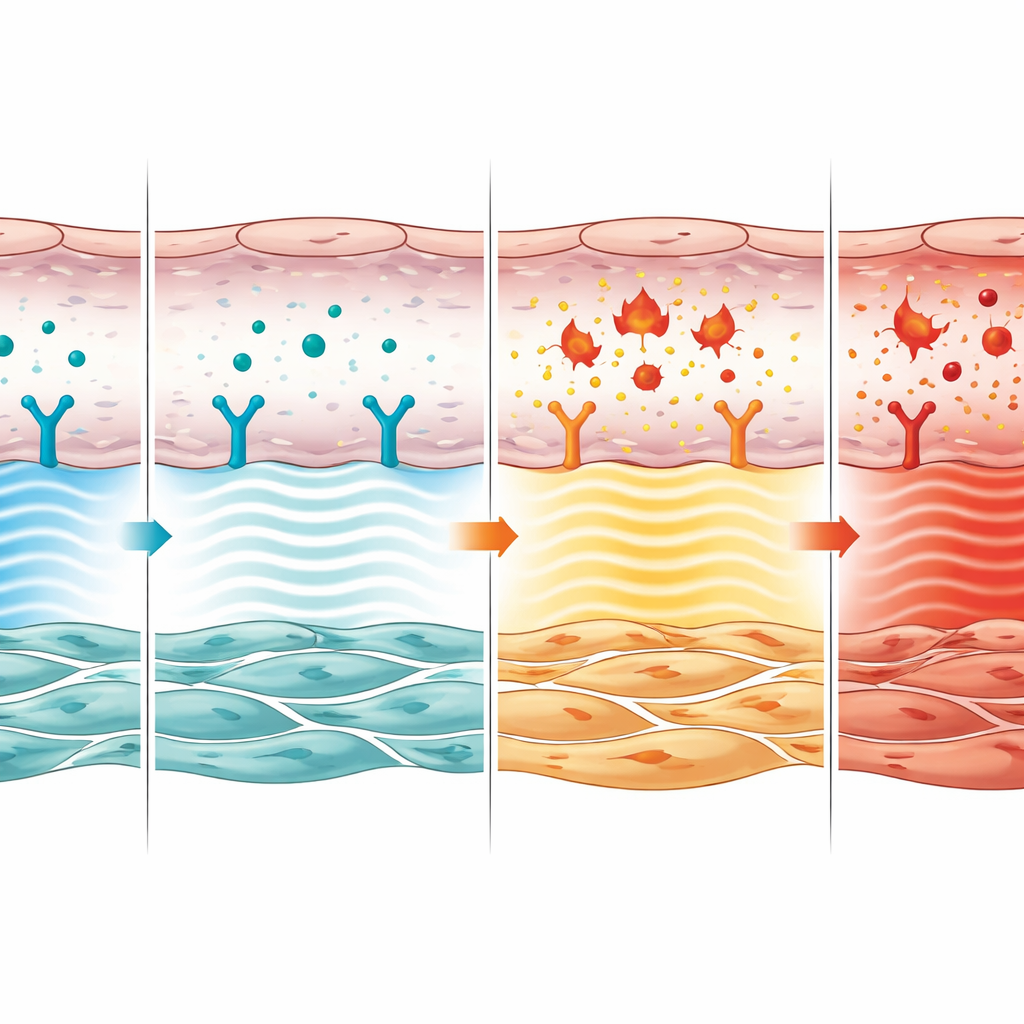
Z rozmowy komórek do przebudowy naczyń
Zespół następnie zapytał, jak ten śródbłonkowy sygnał wpływa na sąsiednie komórki mięśni gładkich, które faktycznie pogrubiają ścianę naczynia. Pokazali, że cząsteczki chemiczne uwalniane z prawidłowych, reagujących na CNP komórek śródbłonka hamowały wzrost i migrację komórek mięśni gładkich w warunkach laboratoryjnych. Gdy receptor CNP został usunięty ze śródbłonka, te sygnały zamiast tego sprzyjały mnożeniu i przemieszczaniu się komórek mięśni gładkich, naśladując przebudowę ściany naczynia obserwowaną w chorobie. W płucach myszy tętnice pozbawione śródbłonkowej sygnalizacji CNP zawierały więcej dzielących się komórek mięśni gładkich i mniej komórek umierających, co potwierdza, że ten szlak normalnie powstrzymuje przerost, który zatyka przepływ krwi.
Testowanie lekopodobnego CNP w ciężkich modelach
Zachęceni tymi wynikami, autorzy przetestowali dłużej działającą formę CNP, nazwaną CNP‑53, podawaną ciągle za pomocą maleńkich pomp u gryzoni. U myszy podawanie CNP‑53 podczas ekspozycji na czynniki chorobotwórcze zapobiegało wzrostom ciśnienia w płucach i pogrubieniu ścian tętnic — ale tylko wtedy, gdy komórki śródbłonka nadal posiadały receptor GC‑B. U szczurów i myszy z wyjątkowo ciężką, przypominającą ludzką postacią nadciśnienia płucnego, rozpoczęcie leczenia CNP‑53 po ustaleniu się choroby obniżało ciśnienia w płucach i poprawiało parametry sercowe. W połączeniu z dwoma istniejącymi lekami — jednym blokującym endoteliny i drugim celującym w powiązany szlak wzrostu — CNP‑53 przynosiło dodatkową korzyść bez obniżania ciśnienia tętniczego poza normę.
Co to znaczy dla przyszłych terapii
Łącznie badanie ujawnia, że naturalny hormon wytwarzany przez wyściółkę naczyń płucnych działa jak strażnik przeciwko nadciśnieniu płucnemu tętniczemu. Gdy sygnał CNP–GC‑B jest zmniejszony, zapalenie, czynniki obkurczające naczynia i szlaki wzrostu wymykają się spod kontroli, pogrubiając ścianę tętnicy i nadwerężając serce. Przywrócenie lub wzmocnienie tego sygnału za pomocą leków opartych na CNP, szczególnie wariantów zaprojektowanych tak, by dłużej utrzymywały się w organizmie, mogłoby otworzyć nową drogę terapeutyczną, która celuje w sam proces chorobowy, zamiast tylko rozkurczać naczynia. Chociaż potrzeba dodatkowych badań, aby przetłumaczyć te odkrycia na terapie dla ludzi, wyniki sugerują, że pomoc w prawidłowej komunikacji wyściółki naczyń może być kluczem do ochrony pacjentów z tym wyniszczającym zaburzeniem płucno‑sercowym.
Cytowanie: Yanagisawa, H., Kuwahara, K., Nakagawa, Y. et al. Endothelial C-type natriuretic peptide/guanylyl cyclase-B signaling prevents pulmonary arterial hypertension. Nat Commun 17, 2331 (2026). https://doi.org/10.1038/s41467-026-70139-2
Słowa kluczowe: nadciśnienie płucne tętnicze, sygnalizacja śródbłonkowa, peptyd natriuretyczny typu C, remodeling naczyń, krążenie płucne