Clear Sky Science · pl
Regulacja translacji przez oksydacyjną desulfurację modyfikacji tRNA
Jak komórki regulują produkcję białek pod stresem
Każda komórka musi zdecydować, które białka wytwarzać, jak szybko to robić i kiedy spowolnić produkcję. W tym badaniu opisano subtelny chemiczny przełącznik na cząsteczkach RNA transportowego (tRNA), który pomaga komórkom ograniczyć syntezę białek, gdy środowisko komórkowe staje się bardziej utleniające, na przykład podczas stanu zapalnego lub zaburzeń metabolicznych. Obserwując zachowanie tego przełącznika w komórkach ssaczych i układach in vitro, badacze ujawniają nowy sposób, w jaki zmiany przypominające uszkodzenia RNA mogą pełnić funkcję sygnału regulacyjnego.
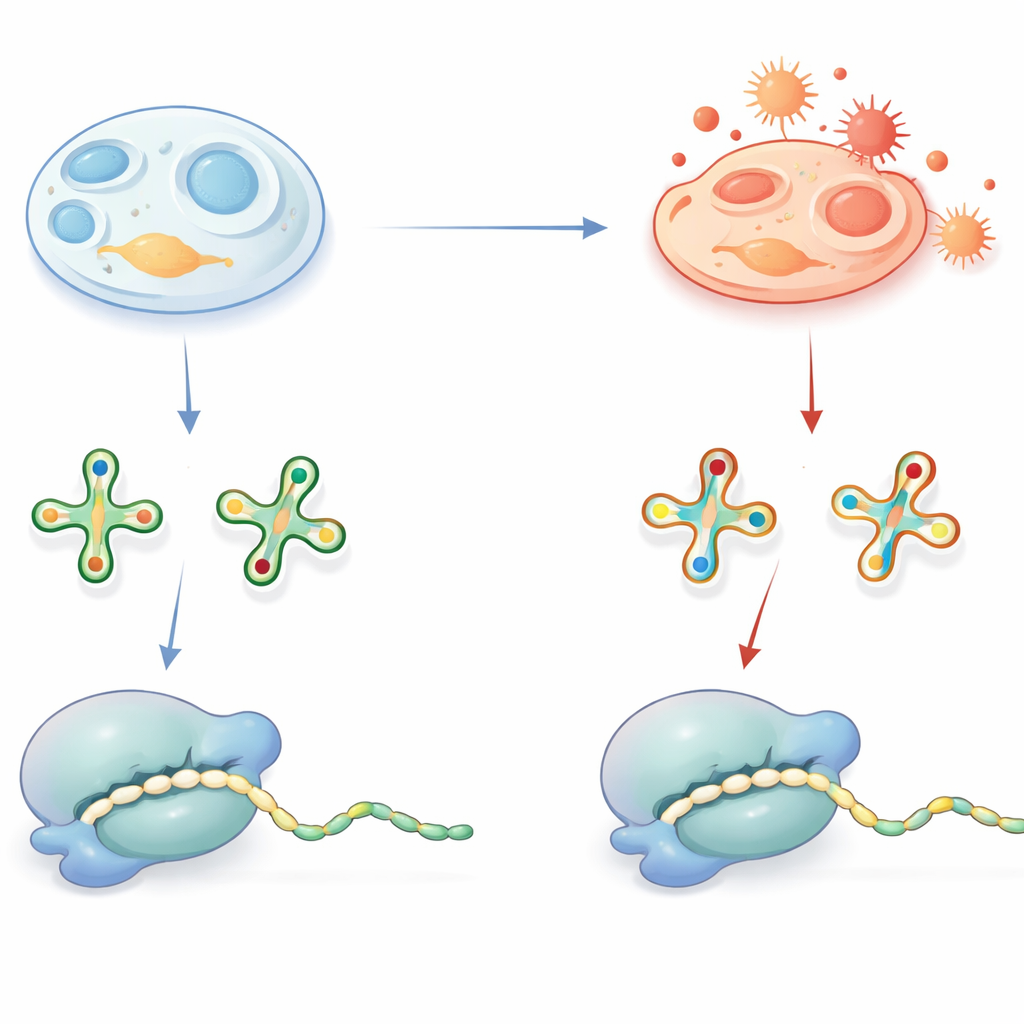
Małe znaki na tRNA o dużych konsekwencjach
tRNA działają jako adaptery, które odczytują trzy-literowe „wyrazy” w mRNA i dostarczają odpowiadające aminokwasy podczas syntezy białek. Aby wykonać tę pracę dokładnie i wydajnie, wiele tRNA nosi specjalne chemiczne dekoracje, zwłaszcza w kluczowej pozycji stykającej się z trzecią literą każdego kodonu. Jedną z powszechnych dekoracji jest grupa zawierająca siarkę na zasadzie urydynowej, często zapisywana jako pochodna 2-tiourydyny. W zdrowych warunkach grupa siarkowa pomaga tRNA rozpoznawać poprawne kodony kończące się literami A lub G i wspiera szybkie, bezbłędne tłumaczenie. Już wiadomo, że defekty tych modyfikacji powodują choroby u ludzi, co podkreśla ich znaczenie.
Kiedy stres oksydacyjny przepisuje tRNA
Grupa siarkowa, która wzmacnia dekodowanie, ma też wadę: jest chemicznie podatna na utlenianie. Zespół zastanowił się, czy wewnątrz komórek ta grupa faktycznie jest usuwana w warunkach oksydacyjnych i co to oznacza dla syntezy białek. Za pomocą czułej spektrometrii mas zidentyfikowali zoxidowane, pozbawione siarki wersje tych zasad tRNA — zwane pochodnymi h2U — w tkankach mysich, mitochondriach świni, bakteriach, drożdżach i różnych liniach komórek ludzkich. Sprytne doświadczenie z domieszką śladu bakteryjnego tRNA wykazało, że te znamiona h2U nie są artefaktami powstającymi podczas przygotowania próbki, lecz tworzą się wewnątrz żywych komórek. Chociaż zoxidowane wersje występowały tylko w ułamku tRNA, ich obfitość różniła się między tkankami i typami komórek, co sugeruje, że stan redoks komórki i zdolności antyoksydacyjne wpływają na częstość takiej konwersji.
Jak zoxidowane tRNA spowalniają linię montażową
Następnie badacze sprawdzili, jak te zmienione tRNA funkcjonują podczas syntezy białek. Chemicznie przekształcili formę zawierającą siarkę w zoxidowaną formę h2U w mieszaninie tRNA i użyli całkowicie odtworzonego ludzkiego układu translacyjnego in vitro. Reporter białkowy, którego produkcja silnie zależała od tych zmodyfikowanych tRNA, wykazał zdecydowanie zmniejszony poziom wytwarzania po desulfuracji tRNA, podczas gdy kontrolny reporter, unikający dotkniętych kodonów, był tłumaczony bez problemu. Testy biochemiczne wyjaśniły przyczynę: zoxidowane tRNA dla lizyny, glutaminy i kwasu glutaminowego były znacznie mniej efektywnie aminoacylowane, podczas gdy odpowiadające tRNA argininowe były w dużej mierze oszczędzone. Co ważne, tRNA niosące h2U nadal pojawiały się w frakcjach związanych z rybosomami (polizosomach) pochodzących z komórek, co wskazuje, że uczestniczą w translacji, ale robią to słabo.
Strukturalny obraz osłabionego dekodowania
Aby zobaczyć dokładnie, jak utlenienie zmienia dekodowanie, zespół zastosował wysokorozdzielczą kriogeniczną mikroskopię elektronową do obrazowania rybosomów bakteryjnych zaprogramowanych ludzkim tRNA dla lizyny i określonymi kodonami. W normalnym stanie z grupą siarkową, zmodyfikowana zasada w pozycji „bujania” tRNA tworzyła albo standardową parę zasad z kodonem kończącym się na A, albo specjalną parę typu wobble z kodonem kończącym się na G, obie mocno osadzone w centrum dekodującym rybosomu. Po desulfuracji ta sama zasada mogła utworzyć tylko pojedynczy słaby kontakt z kodonem kończącym się na A i tworzyła mniej stabilną parę wobble z kodonem kończącym się na G. Eksperymenty wiążące odpowiadały tym strukturom: zoxidowane tRNA lizynowe praktycznie utraciły zdolność rozpoznawania kodonu AAA i znacznie gorzej rozpoznawały kodon AAG. Razem te ustalenia pokazują, że pozornie niewielka modyfikacja chemiczna może przekładać się na specyficzne dla kodonu spowolnienia syntezy białek.
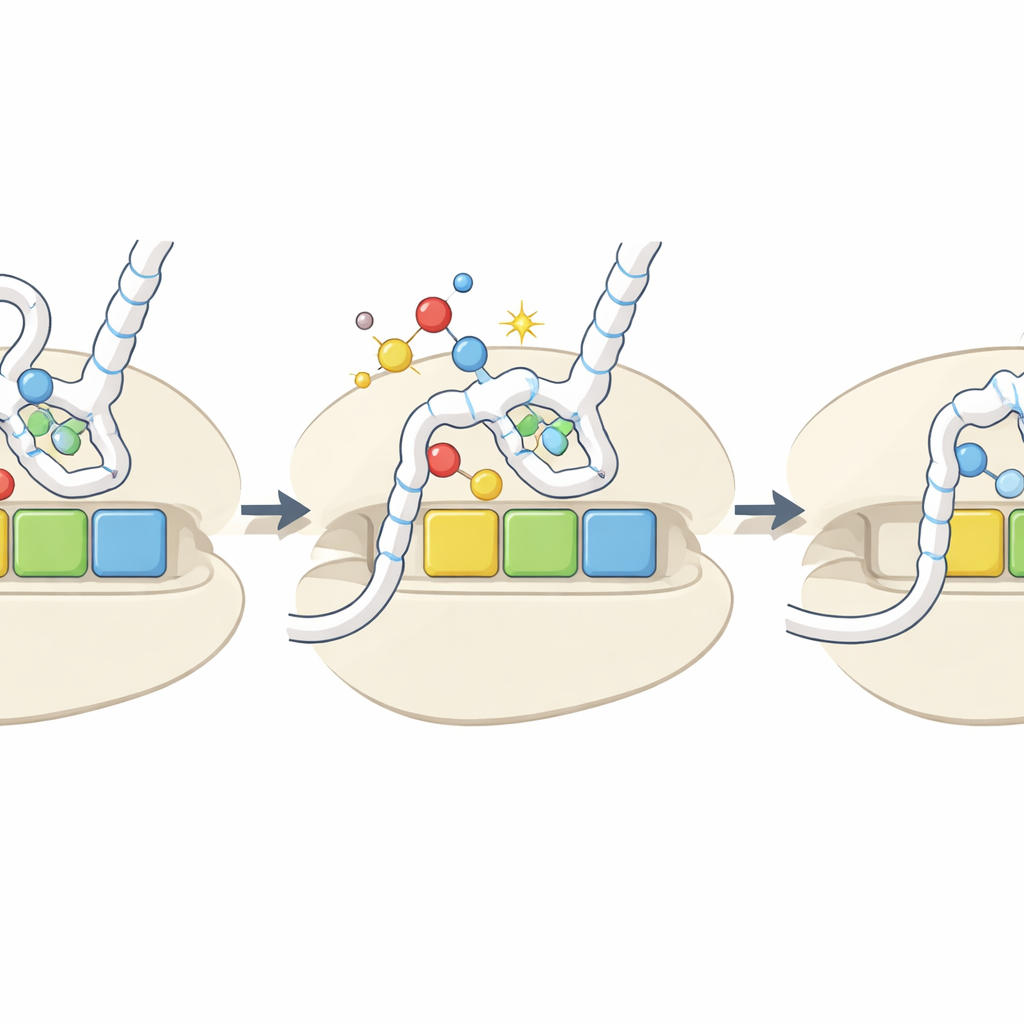
Sygnał uszkodzenia, który staje się pokrętłem regulacyjnym
Podsumowując, badanie sugeruje, że oksydacyjne usunięcie siarki z kluczowych zasad tRNA działa jako wbudowany czujnik środowiska redoks komórki. Pod wpływem stresu oksydacyjnego więcej tRNA przekształca się w formę h2U, które są słabo aminoacylowane i słabo wiążą się z pewnymi kodonami. To selektywnie spowalnia translację przy tych kodonach, co może zmieniać stabilność dotkniętych mRNA, wpływać na składanie białek i uruchamiać ścieżki odpowiedzi na stres, gdy rybosomy zacinają się. Chociaż zoxidowane znaki są stosunkowo rzadkie i ich poziomy nie zawsze gwałtownie rosną pod eksperymentalnym stresem, ich efekty zależne od kodonu i rodzaju aminokwasu oznaczają, że nawet umiarkowane zmiany mogą przełożyć się na zmianę tego, które białka są wytwarzane i z jaką prędkością w trudnych warunkach.
Cytowanie: Mo, Y., Ishiguro, K., Miyauchi, K. et al. Translational regulation by oxidative desulfuration of tRNA modifications. Nat Commun 17, 2125 (2026). https://doi.org/10.1038/s41467-026-70126-7
Słowa kluczowe: modyfikacja tRNA, stres oksydacyjny, synteza białek, regulacja translacji, uszkodzenie RNA